Serotonina
A serotonina [6][7][8] ou 5-hidroxitriptamina (5-HT) é un neurotransmisor monoamina derivado bioquimicamente do aminoácido triptófano, que se encontra principalmente no tracto gastrointestinal, plaquetas, e no sistema nervioso central dos animais, humanos incluídos, pero tamén noutros seres vivos (insectos, fungos, plantas, amebas). É coñecido popularmente que contribúe a producir sensacións de benestar e felicidade, pero ten múltiples funcións.[9]
| Serotonina | |
|---|---|
 | |
 | |
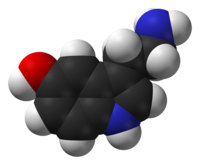 | |
5-Hidroxitriptamina ou | |
Outros nomes 5-HT, Enteramina; Trombocitina, 3-(β-Aminoetil)-5-hidroxiindol, Trombotonina | |
| Identificadores | |
| Número CAS | 50-67-9 |
| PubChem | 5202 |
| ChemSpider | 5013 |
| UNII | 333DO1RDJY |
| KEGG | C00780 |
| MeSH | Serotonin |
| ChEBI | CHEBI:28790 |
| ChEMBL | CHEMBL39 |
| Ligando IUPHAR | 5 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C10H12N2O |
| Masa molecular | 176,215 g/mol |
| Aspecto | po branco |
| Punto de fusión | 121–122 °C (ligroína) [1] |
| Punto de ebulición | 416 ± 30 °C (a 760 Torr) [2] |
| Solubilidade en auga | lixeiramente soluble |
| Acidez (pKa) | 10,16 en auga a 23,5 °C [3] |
| Perigosidade | |
| MSDS | External MSDS |
| LD50 | 750 mg/kg (subcutáneo, ratas),[4] 4500 mg/kg (intraperitoneal, ratas),[5] 60 mg/kg (oral, ratas) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
Aproximadamente o 90% da serotonina total do corpo humano está localizada nas células enterocromafíns do intestino, onde se utiliza para regular os movementos intestinais.[10][11] O resto da serotonina sintetízana as neuronas serotoninérxicas do sistema nervioso central, onde exerce varias funcións, entre as que están: regulación do estado de ánimo, apetito, e sono. A serotonina tamén ten algunhas funcións cognitivas, como intervir nos procesos da memoria e a aprendizaxe. A modulación da serotonina nas sinapses pénsase que é o principal efecto exercido por varias clases de fármacos antidepresivos.
A serotonina segregada polas células enterocromafíns finalmente fíltrase entre os tecidos e chega ao sangue. Alí, é captada activamente polas plaquetas, que a almacenan. Cando as plaquetas se unen a un coágulo, liberan a serotonina, que serve como vasoconstritor e axuda a regular a hemostase e a coagulación sanguínea. A serotonina tamén é un factor de crecemento para algúns tipos de células, o cal lle dá un papel na curación de feridas.
A serotonina metabolízase principalmente orixinando 5-HIAA, fundamentalmente no fígado. O seu metabolismo implica primeiro a oxidación pola monoamino oxidase (MAO) ao seu correspondente aldehido, e despois a oxidación pola aldehido deshidroxenase a 5-HIAA, o derivado indol acético. Este último é despois excretado polos riles. Un tipo de tumor chamado carcinoide, ás veces segrega grandes cantidades de serotonina ao sangue, o que causa varias formas de síndrome carcinoide con diarrea, e problemas cardíacos. Debido ao efecto promotor do crecemento da serotonina sobre os miocitos cardíacos, as persoas con carcinoide secretor de serotonina poden sufrir danos no funcionamento da válvula tricúspide do corazón, causados pola proliferación de miocitos na válvula.
Ademais de nos animais, a serotonina atópase nos fungos e plantas.[12] A presenza da serotonina nos velenos de insectos e espiñas de plantas causa a dor que estes producen, que é un efecto secundario da inxección de serotonina. A serotonina producida polas amebas patóxenas, e os seus efectos sobre o intestino causa diarrea. A súa ampla presenza en moitas sementes e froitas pode servir para estimular o tracto dixestivo para expulsar as sementes.
Funcións
editarA serotonina é un neurotransmisor, e atópase en todos os animais con simetría bilateral, nos que media os movementos intestinais e a percepción do animal da dispoñibilidade de recursos, fundamentalmente alimenticios. En resposta á abundancia ou escaseza de recursos percibida, o crecemento do animal, a reprodución ou o estado de ánimo poden elevarse ou deprimirse.
Dispoñibilidade de alimentos
editarA serotonina funciona como un neurotransmisor no sistema nervioso de animais simples e complexos. Por exemplo, no verme nematodo Caenorhabditis elegans, que se alimenta de bacterias, a serotonina libérase como un sinal en resposta a eventos positivos, por exemplo, atopar unha nova fonte de comida ou nos machos atopar unha femia coa que aparearse. Cando un verme sente bacterias na súa cutícula, libérase dopamina, que o ralentiza; se ten fame, libérase tamén serotonina, que ralentiza ao animal un pouco máis. Estre mecanismo incrementa a cantidade de tempo que os animais pasan en presenza da comida.[13] A liberación de serotonina activa os músculos usados para a alimentación, entanto que a octopamina suprime a activación.[14] A serotonina difunde a neuronas sensibles á serotonina, as cales controlan a percepción que ten o animal da dispoñibilidade de nutrientes. Este sistema foi parcialmente conservado durante os 700 millóns de anos de evolución que separan C. elegans dos humanos. Cando os humanos olen a comida, libérase dopamina que incrementa o apetito. Pero a diferenza dos vermes, a serotonina non incrementa un comportamento anticipatorio nos humanos, senón a serotonina liberada co consumo activa os receptores 5-HT2C nas células produtoras de dopamina. Isto detén a liberación de dopamina por parte destas células, e, por tanto, a serotonina fai diminuír o apetito. As drogas que bloquean os receptores 5-HT2C fan que o corpo non poida facer cesar a sensación de apetito, e están asociadas cun incremento de peso,[15] especialmente en persoas que teñen un número de receptores baixo.[16] A expresión de receptores 5-HT2C no hipocampo segue un ritmo diúrno,[17] igual que a liberación de serotonina no núcleo ventromedial, que está caracterizado por un pico pola mañá cando a motivación para comer é máis forte.[18]
Efectos do seu contido nos alimentos
editarNos humanos, os niveis de serotonina están afectados pola dieta. Un incremento na proporción do triptófano en relación coa fenilalanina e a leucina elevará os niveis de serotonina. Entre as froitas que teñen unha boa proporción destes aminoácidos están: dátiles, papaias e bananas. Alimentos cunha proporción baixa inhiben a produción de serotonina, e entre elas están: trigo integral e pan de centeo.[19] As investigacións realizadas tamén suxiren que tomar unha dieta rica en carbohidratos e baixa en proteínas incrementa a serotonina ao segregar insulina, o que axuda na competición entre aminoácidos.[20] Porén, o incremento do nivel de insulina durante un longo período pode desencadear o comezo da resistencia á insulina, obesidade, diabetes tipo 2, e baixada dos niveis de serotonina.[21][22] Os músculos utilizan moitos dos aminoácidos excepto o triptófano, o que permite que os individuos máis musculosos produzan máis serotonina.[23] Sábese que o mio-inositol, un poliol carbocíclico presente en moitos alimentos, xoga un papel na modulación da serotonina.[24]
No tracto dixestivo
editarO intestino contén moitas células enterocromafíns, que liberan serotonina en resposta á presenza de comida na luz intestinal. Isto fai que o intestino se contraia. As plaquetas no sistema portal hepático de vasos sanguíneos que drenan o intestino recollen o exceso de serotonina.
Se na comida están presentes irritantes, as células enterocromafíns liberan máis serotonina para facer que o intestino se mova máis rápido, é dicir, poden causar diarrea, para que así o intestino se baleire rápido e elimine a substancia nociva. Se a serotonina se libera no sangue con maior rapidez da que as plaquetas poden absorbela, o nivel de serotonina libre no sangue elévase. Isto activa os receptores 5HT3 na zona de activación quimiorreceptora que estimula o vómito.[25] As células enterocromafíns non só reaccionan á comida en mal estado, senón que son tamén moi sensibles ás terapias de irradiación e á quimioterapia anticancerosas. Os fármacos que bloquean o 5HT3 son moi efectivas no control das náuseas e vómitos producidos polo tratamento do cancro, e son considerados o mellor tratamento para isto.[26]
Situación social
editarA cantidade de comida que un animal obtén non só depende da abundancia de comida, senón tamén da capacidade do animal de competir con outros por ese recurso. Isto é especialmente certo nos animais sociais, nos que os individuos máis fortes poderían arrebatarlles a comida aos máis febles. Así, a serotonina non só está implicada na percepción da dispoñibilidade de comida, senón que tamén na do rango social. Se a unha lagosta (crustáceo) se lle inxecta serotonina, compórtase como un animal alfa ou dominante, entanto que a octopamina causa un comportamento de subordinación.[27] Un crustáceo caridoide asustado moverá rapidamente a súa cola para nadar e escapar, e o efecto da serotonina neste comportamento dependerá do status social do animal. A serotonina inhibe a reacción de fuxida nos individuos subordinados, pero amplifícaa nos que son socialmente dominantes ou son individuos illados. A razón disto é que a experiencia social altera a proporción entre os receptores de serotonina (receptores 5-HT) que teñen efectos opostos sobre a resposta de loita ou fuxida. O efecto dos receptores 5-HT1 predomina nos animais subordinados, e o dos receptores 5-HT2 predomina nos dominantes.[28] Nos humanos, os niveis de activación do receptor 5-HT1A no cerebro mostran unha correlación negativa coa agresión,[29] e unha mutación no xene que codifica o receptor 5-HT2A pode duplicar o risco de suicidio nos que teñan ese xenotipo [30] A maioría da serotonina do cerebro non se degrada despois do seu uso, senón que é recollida polas neuronas serotoninérxicas polo transportador de serotonina da súa superficie celular. Certos estudos revelaron que case o 10% da varianza total da personalidade relacionada coa ansiedade depende de variacións sobre onde, cando e en que cantidade expresan as neuronas os transportadores da serotonina [31].
Efectos sobre o comportamento e a reprodución
editarEn C. elegans, a diminución artificial de serotonina ou o incremento de octopamina causa un comportamento típico dunha situación en que hai pouca comida no medio: C. elegans faise máis activo, e suprímese o apareamento e a deposición de ovos, e ocorre o contrario cando se incrementa a serotonina ou diminúe a octopamina.[32] A serotonina é necesaria para un comportamento de apareamento normal,[33] e para a inclinación a deixar de alimentarse para procurar parella.[34] A sinalización serotoninérxica usada para adaptar o comportamento do verme ante os cambios rápidos do ambiente afecta á sinalización similar á da insulina e á vía de sinalización do TGF beta, que controla a adaptación a longo prazo. A serotonina foi tamén identificada como o causante do comportamento de formación de enxames das lagostas (insectos).[35]
Metabolismo óseo
editarNos ratos e humanos, as alteracións nos niveis de serotonina e na sinalización serven para regular a masa ósea.[36][37][38] Os ratos que carecen de serotonina no cerebro teñen osteopenia, pero os ratos que carecen de serotonina no intestino teñen unha densidade ósea alta. Nos humanos os niveis sanguíneos elevados de serotonina están inversamente asociados coa dendidade mineral ósea [39]. A serotonina pode tamén sintetizarse, aínda que en moi baixas cantidades, nas células óseas. A serotonina media as súas accións sobre as células óseas utilizando tres receptores diferentes. Por medio do receptor Htr1b regula negativamente a masa ósea e faino positivamente por medio dos receptores Htr2b e Htr2c. Estes estudos abriron unha nova área de investigación do metabolismo óseo que pode ser potencialmente aproveitado para tratar os trastornos na masa ósea.[40]
Efectos sobre o crecemento
editarNa mosca da froita, na que a insulina regula o nivel de azucre e actúa como factor de crecemento, as neuronas serotoninérxicas regulan o tamaño do corpo do adulto ao afectar á secreción de insulina.[41][42]
Nos humanos, aínda que a insulina controla os niveis de azucre sanguíneos e o IGF regula o crecemento, a serotonina controla a liberación de ambas as hormonas e a serotonina suprime a liberación de insulina nas células beta do páncreas,[43] e a exposición a SSRIs reduce o crecemento fetal.[44] A serotonina humana pode tamén actuar como un factor de crecemento directamente. Os danos no fígado incrementan a expresión celular dos receptores 5-HT2A e 5-HT2B.[45] A serotonina presente no sangue entón estimula o crecemento celular para reparar os danos hepáticos.[46] Os receptores 5HT2B tamén activan os osteocitos, os cales constrúen óso [47] Porén, a serotonina tamén inhibe os osteoblastos, por medio do receptor 5-HT1B.[48]
Factor de crecemento cardiovascular
editarA serotonina provoca a activación da ácido nítrico sintase endotelial e estimula, a través dun mecanismo mediado polo receptor 5-HT1B, a fosforilación dunha proteína quinase en cultivos de células endoteliais aórticas bovinas.[49] No sangue, a serotonina é recollida do plasma polas plaquetas, que a almacenan. Deste modo é activa cando as plaquetas se unen aos tecidos danados, actuando como un vasoconstritor que para a hemorraxia, e tamén como un mitótico de fibrocitos (factor de crecemento), para axudar á curación.[50]
Algúns fármacos agonistas serotoninérxicos tamén causan fibrose en calquera parte do corpo, especialmente na síndrome de fibrose retroperitoneal, e na fibrose de válvula cardíaca.[51] No pasado, foron asociados epidemioloxicamente con estas síndromes tres grupos de fármacos serotonérxicos. Son os fármacos antimigrañas vasoconstritores serotoninérxicos (ergotamina e methysergide),[51] os fármacos supresores do apetito serotoninérxicos (fenfluramina, clorfentermina, e aminorex), e certos agonistas dopaminérxicos anti-Parkinsonianos, os cales tamén estimulan os receptores 5-HT2B serotoninérxicos. Estes inclúen o pergolide e o cabergoline, pero non o específico da dopamina lisuride.[52] Igual que a fenfluramina, algunhas destas drogas (por exemplo o pergolide) foron retiradas do mercado debido aos seus efectos secundarios.[53][54][55][56] Algunhas como cabergoline, que nos Estados Unidos só está aprobado o seu uso para a hiperprolactinemia (non para o párkinson), seguen no mercado porque se usan a baixas doses ás que teñen un risco baixo de producir enfermidades nas válvulas cardíacas.[57]
Efectos locais da súa inxección: velenos e dor
editarA serotonina está asociada coas hemorraxias, e un grande incremento súpeto dos niveis periféricos de serotonina causa dor. A razón de que os velenos das avespas e de certos escorpións teñan serotonina [58][59] pode ser incrementar a dor da súa picada nos animais grandes, e tamén causar unha vasoconstrición letal nas presas pequenas.
Deficiencia
editarOs vermes C. elegans alterados xeneticamente que carecen de serotonina presentan un incremento da súa vida reprodutiva, poden volverse obesos, e ás veces deteñen o seu desenvolvemento no estado larvario.[60][61]
Nos mamíferos a serotonina prodúcena dúas triptófano hidroxilases diferentes, que son: a TPH1, que produce serotonina na glándula pineal [62] e nas células enterocromafíns, e a TPH2 que a produce nos núcleos do rafe e no plexo mientérico. Os ratos alterados xeneticamente que carecen de TPH1 desenvolven unha progresiva perda de forza no corazón, teñen pel pálida e dificultades respiratorias, cansan facilmente, e finalmente morren de insuficiencia cardíaca.[63] Os ratos alterados xeneticamente que carecen de TPH2 son normais no momento do nacemento. Porén, tres días despois parecen ser máis pequenos e febles, e teñen peles máis suaves cos seus irmáns. Nunha liña pura destes ratos, o 50% dos mutantes morreron durante as primeiras catro semanas, pero nunha liña mixta, o 90% sobreviviron. Normalmente, a nai desteta as crías despois da teceira semana, pero os animais mutantes necesitaron cinco semanas. Despois diso, colleron o peso normal e tiveron taxas normais de mortalidade. Hai cambios sutís no sistema nervioso autónomo, pero a diferenza máis obvia cos ratos normais é o incremento de agresividade no coidado materno das crías.[64] A pesar da barreira hematoencefálica, a perda da produción de serotonina no cerebro está compensada parcialmente pola serotonina intestinal. Os cambios de comportamento vense moi potenciados se cruzamos os ratos carentes de TPH1 cos carentes de TPH2 e obtemos ratos que carecen de ambos os encimas TPH.[65]
Nos humanos, unha sinalización defectiva de serotonina no cerebro pode ser a causa da síndrome da morte súbita do lactante. Os científicos do Laboratorio de Bioloxía Moleclar Europeo de Monterotondo, Italia[66] modificaron xeneticamente un rato de laboratorio para que producise baixos niveis do neurotransmisor serotonina. Os resultados que obtiveron mostraron que os ratos sufrían unha diminución da frecuencia cardíaca e outros síntomas da síndrome da morte súbita do lactante, e moitos dos animais morreron a curta idade. Os investigadores agora cren que os niveis baixos de serotonina no tronco cerebral dos animais, a cal controla a frecuencia cardíaca e respiratoria, pode ser a causa da morte súbita.[45] Se as neuronas que producen serotonina (neuronas serotoninérxicas) son anormais nos lactantes, hai un risco de síndrome de morte súbita do lactante.[67]
Investigacións recentes levadas a cabo na Universidade Rockefeller mostran que tanto en pacientes que sofren de depresión coma nos ratos cos que se modeliza ese trastorno, os niveis da proteína p11 están diminuídos. Esta proteína está relacionada coa transmisión da serotonina no cerebro.[68]
No cerebro
editarAnatomía
editarAs neuronas do núcleo do rafe son a principal fonte de secreción de serotonina no cerebro.[69] Os núcleos do rafe son unha agrupación de neuronas distribuídas en 9 pares ao longo de todo o tronco cerebral, centradas arredor da formación reticular.[70] Os axóns das neuronas dos núcleos do rafe forman un sistema neurotransmisor, que atingue case todas as partes do sistema nervioso central. Os axóns das neuronas nos núcleos do rafe inferiores terminan no cerebelo e na medula espiñal, e os axóns dos núcleos do rafe superiores esténdense a todo o cerebro.
Microanatomía
editarA serotonina libérase no espazo entre as neuronas, e difunde no espazo sináptico (de >20 µm) para activar os receptores 5-HT localizados nas dendritas, corpos celulares e terminais presinápticas das neuronas adxacentes.
Receptores
editar- Artigo principal: receptor 5-HT.
Os receptores 5-HT son os receptores para a serotonina. Están localizados nas membranas celulares das neuronas e outras céluas nos animais, e median os efectos da serotonina como ligando endóxeno e dun amplo rango de fármacos e drogas alucinóxenas. Coa excepción do receptor 5-HT3, un ligando con canle iónica de apertura, todos ao demais receptores 5-HT son receptores acoplados á proteína G, 7-TM (ou heptahelicais) receptores que activan unha cascada de segundo mensaxeiro intracelular.[71]
Terminación
editarA acción serotoninérxica termina principalmente por medio da recaptación da serotonina (5-HT) na zona sináptica. Isto realízase por medio do transportador monoamína específico para a serotonina, chamado SERT, na neurona presináptica. Varios axentes poden inhibir a recaptación de serotonina, como o MDMA (éxtase), anfetaminas, cocaína, dextrometorfano (un antitusivo), antidepresivos tricíclicos (TCAs) e inhibidores da recaptación de serotonina selectivos (SSRIs). Un estudo de 2006 da Universidade de Washington suxeriu que un transportador monoamina acabado de descubrir, coñecido como PMAT, podía explicar unha "porcentaxe significativa da recaptación de 5-HT".[72] A diferenza do transportador de alta afinidade SERT, o PMAT é un transportador de baixa afinidade, cun Km aparente de 114 micromoles/L para a serotonina; aproximadamente 230 veces maior có do SERT. Porén, o PMAT, malia a súa relativamente baixa afinidade serotoninérxica, ten unha capacidade de transporte considerablemente maior có SERT, "..resultando que ten unha eficiencia de recaptación aproximadamente comparable á do SERT en sistemas de expresión heterólogos." O estudo tamén suxire que algúns SSRIs, como fluoxetina e sertralina, inhiben o PMAT pero a valores IC50 que superan as concentracións plasmáticas terapéuticas ata en catro ordes de magnitude; por tanto, a monoterapia con SSRI é ineficaz na inhibición de PMAT. Actualmente, non hai ningún fármaco coñecido que inhiba apreciablemente o PMAT nas doses terapéuticas normais. O PMAT tamén transporta dopamina e noradrenalina (norepinefrina), aínda que a valores de Km mesmo maiores cós da serotonina (330–15,000 μmoles/L).
Serotonilación
editarA serotonina pode tamén sinalizar por medio dun mecanismo sen receptor chamado serotonilación, no cal a serotonina modifica proteínas.[43] Este proceso está detrás dos efectos da serotonina sobre os trombocitos no que se modifican encimas sinalizadores chamados GTPases que despois desencadean a liberación do contido de vesículas por exocitose.[73] Un proceso similar explicaría o mecanismo de liberación da insulina pancreática.[43] Os efectos da serotonina sobre o "ton" da musculatura lisa vascular (que é a función pola cal a serotonina recibiu o seu nome) depende da serotonilación de proteínas implicadas no aparato contráctil das células musculares.[74]
Biosíntese
editarNos animais, incluíndo os humanos, a serotonina é sintetizada a partir do aminoácido L-triptófano por unha curta vía metabólica que consta de dous encimas: triptófano hidroxilase (TPH) e L-aminoácido aromático descarboxilase (DDC). A reacción mediada por TPH é o paso limitante da ruta. A primeira reacción consiste en que a TPH transforma o L-triptófano en 5-hidroxi-L-triptófano (5-HTP), reacción na que intervén o O2 e a tetrahidrobiopterina; despois a L-aminoácido aromático descarboxilase transforma o 5-hidroxi-L-triptófano en serotonina (5-HT), reacción na que intervén o fosfato de piridoxal. A TPH existe en dúas formas: TPH1, que se encontra en varios tecidos, e TPH2, que é unha isoforma específica do cerebro.[75]
A serotonina tomada por vía oral non pasa ás vías serotoninérxicas do sistema nervioso central, porque non pode cruzar a barreira hematoencefálica. Porén, o triptófano e o seu metabolito o 5-hidroxitriptófano (5-HTP), a partir do cal se sintetiza a serotonina, pode atravesar dita barreira. Estes axentes están dispoñibles como suplementos dietarios e poden ser efectivos como axentes serotoninérxicos. Un produto da degradación da serotonina é o ácido 5-hidroxiindolacético (5-HIAA), o cal se excreta na urina. Na transformación da serotonina en 5-HIAA intervén o encima monoaminooxidase, consómese O2 e H2O e prodúcese amoníaco e peróxido de hidróxeno. A serotonina e o 5-HIAA son producidos ás veces en cantidades excesivas en certos tumores, e os niveis destas substancias poden medirse na urina como unha proba de detección de ditos tumores.
Drogas que afectan ao sistema 5-HT
editarVarias clases de fármacos teñen como obxectivo o sistema 5-HT, e entre eles están antidepresivos, antipsicóticos, ansiolíticos, antieméticos, e fármacos contra as migrañas, e tamén as drogas psicodélicas e empatóxenos.
Drogas psicodélicas
editarAs drogas psicodélicas psilocina/psilocibina, DMT, mescalina, e LSD son agonistas, principalmente nos receptores 5HT2A e 5HT2C.[76][77] O empatóxeno-entactóxeno MDMA libera serotonina das vesículas sinápticas das neuronas.[78]
Antidepresivo
editarOs fármacos que alteran a serotonina están entre os máis prescribidos na maior parte do mundo. Utilízanse para tratar a depresión, trastornos de ansiedade e fobia social. Os inhibidores da monoaminooxidase (MAOI) impiden a degradación dos neurotransmisores monoamina (como a serotonina), e, por tanto, incrementan as concentracións do neurotransmisor no cerebro. A terapia con MAOI está asociada con moitas reaccións adversas, e os pacientes teñen o risco de sufrir unha emerxencia hipertensiva desencadeada por alimentos con alto contido de tiramina e por certas drogas. Algúns fármacos inhiben a recaptación de serotonina, facendo que permaneza na fenda sináptica durante máis tempo. Os antidepresivos tricíclicos (TCAs) inhiben a recaptación de serotonina e noradrenalina (norepinefrina). Os novos inhibidores selectivos da recaptación de serotonina (SSRIs) teñen menos efectos secundarios e menos interaccións con outros fármacos. Os efectos secundarios inclúen unha diminución da masa ósea en anciáns e un incremento do risco de osteoporose. Porén, non está aínda claro se isto é debido á acción do SSRI sobre a produción de serotonina periférica ou á súa acción no cerebro e aparato dixestivo.[48] Certos fármacos SSRI fan baixar os niveis de serotonina por debaixo do nivel basal despois dun uso crónico, malia producirse un incremento inicial de serotonina. Isto foi relacionado coa observación de que os beneficios do tratamento con SSRIs poden diminuír en pacientes seleccionados despois dun tratamento a longo prazo. Unha interrupción desta medicación xeralmente resolve o problema (ata no 70% dos casos).[79] O novo antidepresivo tianeptina, un potenciador selectivo da recaptación de serotonina, ten o efecto de mellorar o estado de ánimo. Isto é unha evidencia que apoia a teoría de que a serotonina é usada probablemente para regular o grao ou intensidade dos estados de ánimo. De feito, o xene 5-HTTLPR codifica para os transportadores de serotonina no cerebro, con máis transportadores de serotonina facendo que diminúa a duración e magnitude da sinalización serotoninérxica.[80] O polimorfismo do 5-HTTLPR (l/l), que fai que se formen máis transportadores de serotonina, tamén é máis resistente contra a depresión e ansiedade.[81][82]
Aínda que as fobias e a depresión poderían ser atenuadas con fármacos que alteran a serotonina, iso non significa que a situación do individuo mellorase, senón só a precepción que ten o individuo do seu ambiente. Ás veces, un nivel baixo de serotonina pode ser beneficioso; por exemplo no chamado xogo do ultimato, no cal os xogadores con niveis normais de serotonina están máis inclinados a aceptar ofertas inxustas que os outros participantes aos que se lles reduciron artificialmente os seus niveis de serotonina.[83]
Síndrome de serotonina
editarNiveis extremadamente altos de serotonina poden orixinar unha condición chamada síndrome de serotonina, con efectos tóxicos potencialmente letais. Na práctica, tales efectos tóxicos son practicamente imposibles de atinguir cunha sobredose dun só fármaco antidepresivo, e requírese unha combinación de axentes serotoninérxicos, como un SSRI cun MAOI.[84] A intensidade dos síntomas da síndrome de serotonina varía amplamente, e as formas máis leves poden darse mesmo con niveis non tóxicos.[85]
Antieméticos
editarAlgúns antagonistas do 5-HT3, como ondansetron, granisetron, e tropisetron, son importantes axentes antieméticos. Son particularmente importantes no tratamento das náuseas e o vómito que aparecen durante os tratamentos anticancerosos con quimioterapia nos que se utilizan drogas citotóxicas. Outra aplicación é o tratamento de náuseas e vómitos postoperatorios.
En organismos unicelulares
editarUnha variedade de organismos uniceluares utilizan a serotonina para varias funcións. Os inhibidores da captación selectiva de serotonina (SSRIs) son tóxicos para as algas.[86] O parasito gastrointestinal Entamoeba histolytica segrega serotonina, causando unha constante diarrea secretora nalgúns pacientes.[87][88] Os pacientes infaectados con E. histolytica teñen un nivel sérico de serotonina moi alto, que torna aos niveis normais despois de acabada a infección.[89] Ademais, E. histolytica responde á presenza de serotonina facéndose máis virulenta.[90] Isto significa que a secreción de serotonina non só serve para incrementar a diseminación de entoamoebas orixinando diarrea no hóspede, senón tamén para coordinar o seu comportamento de acordo coa densidade da súa poboación, un fenómeno chamado percepción do quórum (quorum sensing). Fóra do hóspede, a densidade de entoamoebas é baixa, e, por tanto, tamén a concentración de serotonina. A escaseza de serotonina indica ás entoamoebas que están fóra do hóspede e fanse menos virulentas para así conservar enerxía. Cando entran nun hóspede, multiplícanse no intestino, e fanse máis virulentas a medida que se incrementa a secreción de serotonina.
Nas plantas
editarNas sementes secas a produción de serotonina é unha maneira de eliminar a acumulación do velenoso amoníaco. O amoníaco únese ao grupo indol do L-triptófano, que despois é descarboxilado pola L-aminoácido aromático descarboxilase para dar triptamina, que é despois hidroxilada pola citocromo P450 monooxixenase, rendendo serotonina.[91]
Porén, como a serotonina é un importante modulador gastrointestinal, pode ser producida polas plantas nos seus froitos como un medio de acelerar o paso das sementes a través do tracto dixestivo dos animais que as comen, do mesmo xeito en que actúan certos froitos e sementes que teñen propiedades laxantes. A serotonina atópase nos cogomelos (fungos), froitas e hortalizas. Atopáronse valores superiores a 25–400 mg/kg nas noces de nogueira (Juglans) e do xénero Carya. Concentracións de 3–30 mg/kg atópanse en plátanos, piña de América, kiwi, ameixas, e tomates. Niveis moderados de 0,1–3 mg/kg atópanse nunha gran variedade de vexetais.[92]
A serotonina é un composto que forma parte do veleno que conteñen as ortigas (Urtica dioica), que causa dor ao ser inxectado na pel da mesma maneira que os velenos de insecto con serotonina que se comentaron máis arriba.
A diferenza dos seus precursores (5-HTP e triptófano), a serotonina non pode cruzar a barreira hematoencefálica, o que significa que a inxestión de serotonina na dieta non ten efecto sobre os seus niveis no cerebro.
Metil-triptaminas e alucinóxenos
editarVarias plantas conteñen serotonina xunto cunha familia relacionada de triptaminas que son metiladas no grupo amino (NH2) e nos grupos (OH), son N-óxidos, ou perden o grupo OH. Estes compostos poden chegar ao cerebro, aínda que unha parte deles é metabolizada polos encimas MAO-B no fígado. Exemplos disto son plantas como as do xénero Anadenanthera que se usan para facer o alucinóxeno yopo. Estes compostos están amplamente presentes nas follas de moitas plantas, e poden servir como disuasorios para os animais que as poderían inxerir.
Historia
editarEn 1935, o italiano Vittorio Erspamer observou que un extracto de células enterocromafíns provocaba a contracción dos intestinos. Algúns pensaban que contiña adrenalina (epinefrina), pero dous anos despois Erspamer demostrou que se trataba dunha amina ata entón descoñecida, que denominou enteramina.[93] En 1948, Maurice M. Rapport, Arda Green, e Irvine Page descubriron unha substancia vasoconstritora no plasma sanguíneo, e como era un axente sérico que afectaba ao ton vascular, denominárona serotonina (sero=soro sanguíneo, ton= ton vascular).[94] En 1952 viuse que a enteramina era a mesma substancia cá serotonina, e a medida que se lle descubrían máis funcións fisiolóxicas, o nome que se fixo preferido no campo farmacolóxico foi a abreviación 5-HT do seu nome químico 5-hidroxitriptamina.[95]
Notas
editar- ↑ Pietra, S.;Farmaco, Edizione Scientifica 1958, Vol. 13, pp. 75–9.
- ↑ Calculated using Advanced Chemistry Development (ACD/Labs) Software V11.02 (©1994–2011 ACD/Labs)
- ↑ Mazák, K.; Dóczy, V.; Kökösi, J.; Noszál, B. (2009). "Proton Speciation and Microspeciation of Serotonin and 5-Hydroxytryptophan". Chemistry & Biodiversity 6 (4): 578–90. PMID 19353542. doi:10.1002/cbdv.200800087.
- ↑ Erspamer, Vittorio (1952). "Enteramina e 5-metossitriptamina. Tossicita. Azione sulla diuresi, sulla pressione del sangue e su alcuni organi a muscolatura liscia". Ricerca Scientifica 22: 694–702.
- ↑ {Cita publicación periódica|título=Increased toxicity of 5-hydroxytryptamine by ethanol in rats and mice|url=https://www.ncbi.nlm.nih.gov/pubmed/5734241%7Crevista=Annales Medicinae Experimentalis Et Biologiae Fenniae|data=1968|ISSN=0003-4479|PMID=5734241|páxina=382–384|volume=46|número=3|nome=T.|apelidos=Tammisto}}
- ↑ PubChem compound Serotonin
- ↑ chemSpider Serotonin
- ↑ CHEBI Serotonin
- ↑ Young SN (2007). "How to increase serotonin in the human brain without drugs". Rev. Psychiatr. Neurosci. 32 (6): 394–99. PMC 2077351. PMID 18043762.
- ↑ King MW. "Serotonin". The Medical Biochemistry Page. Indiana University School of Medicine. Consultado o 2009-12-01.
- ↑ Berger M, Gray JA, Roth BL (2009). "The expanded biology of serotonin". Annu. Rev. Med. 60: 355–66. PMID 19630576. doi:10.1146/annurev.med.60.042307.110802.
- ↑ Kang K, Park S, Kim YS, Lee S, Back K (2009). "Biosynthesis and biotechnological production of serotonin derivatives". Appl. Microbiol. Biotechnol. 83 (1): 27–34. PMID 19308403. doi:10.1007/s00253-009-1956-1.
- ↑ Sawin ER, Ranganathan R, Horvitz HR (2000). "C. elegans locomotory rate is modulated by the environment through a dopaminergic pathway and by experience through a serotonergic pathway". Neuron 26 (3): 619–31. PMID 10896158. doi:10.1016/S0896-6273(00)81199-X.
- ↑ Niacaris T, Avery L (2003). "Serotonin regulates repolarization of the C. elegans pharyngeal muscle". J. Exp. Biol. 206 (Pt 2): 223–31. PMID 12477893. doi:10.1242/jeb.00101.
- ↑ Stahl SM, Mignon L, Meyer JM (2009). "Which comes first: atypical antipsychotic treatment or cardiometabolic risk?". Acta Psychiatr Scand 119 (3): 171–9. PMID 19178394. doi:10.1111/j.1600-0447.2008.01334.x.
- ↑ Buckland PR, Hoogendoorn B, Guy CA, Smith SK, Coleman SL, O'Donovan MC (2005). "Low gene expression conferred by association of an allele of the 5-HT2C receptor gene with antipsychotic-induced weight gain". Am J Psychiatry 162 (3): 613–5. PMID 15741483. doi:10.1176/appi.ajp.162.3.613.
- ↑ Holmes MC, French KL, Seckl JR (1997). "Dysregulation of diurnal rhythms of serotonin 5-HT2C and corticosteroid receptor gene expression in the hippocampus with food restriction and glucocorticoids". J. Neurosci. 17 (11): 4056–65. PMID 9151722.
- ↑ Leibowitz SF (1990). "The role of serotonin in eating disorders". Drugs. 39 Suppl 3: 33–48. PMID 2197074.
- ↑ Abu-Jayyab A. "Nutritional Pharmacology Of Sleep & Depression". SelfGrowth.com. Consultado o 2009-12-02.
- ↑ Young SN (2007). "How to increase serotonin in the human brain without drugs". J Psychiatry Neurosci 32 (6): 394–9. PMC 2077351. PMID 18043762.
- ↑ "www.medicinenet.com".
- ↑ "Insulin Resistance Syndrome (Metabolic Syndrome) Symptoms, Treatments". Arquivado dende o orixinal o 05 de abril de 2012.
- ↑ Grossman, Mary H.; Hart, Cheryle R. (2008). McGraw-Hill - New York, ed. The Feel-Good Diet. p. 64. ISBN 0-07-154849-1.
- ↑ Clements RS, Darnell B (1980). "Myo-inositol content of common foods: development of a high-myo-inositol diet". Am. J. Clin. Nutr. 33 (9): 1954–67. PMID 7416064.
- ↑ Rang, H. P. (2003). Churchill Livingstone, ed. Pharmacology. Edinburgh. p. 187. ISBN 0-443-07145-4.
- ↑ de Wit R, Aapro M, Blower PR (2005). "Is there a pharmacological basis for differences in 5-HT3-receptor antagonist efficacy in refractory patients?". Cancer Chemother Pharmacol 56 (3): 231–8. PMID 15838653. doi:10.1007/s00280-005-1033-0.
- ↑ Kravitz EA (1988). "Hormonal control of behavior: amines and the biasing of behavioral output in lobsters". Science 241 (4874): 1775–81. PMID 2902685. doi:10.1126/science.2902685.
- ↑ Yeh SR, Fricke RA, Edwards DH (1996). "The effect of social experience on serotonergic modulation of the escape circuit of crayfish". Science 271 (5247): 366–9. PMID 8553075. doi:10.1126/science.271.5247.366.
- ↑ Caspi N, Modai I, Barak P, Waisbourd A, Zbarsky H, Hirschmann S, Ritsner M. (2001 Mar). "Pindolol augmentation in aggressive schizophrenic patients: a double-blind crossover randomized study". Int Clin Psychopharmacol. 16 (2): 111–5. PMID 11236069. doi:10.1097/00004850-200103000-00006.
- ↑ Basky, Greg (2000). "Suicide linked to serotonin gene". CMAJ 162 (9): 1343.
- ↑ Lesch KP, Bengel D, Heils A, Sabol SZ, Greenberg BD, Petri S, Benjamin J, Müller CR, Hamer DH, Murphy DL (1996). "Association of anxiety-related traits with a polymorphism in the serotonin transporter gene regulatory region". Science 274 (5292): 1527–31. PMID 8929413. doi:10.1126/science.274.5292.1527.
- ↑ Srinivasan S, Sadegh L, Elle IC, Christensen AG, Faergeman NJ, Ashrafi K (2008). "Serotonin regulates C. elegans fat and feeding through independent molecular mechanisms". Cell Metab. 7 (6): 533–44. PMC 2495008. PMID 18522834. doi:10.1016/j.cmet.2008.04.012.
- ↑ Loer CM, Kenyon CJ (1993). "Serotonin-deficient mutants and male mating behavior in the nematode Caenorhabditis elegans". J. Neurosci. 13 (12): 5407–17. PMID 8254383.
- ↑ Lipton J, Kleemann G, Ghosh R, Lints R, Emmons SW (2004). "Mate searching in Caenorhabditis elegans: a genetic model for sex drive in a simple invertebrate". J. Neurosci. 24 (34): 7427–34. PMID 15329389. doi:10.1523/JNEUROSCI.1746-04.2004.
- ↑ Anstey ML, Rogers SM, Ott SR, Burrows M, Simpson SJ (2009). "Serotonin mediates behavioral gregarization underlying swarm formation in desert locusts". Science 323 (5914): 627–30. PMID 19179529. doi:10.1126/science.1165939. Resumo divulgativo – BBC News.
- ↑ Frost M, Andersen TE, Yadav V, Brixen K, Karsenty G, Kassem M (2010). "Patients with high-bone-mass phenotype owing to Lrp5-T253I mutation have low plasma levels of serotonin". J Bone Miner Res. 25 (3): 673–5. PMID 20200960. doi:10.1002/jbmr.44.
- ↑ Rosen CJ (2009). "Breaking into bone biology: serotonin's secrets". Nat Med. 15 (2): 145–6. PMID 19197289. doi:10.1038/nm0209-145.
- ↑ Frost M, Andersen T, Gossiel F, Hansen S, Bollerslev J, Van Hul W, Eastell R, Kassem M, Brixen K. (2011). "Levels of serotonin, sclerostin, bone turnover markers as well as bone density and microarchitecture in patients with high bone mass phenotype due to a mutation in Lrp5". J Bone Miner Res. 26 (8): 1721–8. PMID 21351148. doi:10.1002/jbmr.376.
- ↑ Mödder UI, Achenbach SJ, Amin S, Riggs BL, Melton LJ 3rd, Khosla S (2010). "Relation of serum serotonin levels to bone density and structural parameters in women". J Bone Miner Res. 25 (2): 415–22. PMC 3153390. PMID 19594297. doi:10.1359/jbmr.090721.
- ↑ Yadav VK, Balaji S, Suresh PS, Liu XS, Lu X, Li Z, Guo XE, Mann JJ, Balapure AK, Gershon MD, Medhamurthy R, Vidal M, Karsenty G, Ducy P. (2010). "Pharmacological inhibition of gut-derived serotonin synthesis is a potential bone anabolic treatment for osteoporosis". Nat Med. 16 (3): 308–12. PMC 2836724. PMID 20139991. doi:10.1038/nm.2098.
- ↑ Kaplan DD, Zimmermann G, Suyama K, Meyer T, Scott MP (2008). "A nucleostemin family GTPase, NS3, acts in serotonergic neurons to regulate insulin signaling and control body size". Genes Dev. 22 (14): 1877–93. PMC 2492735. PMID 18628395. doi:10.1101/gad.1670508.
- ↑ Ruaud AF, Thummel CS (2008). "Serotonin and insulin signaling team up to control growth in Drosophila". Genes Dev. 22 (14): 1851–5. PMC 2735276. PMID 18628391. doi:10.1101/gad.1700708.
- ↑ 43,0 43,1 43,2 Paulmann N, Grohmann M, Voigt JP, Bert B, Vowinckel J, Bader M, Skelin M, Jevsek M, Fink H, Rupnik M, Walther DJ (2009). O'Rahilly, Steve, ed. "Intracellular serotonin modulates insulin secretion from pancreatic beta-cells by protein serotonylation". PLoS Biol. 7 (10): e1000229. PMC 2760755. PMID 19859528. doi:10.1371/journal.pbio.1000229.
- ↑ Davidson S, Prokonov D, Taler M, Maayan R, Harell D, Gil-Ad I, Weizman A (2009). "Effect of exposure to selective serotonin reuptake inhibitors in utero on fetal growth: potential role for the IGF-I and HPA axes". Pediatr. Res. 65 (2): 236–41. PMID 19262294. doi:10.1203/PDR.0b013e318193594a.
- ↑ 45,0 45,1 Lesurtel M, Graf R, Aleil B, Walther DJ, Tian Y, Jochum W, Gachet C, Bader M, Clavien PA (2006). "Platelet-derived serotonin mediates liver regeneration". Science 312 (5770): 104–7. PMID 16601191. doi:10.1126/science.1123842.
- ↑ Matondo RB, Punt C, Homberg J, Toussaint MJ, Kisjes R, Korporaal SJ, Akkerman JW, Cuppen E, de Bruin A (2009). "Deletion of the serotonin transporter in rats disturbs serotonin homeostasis without impairing liver regeneration". Am. J. Physiol. Gastrointest. Liver Physiol. 296 (4): G963–8. PMID 19246633. doi:10.1152/ajpgi.90709.2008.
- ↑ Collet C, Schiltz C, Geoffroy V, Maroteaux L, Launay JM, de Vernejoul MC (2008). "The serotonin 5-HT2B receptor controls bone mass via osteoblast recruitment and proliferation". FASEB J. 22 (2): 418–27. PMID 17846081. doi:10.1096/fj.07-9209com.
- ↑ 48,0 48,1 Yadav VK, Ryu JH, Suda N, Tanaka KF, Gingrich JA, Schütz G, Glorieux FH, Chiang CY, Zajac JD, Insogna KL, Mann JJ, Hen R, Ducy P, Karsenty G (2008). "Lrp5 controls bone formation by inhibiting serotonin synthesis in the duodenum". Cell 135 (5): 825–37. PMC 2614332. PMID 19041748. doi:10.1016/j.cell.2008.09.059. Resumo divulgativo – Science Daily.
- ↑ McDuffie JE, Motley ED, Limbird LE, Maleque MA (2000). "5-hydroxytryptamine stimulates phosphorylation of p44/p42 mitogen-activated protein kinase activation in bovine aortic endothelial cell cultures". J. Cardiovasc. Pharmacol. 35 (3): 398–402. PMID 10710124. doi:10.1097/00005344-200003000-00008.
- ↑ Marieb, Elaine Nicpon (2009). Essentials of human anatomy & physiology (Eighth ed.). Pearson/Benjamin Cummings - San Francisco. p. 336. ISBN 0-321-51342-8.
- ↑ 51,0 51,1 Baskin SI (1991). Principles of cardiac toxicology. Boca Raton: CRC Press. ISBN 0-8493-8809-0. Consultado o 2010-02-03.
- ↑ Jähnichen S, Horowski R, Pertz H. "Pergolide and Cabergoline But not Lisuride Exhibit Agonist Efficacy at Serotonin 5-HT2B Receptors" (PDF). Consultado o 2010-02-03.
- ↑ ADRAC (2004). "Cardiac valvulopathy with pergolide". Aust Adv Drug React Bull 23 (4). Arquivado dende o orixinal o 27 de xuño de 2012. Consultado o 05 de abril de 2012. Free full text Arquivado 27 de xuño de 2012 en Wayback Machine. from the Australian Therapeutic Goods Administration
- ↑ Schade R, Andersohn F, Suissa S, Haverkamp W, Garbe E (2007). "Dopamine agonists and the risk of cardiac-valve regurgitation". N. Engl. J. Med. 356 (1): 29–38. PMID 17202453. doi:10.1056/NEJMoa062222.
- ↑ Zanettini R, Antonini A, Gatto G, Gentile R, Tesei S, Pezzoli G (2007). "Valvular heart disease and the use of dopamine agonists for Parkinson's disease". N. Engl. J. Med. 356 (1): 39–46. PMID 17202454. doi:10.1056/NEJMoa054830.
- ↑ "Food and Drug Administration Public Health Advisory". 2007-03-29. Consultado o 2010-02-07.
- ↑ "MedWatch – 2007 Safety Information Alerts. Permax (pergolide) and generic equivalents". U.S. Food and Drug Administration. March 29, 2007. Arquivado dende o orixinal o 29 de marzo de 2007. Consultado o 2007-03-30.
- ↑ Jaques R, Schachter M (1954). "The presence of histamine, 5-hydroxytryptamine and a potent, slow contracting substance in wasp venom". Br J Pharmacol Chemother 9 (1): 53–8. PMC 1509391. PMID 13149776.
- ↑ Adam KR, Weiss C (1959). "Distribution of 5-hydroxytryptamine in scorpion venoms". Nature 183 (4672): 1398–9. PMID 13657136. doi:10.1038/1831398a0.
- ↑ Ben Arous J, Laffont S, Chatenay D (2009). Brezina, Vladimir, ed. "Molecular and sensory basis of a food related two-state behavior in C. elegans". PLoS ONE 4 (10): e7584. PMC 2762077. PMID 19851507. doi:10.1371/journal.pone.0007584.
- ↑ Sze JY, Victor M, Loer C, Shi Y, Ruvkun G (2000). "Food and metabolic signaling defects in a Caenorhabditis elegans serotonin-synthesis mutant". Nature 403 (6769): 560–4. PMID 10676966. doi:10.1038/35000609.
- ↑ . Huang Z, Liu T, Chattoraj A, Ahmed S, Wang MM, Deng J, Sun X, Borjigin J. Posttranslational regulation of TPH1 is responsible for the nightly surge of 5-HT output in the rat pineal gland. J Pineal Res. 2008 Nov;45(4):506-14. Epub 2008 Aug 13 [1] PMID 18705647
- ↑ Côté F; Thévenot E; Fligny C; et al. (2003). "Disruption of the nonneuronal tph1 gene demonstrates the importance of peripheral serotonin in cardiac function". Proc. Natl. Acad. Sci. U.S.A. 100 (23): 13525–30. PMC 263847. PMID 14597720. doi:10.1073/pnas.2233056100.
- ↑ Alenina N, Kikic D, Todiras M, Mosienko V, Qadri F, Plehm R, Boyé P, Vilianovitch L, Sohr R, Tenner K, Hörtnagl H, Bader M (2009). "Growth retardation and altered autonomic control in mice lacking brain serotonin". Proc. Natl. Acad. Sci. U.S.A. 106 (25): 10332–7. PMC 2700938. PMID 19520831. doi:10.1073/pnas.0810793106.
- ↑ Savelieva KV; Zhao S; Pogorelov VM; et al. (2008). Bartolomucci, Alessandro, ed. "Genetic disruption of both tryptophan hydroxylase genes dramatically reduces serotonin and affects behavior in models sensitive to antidepressants". PLoS ONE 3 (10): e3301. Bibcode:2008PLoSO...3.3301S. PMC 2565062. PMID 18923670. doi:10.1371/journal.pone.0003301.
- ↑ Audero, Enrica; Coppi, Elisabetta; Mlinar, Boris; Rossetti, Tiziana; Caprioli, Antonio; Al Banchaabouchi, Mumna; Corradetti, Renato; Gross, Cornelius (2008). "Sporadic Autonomic Dysregulation and Death Associated with Excessive Serotonin Autoinhibition". Science 321 (5885): 130–133. PMID 18599790. doi:10.1126/science.1157871.
- ↑ Paterson DS, Trachtenberg FL, Thompson EG, Belliveau RA, Beggs AH, Darnall R, Chadwick AE, Krous HF, Kinney HC (2006). "Multiple serotonergic brainstem abnormalities in sudden infant death syndrome". JAMA 296 (17): 2124–32. PMID 17077377. doi:10.1001/jama.296.17.2124.
- ↑ Svenningsson P, Chergui K, Rachleff I, Flajolet M, Zhang X, El Yacoubi M, Vaugeois JM, Nomikos GG, Greengard P (2006). "Alterations in 5-HT1B receptor function by p11 in depression-like states". Science 311 (5757): 77–80. PMID 16400147. doi:10.1126/science.1117571.
- ↑ Frazer, A.; and Hensler, J. G. (1999). "Understanding the neuroanatomical organization of serotonergic cells in the brain provides insight into the functions of this neurotransmitter". En Siegel, G. J. Agranoff, Bernard W.; Fisher, Stephen K.; Albers, R. Wayne; Uhler, Michael D. Basic Neurochemistry (Sixth ed.). Lippincott Williams and Wilkins. ISBN 0-397-51820-X.
En 1964, Dahlstrom e Fuxe (discutido en [2]), usando a técnica de Falck-Hillarp de histofluorescencia, observaron que a maioría dos somas serotoninérxicos se encontraban en grupos de corpos celulares, que previamente se designaran como os núcleos do rafe.
- ↑ O grupo de neuronas dos núcleos do rafe están localizadas ao longo da formación reticular do tronco cerebral desde o mesencéfalo ao bulbo raquídeo, centradas na ponte de Varolio. (Ver imaxe.)
- ↑ Hannon J, Hoyer D (2008). "Molecular biology of 5-HT receptors". Behav. Brain Res. 195 (1): 198–213. PMID 18571247. doi:10.1016/j.bbr.2008.03.020.
- ↑ Zhou M, Engel K, Wang J (2007). "Evidence for significant contribution of a newly identified monoamine transporter (PMAT) to serotonin uptake in the human brain". Biochem. Pharmacol. 73 (1): 147–54. PMC 1828907. PMID 17046718. doi:10.1016/j.bcp.2006.09.008.
- ↑ Walther DJ, Peter JU, Winter S, Höltje M, Paulmann N, Grohmann M, Vowinckel J, Alamo-Bethencourt V, Wilhelm CS, Ahnert-Hilger G, Bader M (2003). "Serotonylation of small GTPases is a signal transduction pathway that triggers platelet alpha-granule release". Cell 115 (7): 851–62. PMID 14697203. doi:10.1016/S0092-8674(03)01014-6.
- ↑ Watts SW, Priestley JR, Thompson JM (2009). Kreindler, James L., ed. "Serotonylation of vascular proteins important to contraction". PLoS ONE 4 (5): e5682. PMC 2682564. PMID 19479059. doi:10.1371/journal.pone.0005682.
- ↑ Walther DJ, Peter JU, Bashammakh S, Hörtnagl H, Voits M, Fink H, Bader M (2003). "Synthesis of serotonin by a second tryptophan hydroxylase isoform". Science 299 (5603): 76. PMID 12511643. doi:10.1126/science.1078197.
- ↑ Titeler M, Lyon RA, Glennon RA (1988). "Radioligand binding evidence implicates the brain 5-HT2 receptor as a site of action for LSD and phenylisopropylamine hallucinogens". Psychopharmacology (Berl.) 94 (2): 213–6. PMID 3127847.
- ↑ Nichols DE (2000). "Role of serotonergic neurons and 5-HT receptors in the action of hallucinogens". En Baumgarten HG, Gothert M. Serotoninergic Neurons and 5-HT Receptors in the CNS. Santa Clara, CA: Springer-Verlag TELOS. ISBN 3-540-66715-6.
- ↑ Johnson MP, Hoffman AJ, Nichols DE (1986). "Effects of the enantiomers of MDA, MDMA and related analogues on [3H]serotonin and [3H]dopamine release from superfused rat brain slices". Eur. J. Pharmacol. 132 (2–3): 269–76. PMID 2880735. doi:10.1016/0014-2999(86)90615-1.
- ↑ Benmansour S, Cecchi M, Morilak DA, Gerhardt GA, Javors MA, Gould GG, Frazer A (1999). "Effects of chronic antidepressant treatments on serotonin transporter function, density, and mRNA level". J. Neurosci. 19 (23): 10494–501. PMID 10575045.
- ↑ Beitchman J, Baldassarra L, Mik H, De Luca V, King N, Bender D, Ehtesham S, Kennedy J (2011). "Serotonin Transporter Polymorphisms and Persistent, Pervasive Childhood Aggression". The American Journal of Psychiatry 163 (6): 1103–5. PMID 16741214. doi:10.1176/appi.ajp.163.6.1103.
- ↑ Pezawas, L.; Meyer-Lindenberg, A.; Drabant, E. M.; Verchinski, B. A.; Munoz, K. E.; Kolachana, B. S.; Egan, M. F.; Mattay, V. S. et al (2005). "5-HTTLPR polymorphism impacts human cingulate-amygdala interactions: A genetic susceptibility mechanism for depression". Nature Neuroscience 8 (6): 828–834. doi:10.1038/nn1463. PMID 15880108.
- ↑ Schinka, J. A.; Busch, R. M.; Robichaux-Keene, N. (2004). "A meta-analysis of the association between the serotonin transporter gene polymorphism (5-HTTLPR) and trait anxiety". Molecular Psychiatry 9 (2): 197–202. doi:10.1038/sj.mp.4001405. PMID 14966478.
- ↑ Crockett MJ, Clark L, Tabibnia G, Lieberman MD, Robbins TW (2008). "Serotonin modulates behavioral reactions to unfairness". Science 320 (5884): 1739. PMC 2504725. PMID 18535210. doi:10.1126/science.1155577. Resumo divulgativo.
- ↑ Isbister, G. K.; Bowe, S. J.; Dawson, A.; Whyte, I. M. (2004). "Relative toxicity of selective serotonin reuptake inhibitors (SSRIs) in overdose". J. Toxicol. Clin. Toxicol. 42 (3): 277–85. PMID 15362595. doi:10.1081/CLT-120037428.
- ↑ Dunkley EJ, Isbister GK, Sibbritt D, Dawson AH, Whyte IM (2003). "The Hunter Serotonin Toxicity Criteria: simple and accurate diagnostic decision rules for serotonin toxicity". QJM 96 (9): 635–42. PMID 12925718. doi:10.1093/qjmed/hcg109.
- ↑ Johnson DJ, Sanderson H, Brain RA, Wilson CJ, Solomon KR (2007). "Toxicity and hazard of selective serotonin reuptake inhibitor antidepressants fluoxetine, fluvoxamine, and sertraline to algae". Ecotoxicol. Environ. Saf. 67 (1): 128–39. PMID 16753215. doi:10.1016/j.ecoenv.2006.03.016.
- ↑ McGowan K, Kane A, Asarkof N, Wicks J, Guerina V, Kellum J, Baron S, Gintzler AR, Donowitz M (1983). "Entamoeba histolytica causes intestinal secretion: role of serotonin". Science 221 (4612): 762–4. PMID 6308760. doi:10.1126/science.6308760.
- ↑ McGowan K, Guerina V, Wicks J, Donowitz M (1985). "Secretory hormones of Entamoeba histolytica". Ciba Found. Symp. 112: 139–54. PMID 2861068.
- ↑ Banu N, Zaidi KR, Mehdi G, Mansoor T (2005). "Neurohumoral alterations and their role in amoebiasis". Indian J. Clin Biochem 20 (2): 142–5. doi:10.1007/BF02867414.
- ↑ Acharya DP, Sen MR, Sen PC (1989). "Effect of exogenous 5-hydroxytryptamine on pathogenicity of Entamoeba histolytica in experimental animals". Indian J. Exp. Biol. 27 (8): 718–20. PMID 2561282.
- ↑ Schröder P, Abele C, Gohr P, Stuhlfauth-Roisch U, Grosse W. (1999). "Latest on enzymology of serotonin biosynthesis in walnut seeds". Adv Exp Med Biol. Advances in Experimental Medicine and Biology 467: 637–644. ISBN 978-0-306-46204-7. PMID 10721112. doi:10.1007/978-1-4615-4709-9_81.
- ↑ Feldman, J. M.; Lee, E. M. (1985). "Serotonin content of foods: effect on urinary excretion of 5-hydroxyindoleacetic acid". Am. J. Clin. Nutr. 42 (4): 639–43. PMID 2413754.
- ↑ Negri L (2006). "[Vittorio Erspamer (1909–1999)]". Med Secoli (en Italian) 18 (1): 97–113. PMID 17526278.
- ↑ Rapport MM, Green AA, Page IH (1948). "Serum vasoconstrictor, serotonin; isolation and characterization". J. Biol. Chem. 176 (3): 1243–51. PMID 18100415.
- ↑ Feldberg W, Toh CC (1953). "Distribution of 5-hydroxytryptamine (serotonin, enteramine) in the wall of the digestive tract". J. Physiol. (Lond.) 119 (2–3): 352–62. PMC 1392800. PMID 13035756.
Véxase tamén
editarLigazóns externas
editar- Serotonin bound to proteins in the PDB
- PsychoTropicalResearch Extensive reviews on serotonergic drugs and Serotonin Syndrome.
- Molecule of the Month: Serotonin at University of Bristol
- 60-Second Psych: No Fair! My Serotonin Level Is Low, Scientific American
- Serotonin Test Interpretation on ClinLab Navigator.
- Tryptophan hydroxylase-2 gene variation influences personality traits and disorders related to emotional dysregulation at the National Center for Biotechnology Information.