Paracetamol
O paracetamol (DCI) ou acetaminofén (acetaminofeno) é un fármaco con propiedades analxésicas, sen propiedades antiinflamatorias clinicamente significativas. Actúa inhibindo a síntese de prostaglandinas, mediadores celulares responsables da aparición da dor. Ademais, ten efectos antipiréticos. Preséntase habitualmente en forma de cápsulas, comprimidos, supositorios ou pingas de administración oral.
| Paracetamol | |
|---|---|
 | |
| Identificadores | |
Se cre que pode requirir tratamento, por favor, consúltello ao médico. |
É un ingrediente frecuente dunha serie de produtos contra o arrefriado común e a gripe. A dose estándar é case segura, pero o seu baixo prezo e ampla dispoñibilidade deron como resultado frecuentes casos de sobredosificación. Nas doses indicadas o paracetamol non afecta á mucosa gástrica nin á coagulación sanguínea ou os riles, pero si ao fígado, severamente.
A diferenza dos analxésicos opioides, non provoca euforia nin altera o estado de humor do paciente. Do mesmo xeito que os antiinflamatorios non esteroideos (AINEs), non se asocia con problemas de adicción, tolerancia e síndrome de abstinencia.
Os nomes paracetamol e acetaminofén pertencen á historia deste composto e proveñen da nomenclatura tradicional da química orgánica, N-acetil-para-aminofenol e para-acetil-aminofenol.
Segundo as recomendacións de 1993 da IUPAC, o nome deste composto é N-(4-hidroxifenil)etanamida.
Historia
editarNa antigüidade e durante o medievo, os únicos axentes antipiréticos coñecidos eran compostos presentes na cortiza do salgueiro (unha familia de compostos coñecidos como salicilinas, os cales finalmente deron lugar ao ácido acetilsalicílico), e outros contidos na cortiza da quina. A cortiza da quina así mesmo era usada para a obtención de quinina, composto con actividade antimalaria. A quinina en si mesma tamén ten actividade antipirética. Os esforzos para illar e purificar a salicilina e o ácido salicílico tiveron lugar durante mediados e finais do século XIX.
Cando a quina empezou a escasear na década de 1880, a xente empezou a buscar alternativas. Dous axentes antipiréticos alternativos foron desenvolvidos nos anos 1880: a acetanilida en 1886 e a fenacetina en 1887. Nese momento, o paracetamol xa fora sintetizado por Harmon Morse de Northrop mediante a redución do p-nitrofenol en ácido acético glacial. Este feito produciuse en 1873, pero o paracetamol non se usou con fins médicos durante dúas décadas. En 1893, o paracetamol foi atopado nos ouriños de persoas que inxeriran fenacetina e foi illado como un composto branco e cristalino de sabor amargo. En 1899, o paracetamol foi identificado como un metabolito da acetanilida. Devandito descubrimento foi amplamente ignorado naquel momento.
En 1946, o Instituto para o Estudo de Drogas Analxésicas e Sedantes outorgou unha subvención ao Ministerio de Sanidade de Nova York para estudar os problemas asociados co uso de analxésicos. Bernard Brodie e Julius Axelrod foron asignados para investigar por que compostos non relacionados coa aspirina daban lugar a metahemoglobinemia, unha síndrome non letal consistente na deformación da molécula da hemoglobina e por tanto causante da súa incapacidade para transportar osíxeno de forma efectiva. En 1948 ambos os investigadores relacionaron o uso da acetanilida coa metahemoglobinemia e deduciron que o seu efecto analxésico era debido ao seu metabolito paracetamol. Propuxeron o uso de paracetamol (acetaminofén) xa que este non tiña os efectos tóxicos da acetanilida.[1]
O paracetamol foi posto á venda nos Estados Unidos en 1955 baixo o nome comercial Tylenol. En 1956, pastillas de 500 mg de paracetamol puxéronse á venda no Reino Unido baixo o nome de Panadol, producido por Frederick Stearns & Co, unha filial de Sterling Drug Inc. Ao principio Panadol estivo dispoñible unicamente con receita médica, para o alivio da dor e a febre, e foi anunciado como "inocuo para o estómago", debido a que outros analxésicos da época contiñan ácido acetilsalicílico, un irritante coñecido do estómago, pero xa en abril do 2009 a Administración de Alimentos e Medicamentos de EUA obriga a fabricantes a informar que o paracetamol, cando se administra en doses moi altas ou xunto con bebidas alcohólicas, pode ser altamente tóxico e potencialmente mortal, en virtude dos danos que pode causar ao fígado.[2] En xuño de 1958 comercializouse unha formulación para nenos, Panadol Elixir. En 1963 o paracetamol engadiuse ao vademécum británico, e desde entón popularizouse como un analxésico con poucos efectos secundarios e con poucas interaccións con outros medicamentos.
A patente sobre o paracetamol expirou nos Estados Unidos, e varios xenéricos están amplamente dispoñibles baixo a Acta de Competitividade de Prezos e a Lei de Restauración de Patentes de 1984, aínda que certos preparados de Tylenol estiveron protexidos até o 2007. Nos EUA, a patente número 6.126.967 do 3 de setembro de 1998 foi concedida para a "liberación estendida de preparados de acetaminofén".
Dispoñibilidade comercial
editarNormalmente comercialízase como suspensión líquida, en comprimidos ou como supositorio.
O Panadol, que se vende en Europa, América Latina, Asia e Australia, é a marca máis estendida, vendida en máis de 80 países. En Norteamérica, o paracetamol véndese como xenérico ou baixo varias marcas: por exemplo Tylenol (McNeil - PPC, Inc), Anacin 3 e Datril.
Nalgunhas formulacións o paracetamol combínase co opioide codeína, ás veces chamado co-codamol, por exemplo o Algidol (Almirall) en España, o que o converte en máis tóxico[Cómpre referencia]. Nos Estados Unidos e no Canadá véndese como Tylenol 1/2/3/4; nos Estados Unidos só se pode adquirir con receita médica, o contrario que no Canadá. No Reino Unido e noutros moitos países, esta combinación véndese como Tylex CD e Panadeine. Outras marcas dispoñibles son: Captin, Disprol, Dymadon, Fensum, Hedex, Mexalen, Nofedol, Pediapirin, Atamel e Perfalgan. En España pode adquirirse indistintamente como xenérico ou como medicamento "de marca", como o moi coñecido Efferalgan de (Upsa Laboratoires), Termalgin (Novartis), Gelocatil ou Frenadol (composto con Dextrometorfano, ácido ascórbico e clorfenamina comercializado por McNeil).
Tamén se pode combinar con oxicodona, por exemplo o Percocet nos Estados Unidos.
Síntese
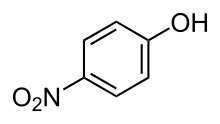
editarAs reacción do p-aminofenol con anhídrido acético, produce a acetilación do primeiro, obténdose como produtos o paracetamol e ácido acético.
Aínda que convén protexer o grupo hidroxilo fenólico debido ao seu maior poder nucleófilo, respecto ao nitróxeno anilínico.
Farmacodinamia
editarDurante moito tempo creuse que o mecanismo de acción do paracetamol é similar ao do ácido acetilsalicílico (AAS). É dicir, que actúa reducindo a síntese de prostaglandinas, compostos relacionados cos procesos febrís e a dor, inhibindo a cicloosixenase (COX).
Con todo, hai diferenzas importantes entre os efectos do ácido acetilsalicílico e o paracetamol. As prostaglandinas participan nos procesos inflamatorios, pero o paracetamol non presenta actividade antiinflamatoria apreciable. Ademais, a COX tamén participa na síntese de tromboxanos que favorecen a coagulación do sangue; o AAS ten efectos anticoagulantes, pero o paracetamol non. Finalmente, o AAS e outros AINEs son prexudiciais para a mucosa gástrica, onde as prostaglandinas desempeñan un papel protector, pero neste caso o paracetamol é seguro.
Desta forma, mentres o AAS actúa como un inhibidor irreversible da COX e bloquea o centro activo da encima directamente, o paracetamol bloquéaa indirectamente e este bloqueo é inútil en presenza de peróxidos.[3] Isto podería explicar por que o paracetamol é eficaz no sistema nervioso central e en células endoteliales, pero non en plaquetas e células do sistema inmunitario, as cales teñen niveis altos de peróxidos.
Swierkosz et al. (2002) atopou evidencias que indican que o paracetamol inhibe unha variante da encima COX que é diferente ás variantes COX-1 e COX-2, denominada agora COX-3.[4] O seu mecanismo de acción exacto non é ben comprendido aínda, pero futuras investigacións poden esclarecelo.
Farmacocinética
editarnegro - carbono
branco - hidróxeno
vermello - osíxeno
azul - nitróxeno
O paracetamol absórbese rápida e completamente por vía oral, e bastante ben por vía rectal, tendo a vantaxe de evitar o primeiro paso hepático. Existen tamén preparacións intravenosas. As concentracións plasmáticas máximas alcánzanse en función da forma farmacéutica, cun tempo, até a concentración máxima, de 0,5-2 horas. O paracetamol distribúese rapidamente por todos os tecidos. As concentracións son similares no sangue, a saliva e o plasma. A taxa de unión ás proteínas plasmáticas é baixa.
A biodispoñibilidade é moi elevada (próxima ao 100%), sendo a biodispoñibilidade por vía oral do 75-85%. O paracetamol metabolízase principalmente a nivel do fígado. As dúas principais rutas metabólicas son a glucuro e sulfuroconxugación. Esta última vía satúrase rapidamente con doses superiores ás terapéuticas. Soamente unha pequena proporción se metaboliza mediante o sistema encimático do citocromo P450 no fígado, por acción das oxidases mixtas, xerando un intermedio reactivo, N-acetilbenzoquinoneimida que en condicións normais é inactivado (se detoxifica) por reacción cos grupos sulfhidrilo do glutatión e eliminado nos ouriños conxugado con cisteína e ácido mercaptúrico. Pola contra, durante as intoxicacións graves aumenta a cantidade deste metabolito tóxico.
Doses elevadas de paracetamol, saturan as súas outras dúas vías metabólicas e créase un exceso de N-acetilbenzoquinoneimida que esgota os niveis hepáticos de glutatión. Entón o metabolito pode reaccionar covalentemente con aminoácidos das encimas e proteínas hepáticas, ás que inactiva e chega a provocar necrose hepática aguda. Os nenos teñen unha menor capacidade de glicuronidación, o que os fai máis susceptibles a sufrir este trastorno.
A eliminación é principalmente urinaria. O 90% da dose inxerida elimínaa o ril en 24 horas, principalmente como glicurónidos (60 a 80%) e sulfoconxugados (20 a 30%). Menos do 5% elimínase sen modificar. A semi-vida de eliminación do paracetamol é de 2-4 horas nos pacientes coa función hepática normal, sendo practicamente indetectable no plasma 8 horas despois da súa administración. Nos pacientes con disfunción hepática a semi-vida aumenta substancialmente, o que pode ocasionar o desenvolvemento dunha necrose hepática.[5]
Toxicidade
editar- Artigo principal: Toxicidade do paracetamol.
Consideracións xerais
editarO paracetamol ten un índice terapéutico moi axustado. Isto significa que a dose normal (un máximo ao día de 4 gramos en adultos) é próxima á sobredose[6]., facendo del un composto perigoso. Unha dose única de paracetamol de 10 g ou doses continuadas de 5 g/día nun non consumidor de alcol con boa saúde, ou 4 g/día nun consumidor habitual de alcol, poden causar danos importantes no fígado. Sen un tratamento adecuado no momento oportuno, a sobredose ou a dose case normal de paracetamol pode dar como resultado un fallo hepático (insuficiencia hepática) seguido da morte inevitable. Debido á ampla dispoñibilidade sen receita do paracetamol (acetaminofen) -como Especialidade Farmacéutica Publicitaria, EFP=OTC (OTC nos EEUU)-, este utilizouse en moitos intentos de suicidio. O antídoto específico da intoxicación por paracetamol - ou acetaminofen - é a Acetil-Cisteína por vía intravenosa. A FDA -axencia para medicamentos e alimentos dos EEUU - pediu a todos os laboratorios que deixasen de comercializar paracetamol - acetaminofen - en doses unitarias superiores a 650 mg; doses totais diarias de 3.000 mg (3gr) poden ser moi tóxicas ou mortais para algunhas persoas.[7]
O paracetamol non debe tomarse tras consumir alcol, debido a que o fígado, cando está metabolizando o alcol, non pode metabolizar simultaneamente o paracetamol, aumentando por tanto o risco de hepatotoxicidade. Usado responsablemente, o paracetamol é un dos tratamentos máis seguros dispoñibles para a analxesia. O composto carece de efectos sobre o sistema da cicloosixenase, por tanto non ten efectos negativos sobre o esófago, estómago, intestino delgado ou intestino groso, ao contrario que os AINEs. Ademais, os pacientes con enfermidadees do ril poden tomar paracetamol mentres que os AINEs poden provocar insuficiencia renal aguda a certos pacientes. Ademais, o paracetamol ten poucos problemas de interacción con outros medicamentos.
A potencia do analxésico é equivalente, cando non hai inflamación, á dos AINEs, sempre que a dose de paracetamol sexa a adecuada. Un gramo diario de paracetamol ten un efecto analxésico equivalente ao dos AINEs, por exemplo en osteoartritis (En España, artroses). Cando se administra simultaneamente con 50 mg do antidepresivo tricíclico amitriptilina dúas veces ao día, dita combinación é tan eficaz como a de paracetamol e codeína, pero non perde efectividade co tempo como ocorre coa administración crónica de narcóticos. A diferenza do ácido acetilsalicílico, o paracetamol non contribúe á síndrome de Reye en nenos con enfermidades víricas. Estes factores fixeron do paracetamol o analxésico preferido para pacientes hospitalizados en casos de dor suave a moderado, ademais de ser o analxésico máis utilizado en pacientes ambulatorios.
O paracetamol é extremadamente tóxico para os cans, gatos etc. e non debería serlles administrado baixo ningunha circunstancia.[8] Calquera caso sospeitoso debería ser tratado por un veterinario para proceder á desintoxicación.[9] O tratamento en gatos é moi similar ao dos humanos.
O acetaminofeno é o analxésico máis amplamente usado nos Estados Unidos (Tylenol), pero pode causar danos ao fígado en doses ordinarias ou lixeiramente superiores. Ese feito será unha noticia para moitos consumidores pero algo sabido para os especialistas en fígado, e recoñeceuse oficialmente en abril de 2009, pola Administración de Alimentos e Medicamentos (FDA, polas súas siglas en inglés). O comité consultivo da FDA declarou hai 32 anos: "Non se debe exceder a dosificación recomendada [acetaminophen-Tylenol] porque pode causar lesión hepática severa e mesmo a morte".[Cómpre referencia]
Mecanismo da toxicidade
editarComo se mencionou anteriormente, o paracetamol é metabolizado a compostos inactivos por combinación con sulfato e ácido glicurónico, sendo unha pequena parte metabolizada polo sistema do citocromo P450. Este oxida ao paracetamol para producir un intermedio moi reactivo, a imina N-acetil-p-benzoquinoneimina (NAPQI). En condicións normais, a NAPQI neutralízase por acción do glutatión.
En episodios de toxicidade por paracetamol, as vías metabólicas do sulfato e o glicurónido satúranse e maior cantidade paracetamol desvíase ao sistema do citocromo P450 onde se produce NAPQI. Consecuentemente, as subministracións hepatocelulares de glutatión esgótanse e en NAPQI pode reaccionar libremente coas membranas celulares, causando amplos danos e morte de moitos hepatocitos, dando como resultado necrose hepática aguda. En estudos en animais, debe consumirse o 70% do glutatión hepático antes de que se dea hepatotoxicidade.
Factores de risco
editarA dose tóxica de paracetamol é moi variable. En adultos, doses únicas por encima de 7,5 g ou 150 mg/kg teñen unha probabilidade razoable de causar hepatotoxicidade. En adultos, doses de máis de 25 gramos son potencialmente letais. Tamén pode darse hepatotoxicidade cando doses pequenas pero múltiples superan ditas cantidades en 24 horas, ou mediante inxesta crónica de pequenas doses. Con todo, a sobredose involuntaria de paracetamol en nenos raramente ten como resultado este tipo de toxicidade. Este feito podería atribuírse en parte ao sistema do citocromo P450, inmaturo aínda nos nenos. O consumo excesivo de alcol pode afectar a función renal e incrementar a toxicidade do paracetamol. Por esta razón, tras grandes inxestas de alcol recoméndanse outros analxésicos como o ibuprofeno ou o ácido acetilsalicílico.
Algunhas persoas son máis propensas á hepatotoxicidade, mesmo con doses baixas como 4 gramos/día, e as doses letais poden baixar até 6 g/día. O xaxún é un factor de risco, posiblemente debido á redución das reservas de glutatión do fígado. Está ben documentado que o uso en combinación con inductores do CYP2E1 como a isoniazida potencia a hepatotoxicidade, aínda que dita relación non está abondo clara.[10][11] O alcoholismo, que tamén dá como resultado a produción de CYP2E1, tamén aumenta o risco de hepatotoxicidade do paracetamol.[12] O uso en combinación con outros medicamentos que inducen a síntese de encimas CYP, como os antiepilépticos (carbamazepina, fenitoína, barbitúricos etc) tamén foron presentados como factores de risco.
Evolución
editarAs persoas que inxeriron unha sobredose de paracetamol, polo xeral non presentan síntomas durante as primeiras 24 horas. Aínda que inicialmente son síntomas comúns náuseas, vómitos e diaforese, estes remiten pasadas varias horas. Tras aliviarse estes síntomas, os pacientes experimentan unha melloría, podendo chegar a pensar que o peor pasou. Con todo, tras inxerir unha dose tóxica, tras estes síntomas produciríase un fallo hepático.
O dano dáse xeralmente nos hepatocitos a medida que van metabolizando o paracetamol. Con todo, tamén pode darse insuficiencia renal aguda. Isto tamén é causado xeralmente por un fallo hepatorenal ou por un fallo orgánico múltiple. A manifestación clínica principal da intoxicación tamén podería ser a insuficiencia renal aguda. Nestes casos, é posible que o metabolito tóxico sexa producido en máis cantidade nos riles que no fígado.
O prognóstico da sobredose por paracetamol varía dependendo da dose e o tratamento empregado. Nalgúns casos, a necrose hepática masiva dá como resultado un fallo hepático fulminante, con complicacións como hemorraxias, hipoglicemia, insuficiencia renal, encefalopatía hepática, edema cerebral, sepse, fallo orgánico múltiple e morte en poucos días. En moitos casos, a necrose hepática pode continuar, volver a función hepática normal e o paciente pode sobrevivir cunha función hepática normal nun prazo de poucas semanas.
Diagnóstico
editarOs síntomas claros de toxicidade hepática poden sobrevir nun prazo de 1 a 4 días, aínda que nalgúns casos estes poden ser evidentes en tan só 12 horas. Poden darse molestias no cuadrante dereito superior. Mediante análise pódese determinar a existencia de necrose hepática masiva se se detectan niveis elevados de AST, LT, bilirrubina e tempos de coagulación elevados (concretamente, tempos elevados de protrombina). A hepatotoxicidade do paracetamol pódese diagnosticar se despois dunha sobredose de paracetamol o AST e ALT superan os 1.000 UI/L. Con todo, os niveis de AST e ALT poden superar os 10.000 UI/L. En xeral, na hepatotoxicidade inducida por paracetamol, os niveis de AST son algo superiores aos de ALT.
Existen nomogramas de paracetamol que permiten estimar o risco de toxicidade baseándose na súa concentración en soro sanguíneo tras un determinado número de horas. Para determinar o risco potencial de hepatotoxicidade, o nivel de paracetamol debe ser seguido ao longo do nomograma estándar. Un nivel de paracetamol trazado durante as primeiras horas de inxestión podería subestimar a cantidade real no organismo, debido a que nese momento o paracetamol podería estar aínda absorbéndose no tracto gastrointestinal. Unha demora na determinación do nivel de paracetamol no organismo non é recomendable, debido a que nestes casos as estimacións poderían non ser adecuadas e un nivel tóxico en calquera momento é suficiente para administrar o antídoto.
Sobredosificación
editarMedidas de rescate
editar- Lavado gástrico
O tratamento para sobredose de paracetamol, sen complicacións, é similar ao usado noutros medicamentos, un lavado gastrointestinal. Adicionalmente, administrar N-acetilcisteína, xa sexa por vía intravenosa ou oral, axuda moito nestes casos. Hai suficiente marxe para que o médico xulgue neste caso se é necesario un lavado gastrointestinal completo ou basta con administrar carbón activado. A absorción total do paracetamol por parte do tracto gastrointestinal complétase en aproximadamente dúas horas. Nestes casos, o xarope de ipecacuana (un emético) non é efectivo, debido a que induce vómitos e isto o único que fai é atrasar a efectividade do carbón activado e a N-acetilcisteína, ao ter que administralos despois de que finalicen os vómitos. O lavado gástrico é efectivo durante a primeira hora posterior á inxestión. Posterior a iso, non ten utilidade clínica.
- Carbón activado
Normalmente, a administración de carbón activado é máis efectiva que o lavado gástrico. Este absorbe ben o paracetamol, e por tanto redúcese a cantidade que se absorbe no tracto gastrointestinal. Ademais, tamén expón menos risco de aspiración que o lavado gástrico. Hai tempo había certa renuencia a administrar carbón activado, debido ao temor a que tamén absorbese a N-acetilcisteína. Estudos recentes demostraron que a cantidade absorbida por esta vía non supera o 39% cando ambos se administran conxuntamente. Outros estudos mostraron que o carbón activado parece ser beneficioso para o paciente. Hai un consenso xeral en administrar carbón activado durante as primeiras 4 horas trala sobredose; tras este tempo, depende do criterio do médico, pero de todos os xeitos considérase un tratamento benigno. Se hai dúbidas sobre a inxestión de paracetamol xunto a outros medicamentos, entón debe administrarse carbón activado. Hai discrepancias en canto a cambiar a dose de N-acetilcisteína administrada, ou mesmo se esta debe modificarse.
A dose de carbón activado é de 2 g/kg de peso do paciente até un tope de 100 gramos totais. En nenos, a dose é de 1 g/kg . Adminístrase por vía oral e pode ser xunto a auga ou mollo para enmascarar en parte o mal sabor deste.
Acetilcisteína
editarA N-acetilcisteína (NAC) actúa proporcionando grupos sulfhidrilo para que reaccionen co metabolito tóxico e desta forma non ataquen aos hepatocitos. Se a NAC adminístrase no primeiras oito horas, redúcese notablemente a toxicidade. Se se administra pasadas 8 horas, a súa eficacia redúcese debido a que xa comezou a fervenza de reaccións tóxicas no fígado, e o risco de necrose hepática aumenta considerablemente. A NAC oral é un medicamento seguro, é fiable en casos de sobredoses por paracetamol durante o embarazo e non se dan reaccións adversas con prognóstico fatal. O fabricante recomenda non administrar o NAC se existe unha encefalopatía, debido a que existen razóns teóricas que argüen que dita encefalopatía podería empeorar. A principios de 2004, a Administración de Alimentos e Medicamentos (FDA, polas súas siglas en inglés) estadounidense autorizou o uso, para pacientes con sobredoses de máis de 10 horas, dun preparado de NAC para infusión intravenosa (dose total de 300 mg/kg) durante un período de 20 horas, que carece de efectos piroxénicos. Este preparado usouse con éxito durante anos noutros países, como Australia, Canadá e Gran Bretaña.
- Administración
Dito tratamento consiste nunha administración inicial de 150 mg/kg durante 15 minutos, seguido de 50 mg/kg durante as catro horas seguintes e finalmente 100 mg/kg durante as 16 horas restantes. A formulación oral tamén pode disolverse, filtrarse e esterilizarse por un farmacéutico do hospital para administración intravenosa. Esta é unha boa opción en casos onde a vía enteral non é viable ou está contraindicada. A administración intravenosa de NAC está relacionada con casos de reacciones alérxicas como choques anafilácticos e broncoespasmos.
Na práctica, se transcorreron máis de 8 horas trala inxestión, o carbón activado non é efectivo e debe administrarse a NAC inmediatamente. Se transcorreron menos de 8 horas, débese administrar carbón activado, empezar a administrar NAC e esperar a ver os niveis de paracetamol. En pacientes cunha sobredose de menos de 8 horas, o risco de hepatotoxicidade é reducido. Se se administran máis de dúas dose de carbón activado debido a que o paciente inxeriu dous ou máis medicamentos, as subseguintes administracións de carbón activado e NAC deben demorarse dúas horas. A NAC é eficaz se se administra con prontitude, pero pode ser efectivo aínda cando transcorresen 48 horas da sobredose.
En xeral, a NAC oral adminístrase enteralmente cunha primeira dose de 140 mg/kg seguidas de 17 dose máis, cada catro horas, de 40 mg/kg ou ata que se obteñan concentracións plasmáticas de paracetamol non tóxicas. A NAC pode ser difícil de administrar debido ao seu sabor e é frecuente que provoque vómitos e náuseas. Para maximizar a súa tolerancia, pode diluírse do 20% ao 5% a partir das doses comerciais. Os estudos iniciais de laboratorio deben incluír bilirrubina, AST, ALT e o tempo de protrombina. As análises deben repetirse, polo menos, diariamente. Unha vez que se determinou que se inxeriu unha dose potencialmente tóxica, deben administrarse as 17 doses de NAC, aínda que o paracetamol deveña indetectable en sangue. Se se desenvolve un fallo hepático, deben continuarse as 17 doses ata que se restableza a función hepática normal ou se efectúe un transplante de fígado.
Prognóstico
editarO risco de mortalidade por sobredose empeza a aumentar a partir dos dous días, alcanza un máximo ao cuarto e posteriormente diminúe gradualmente. Os pacientes cunha mala evolución deben ser trasladados inmediatamente a un centro capaz de efectuar transplantes de fígado. A acidose é o factor máis ominoso que delata o risco de mortalidade e a necesidade dun transplante.
En pacientes non trasplantados, estableceuse un factor de mortalidade do 95% cando o pH sanguíneo sitúase por baixo de 7,3. Outros indicadores dun mal prognóstico médico inclúen insuficiencia renal, grao 3 ou maior de encefalopatía hepática, un tempo de protrombina marcadamente elevado ou un aumento no mesmo do día 3 ao 4. Un estudo mostrou que unha análise do factor V menor que o 10% do normal indica un mal prognóstico (91% de mortalidade), mentres que unha relación menor a 30 entre o factor VIII e o V son indicadores dun bo prognóstico (100% de supervivencia).
Incidencia ambiental e degradación
editarUn dos fármacos máis amplamente atopado e en maiores concentracións é o paracetamol, produto que pode atoparse en efluentes hospitalarios, efluentes de plantas de tratamento, ríos e lodos.
Lamentablemente os medicamentos son deseñados para que posúan determinadas características, por exemplo, aproximadamente o 30 % dos medicamentos son lipófilos, que significa que se disolven en graxa pero non en auga. Esta característica permítelle a estes compostos pasar a través das membranas da célula e actuar dentro das mesmas. Doutra banda, os medicamentos deséñanse para que sexan persistentes, polo que manteñen a súa estrutura química un tempo suficientemente grande como para exercer a súa acción terapéutica, así que unha vez que entran ao medio ambiente persisten no mesmo.
O paracetamol en solución acuosa é susceptible de sufrir unha hidrólise para formar o p-amino fenol, o mesmo é susceptible de degradarse en quinoneimina. A velocidade de degradación do paracetamol crece co aumento da temperatura e da luz. Esta velocidade é mínima a un pH próximo a 6. Para estabilizar o paracetamol en solución, adóitase engadir un tampón e un axente antioxidante ou captador de radicais. Na eliminación do acetaminofeno observouse que reacciona con cloro para formar un gran número de subprodutos, dous dos cales foron identificados como tóxicos. [13]
Notas
editar- ↑ Brodie BB & Axelrod J (1948). J. Pharmacol. Exp. Ther. 94: 29-38.
- ↑ "Briefing Materials For Drug Safety And Risk Management Anesthetic And Life Support And Nonprescription Drugs Advisory Commitee Meeting" (PDF). Arquivado dende o orixinal (PDF) o 30 de decembro de 2011. Consultado o 05 de novembro de 2012.
- ↑ Boutaud Ou, Aronoff DM, Richardson JH, Marnett LJ, Oates JA (2002). "Determinants of the cellular specificity of acetaminophen as an inhibitor of prostaglandin H2 synthases". Proc Natl Acad Sci U S A 99 (10): 7130-5. PMID Dispoñible en liña.
- ↑ Swierkosz TA, Jordan L, McBride M, McGough K, Devlin J, Botting RM (2002). "Actions of paracetamol on cyclooxygenases in tissue and cell homogenates of mouse and rabbit". Med Sci Monit 8 (12): BR496-503. PMID PDF.
- ↑ Benson GD. Acetaminophen in chronic liver disease. Clin Pharmacol Ther 1983;33:95?101
- ↑ Antonio J. Arnal Meinhardt. El Acetamonofén o Paracetamol es un fármaco para toda la familia Arquivado 14 de agosto de 2012 en Wayback Machine. Rev TuDoctorOnline. Consultado 18 de setembro de 2012.
- ↑ Da Oliva, S.; Cánovas, A.; Mencías, E. (2001). "Revisión das intoxicacións por paracetamol consultadas ao Servizo de Información Toxicolóxica. Comunicación presentada no XIV Congreso Español de Toxicoloxía. Murcia, 26-28 de setembro de 2001". Revista de Toxicoloxía. ISSN: 1697-0748, 18 (3): 183. Dispoñible en liña Arquivado 14 de xullo de 2010 en Wayback Machine..
- ↑ Allen AL (2003). "The diagnose of acetaminophen toxicosis in a cat". Can Vet J 44 (6): 509-10. PMID Dispoñible en liña
- ↑ Villar D, Buck WB, Gonzalez JM (1998). "Ibuprofen, aspirin and acetaminophen toxicosis and treatment in dogs and cats". Vet Hum Toxicol 40 (3): 156-62. PMID
- ↑ Crippin JS (1993). "Acetaminophen hepatotoxicity: potentiation by isoniazid". Am J Gastroenterol 88 (4): 590-2. PMID
- ↑ Nolan CM, Sandblom RE, Thummel KE, Slattery JT, Nelson SD (1994). "Hepatotoxicity associated with acetaminophen usage in patients receiving multiple drug therapy for tuberculose". Chest 105 (2): 408-11. PMID
- ↑ Zimmerman HJ, Maddrey WC (1995). "Acetaminophen (paracetamol) hepatotoxicity with regular intake of alcol: analysis of instances of therapeutic misadventure". Hepatology 22 (3): 767-73. PMID
- ↑ "Formulación líquida de paracetamol inyectable - Una solución acuosa de paracetamol para uso por perfusión con un pH entre 4,5 y 6,0, caracterizada". Patentados.com. 27-10-2007. Consultado o 19-03-2011.
Véxase tamén
editar| Commons ten máis contidos multimedia sobre: Paracetamol |
Outros artigos
editarLigazóns externas
editar- Información sobre Paracetamol (en castelán)
- Páxina oficial de Tylenol (en castelán)
- Hepatotoxicidade por paracetamol Arquivado 15 de febreiro de 2009 en Wayback Machine. (en castelán)
- Centro de Información do Paracetamol (en inglés)
- Historia do paracetamol (en inglés)
- The Julius Axelrod Papers (en inglés)
- Mecanismo de acción do paracetamol (en castelán)
