Malaria
A malaria (do italiano medieval "mal aire") ou paludismo (de paludis, xenitivo do termo latino palus: pantano, e -ismo, neste caso acción ou proceso patolóxico) é unha doenza parasitaria aguda ou crónica causada por protozoos parasitos do xénero Plasmodium, transmitidos pola picada da femia do mosquito Anopheles[1]. Algúns estudos científicos suxiren que puido terse transmitido ao ser humano a través do Gorilla gorilla[2]. Entre 700 000 e 2 700 000 persoas morren cada ano por mor da malaria, dos cales máis do 75% son nenos que viven en zonas endémicas de África[3][4]. Así mesmo, causa aproximadamente entre 400 e 900 millóns de casos de febre aguda ao ano na poboación infantil (menores de cinco anos) en ditas zonas[3]. Segundo datos de 2005, estímase que hai entre 350 e 500 millóns de episodios de paludismo clínico cada ano[5].
| Malaria | |
|---|---|
| Clasificación e recursos externos | |
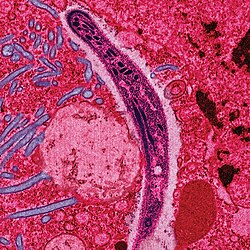 Plasmodium da saliva dun mosquito femia. | |
| ICD-10 | B50-B54 |
| ICD-9 | 084 |
| OMIM | 248310 |
| DiseasesDB | 7728 |
| MedlinePlus | 000621 |
| eMedicine | emerg/305 ped/1357 |
Se cre que pode requirir tratamento, por favor, consúltello ao médico. | |
O primeiro intento dunha vacina sintética contra a malaria foi realizado en 1997 polo equipo de Manuel Elkin Patarroyo. Os resultados foron desiguais, alcanzando en Suramérica unha eficacia máxima do 28%[6]. A día de hoxe, a Organización Mundial da Saúde ten catalogada a esta vacina como «inactiva»[7]. Prometedores resultados anunciáronse en agosto de 2013, cando os xornais fixéronse eco de que unha vacina na fase I de estudo, alcanzaba unha eficacia dun 100%[8].
En maio de 2007, a Organización Mundial da Saúde decidiu conmemorar o Día Mundial da Malaria o 25 de abril de cada ano[9].
Plasmodium
editar- Artigos principais: Plasmodium e Plasmodium falciparum.
O Plasmodium é un protozoo, ou sexa un ser unicelular, eucariota como as células humanas. Existen catro especies que poden producir a infección:
- Plasmodium falciparum: causa a forma de malaria máis grave, a malaria maligna (terzá). Ten o ciclo de vida máis rápido. Ataca tanto as hemacias novas como as maduras. É responsábel do 80% dos casos clinicamente significativos e do 90% das mortes.
- Plasmodium vivax: ataca só eritrocitos inmaturos, especialmente reticulocitos. Causa doenza crónica, a malaria benigna terzá. Pode ficar dormente durante moitos anos e reaparecer despois, debido á reactivación dunha das súas formas parasitas, os hipnozoítos.
- Plasmodium malariae: ataca só os glóbulos vermellos máis maduros. Causa malaria benigna crónica.
- Plasmodium ovale: é común en África e, raramente, no Pacífico Occidental e América do Sur. Ataca só os eritrocitos novos, causando doenza crónica, a malaria benigna terzá ovale. Pode ficar dormente durante moitos anos e despois reaparecer.
O ciclo de vida do plasmodio é complexo. Os esporozoítos son unhas formas que existen nas glándulas salivares do mosquito anófele, sendo inxectados no sangue da vítima humana. De aí, os esporozoítos invaden o fígado, onde, na forma xigante multinucleada de esquizontes, reprodúcense asexualmente, xerando merozoítos - as formas invasoras dos glóbulos vermellos (hemacias ou eritrocitos). Invaden estas células por receptores diferentes para cada especie, de onde se explica a súa preferencia por subpoboacións de eritrocitos. Dentro do eritrocito, o plasmodio non se detecta polo sistema inmunitario, cesando as manifestacións clínicas. No eritrocito, o plasmodio divídese asexuadamente ata que, debido ao número excesivo de merozoítos, o eritrocito rebenta. Nese momento volve haber febre e outros síntomas, porque os merozoítos e as substancias químicas por eles producidas dentro do eritrocito son dispersadas na corrente sanguínea e identificadas polos leucocitos. Estes producen citocinas (especie de hormonas) cando identifican os invasores. Febre violenta, tremores, malestar, dores, son algúns dos efectos da estimulación no cerebro pola citocina IL-1 (a temperatura alta é producida polos tremores musculares e causa malestar, mais inhibe a multiplicación de microorganismos, que prefiren 37 °C). Eses merozoítos invaden entón novas hemacias, multiplicándose cada vez máis en cada ciclo. Algúns transfórmanse en gametontes que se zugan, xuntamente co sangue, por outros mosquitos. Os gametos masculino e feminino fúndense no corpo do mosquito, dando orixe a un cigoto, que se multiplica en novos esporozoítos, que migran para as glándulas salivares do insecto hóspede. Esta fase de reprodución sexual permite unha maior variabilidade xenética, o que explica que un individuo afectado non desenvolve sempre resistencia eficaz a outras estirpes.
O parasito produce e secreta proteínas que se fixan na membrana celular do eritrocito infectado e que se ligan a outras proteínas producidas polo endotelio dos vasos sanguíneos. Así o eritrocito hóspede adhírese á parede do vaso, evitando o paso polo bazo, un centro importante da filtración inmunolóxica do sangue no que son destruídos moitos eritrocitos infectados. A propensión dos eritrocitos infectados a se concentraren nos vans pode levar á oclusión dos pequenos vasos, con hemorraxias e infartos, especialmente na malaria causada por P. falciparum. Estas proteínas non son útiles para a formación de anticorpos específicos, porque o parasito posúe xenes para máis de 50 variedades coa mesma función, cando os anticorpos contra esas proteínas comezan a ser producidos xa a maior parte dos parasitos está a usar outra variedade.
Transmisión
editarA malaria é transmitida pola picada das femias de mosquitos do xénero Anopheles. A transmisión xeralmente ocorre en rexións rurais e semirurais, mais pode ocorrer en áreas urbanas, principalmente nas súas periferias. En cidades situadas en lugares cuxa altitude sexa superior a 1.500 metros, no entanto, o risco de adquisición de malaria é pequeno. Os mosquitos teñen maior actividade durante o período nocturno, do solpor ao amencer. Contamínanse ao picar aos portadores da doenza, tornándose o principal vector de transmisión desta para outras persoas. O risco maior de adquisición de malaria é no interior das habitacións, aínda que a transmisión tamén poida ocorrer ao ar libre.
O mosquito da malaria só sobrevive a temperaturas mínimas maiores que 15 °C, e só atinxe número suficiente de individuos para a transmisión da doenza en rexións con temperaturas mínimas de preto de 20-30 °C e humidade alta. Soamente pican ao ser humano os mosquitos femias, que se alimentan de sangue, mentres que os machos viven dos zumes de plantas. As larvas desenvólvense en augas paradas, principalmente durante as estacións de choivas abundantes.
Progresión e síntomas
editarA malaria causada por P.falciparum caracterízase no inicio por síntomas inespecíficos, como dores de cabeza, fatiga, febre e náuseas. Estes síntomas poden durar varios días (seis para P.falciparum, varias semanas para as outras especies).
Máis tarde aparecen accesos periódicos de calafríos e febre intensos que coinciden coa destrución masiva de hemacias e coa descarga de substancias inmunoxénicas tóxicas na corrente sanguínea ao fin de cada ciclo reprodutivo do parasito. Estas crises paroxísticas, máis frecuentes ao caer da tarde, inícianse con subida da temperatura ata 39-40 °C. Son seguidas de palidez da pel e tremores violentos durante preto de 15 minutos a unha hora. Despois cesan os tremores e seguen dúas a seis horas de febre con 41 °C, terminando con pel avermellada e suores abundantes. O doente séntese perfectamente ben despois e ata a crise seguinte, dous a tres días despois. Se a infección for de P. falciparum, a denominada malaria maligna, pode haber síntomas adicionais máis graves como choque circulatorio, síncopes (desmaios), convulsións, delirios e crises vaso-oclusivas. A morte pode ocorrer en cada crise de malaria maligna. Pode tamén ocorrer a chamada malaria cerebral: a oclusión de vasos sanguíneos no cerebro polos eritrocitos infectados causa déficit mentais e coma seguidos de morte (ou déficit mental irreversíbel). Polas mesmas razóns tamén ocorren danos renais e hepáticos graves. As formas causadas polas outras especies ("benignas") en xeral son soamente debilitantes, raramente ocorrendo a morte.
Os intervalos entre as crises paroxísticas son diferentes segundo a especie. Para as especies de P. falciparum, P. ovale e P. vivax, o ciclo da invasión de hemacias por unha xeración, multiplicación interna na célula, lise (rebentamento da hemacia) e invasión pola nova xeración de máis hemacias dura 48 horas. Normalmente hai accesos de febre violenta e tremores no día 1, e pasados 48 horas xa no día 3 etc, clasificándose como malaria ternaria. A infección polo P. malariae ten ciclos de 72 horas, dándose no día 1, despois no día 4 etc., constituíndo a malaria cuaternaria. A detección precoz de malaria cuaternaria é importante porque este tipo non pode ser debido a P. falciparum, sendo polo tanto menos perigoso.
Os síntomas crónicos inclúen a anemia, cansazo, debilitación con redución da capacidade de traballo e da intelixencia funcional, hemorraxias e infartos de incidencia moi aumentada, como infarto do miocardio e AVCs (especialmente con P. falciparum).
Se non se diagnostica e trata, a malaria maligna causada polo P. falciparum pode evolucionar axiña, resultando en morte. A malaria "benigna" das outras especies resulta en debilitación crónica e máis raramente en morte.
É unha das doenzas máis importantes para a humanidade, debido ao seu impacto e custos, e constitúe un fardo extremadamente pesado para as poboacións dos países afectados, principalmente en África, incomparábel aos custos sociais de calquera doenza occidental. A malaria existe potencialmente en todas as rexións onde existen homes e mosquitos anófele en cantidade suficiente, o que inclúe todas as rexións tropicais de todos os continentes e moitas rexións subtropicais. Hoxe en día, África é particularmente afectada, quedando indemnes só o Norte e mais Suráfrica. Na América existe en toda a rexión central (México e os países do istmo), no Caribe e mais no norte da América do Sur. Na Asia está presente en todo o subcontinente indio, Medio Oriente, Irán, Asia central, Sueste asiático, Indonesia, Filipinas e sur da China. A malaria erradicouse no século XX da rexión mediterránea, incluíndo o sur de Europa: Portugal, España, Italia, sur da Francia e Grecia; e no Sur e Oeste dos EUA. Así e todo, hai case 3 mil millóns de persoas (ou sexa, metade da humanidade) en rexións endémicas, en máis de 100 países.
Hai, todos os anos, 300 a 500 millóns de casos da malaria, dos cales máis do 90% en África, a maioría con resolución satisfactoria, mais resultando en enfraquecemento e perda de días de traballo significativos. Causa a morte, con todo, de preto de 2 millóns de persoas ao ano, cerca dun millón das cales son nenos con menos de 5 anos [Cómpre referencia].
En Europa, os casos son moito menos graves, habendo apenas algúns millares. A gran maioría dos casos impórtanse de persoas que visitan países tropicais.
Prevención
editarA mellor medida é a erradicación do mosquito anófele. Ultimamente, o uso de insecticidas potentes mais tóxicos, prohibidos no occidente, aumentou porque os riscos da malaria son moi superiores aos do insecticida. O uso de redes contra mosquitos é eficaz na protección durante o sono, cando ocorre a gran maioría das infestacións. As cremas repelentes de insectos tamén son eficaces, pero máis caros que as redes. A roupa debe cubrir a pel núa o máis completamente posíbel de día. O mosquito non ten tanta tendencia para picar a cara ou as mans, onde os vasos sanguíneos son menos accesíbeis, canto as pernas, os brazos ou o pescozo.
A drenaxe de pantanos e outras augas paradas é unha medida de saúde pública eficaz.
Diagnóstico
editarDebido á natureza non específica da manifestación dos síntomas, o diagnóstico da malaria en áreas non endémicas require un alto grao de sospeita, que podería estar provocada por algún dos seguintes feitos: historial recente de viaxes, bazo agrandado, febre, baixo número de plaquetas no sangue, e niveis de bilirrubina no sangue máis altos dos normais combinados cun nivel normal de leucocitos[10]. Informes de 2016 e 2017 suxiren altos niveis de sobrediagnóstico debido a insuficientes ou inadecuados tests de laboratorio[11][12][13].
A malaria confírmase normalmente co exame microscópico dun frotis de sangue ou por tests de diagnóstico rápido (RDT nas súas siglas en inglés) baseados en antíxenos[14][15]. Nalgunhas zonas, os RDT necesítanse para poder distinguir se os síntomas da malaria son causados por Plasmodium falciparum ou por outras especies de parasitos e, en consecuencia, as estratexias de tratamento poden diferir a infeccións non-P. falciparum[16]. A observación polo microscopio dos frotis de sangue é o método máis comunmente usado para detectar o parasito da malaria. En 2010 examináronse arredor de 165 millóns de frotis de sangue para malaria[17]. A pesar de estar moi estendido, o diagnóstico por microscopio ten dous importantes inconvenientes: moitos postos sanitarios, especialmente no rural, non están equipados para realizar o test, e a precisión dos resultados depende tanto da habilidade da persoa que examina o frotis de sangue como dos niveis do parasito no sangue. A sensibilidade do frotis de sangue varía desde un 75-90% en condicións óptimas, ata un baixo 50%. Os RDT dispoñibles comercialmente son frecuentemente máis precisos que o frotis de sangue para predicir a presenza dos parasitos da malaria, pero dependendo do fabricante son moi variables no diagnóstico da sensibilidade e especifidade, e son incapaces de dicir cantos parasitos hai[17].
Nas rexións onde as probas de laboratorio están facilmente dispoñibles, debería sospeitarse de ter malaria e facerlle o test a calquera persoa que non se encontre ben e que estivera nunha área onde a malaria é endémica. En áreas que non poden permitirse probas de diagnóstico de laboratorio, chegou a facerse común o uso só do historial de febre como indicador para o tratamento da malaria, de aí o dito común de "febre igual a malaria a non ser que se comprobe o contrario". Un inconveniente desta práctica é o sobrediagnóstico da malaria e a mala xestión da febre non malaria, que gasta recursos limitados, erosiona a confianza no sistema sanitario, e contribúe á resistencia aos medicamentos[18]. Aínda que se desenvolveron tests baseados na reacción en cadea da polimerase, no ano 2012 non eran moi usados en zonas onde a malaria é común, debido á súa complexidade[10].
Tratamento
editarA malaria maligna, causada polo P.falciparum é unha urxencia médica. As outras malarias son doenzas crónicas.
O tratamento farmacolóxico da malaria baséase na susceptibilidade do parasito aos radicais libres e substancias oxidantes, morrendo en concentracións destes axentes inferiores ás mortais para as células humanas. Os fármacos usados aumentan esas concentracións.
A quinina (ou o seu isómero quinidina), un medicamento antigamente extraído da casca da Cinchona, aínda se usa no seu tratamento. Porén, a maioría dos parasitos xa é resistente ós seus efectos. Foi suplantada por drogas sintéticas máis eficientes, como quinacrina, cloroquina, e primaquina. É frecuente o uso de cocktails (mesturas) de varios destes fármacos, pois hai parasitos resistentes a calquera deles por si só. A resistencia torna a cura difícil e cara.
Ultimamente a artemisinina, extraída dunha planta chinesa, ten dado resultados prometedores. Produce radicais libres en contacto con ferro, que existe especialmente na hemoglobina no interior das hemacias, onde se reproduce o parasito. É extremadamente eficaz en destruílo, causando efectos adversos mínimos. Porén, as cantidades producidas hoxe son insuficientes. No futuro, o cultivo da planta artemisina en África poderá reducir substancialmente os custos. É o único fármaco antimalárico para o cal aínda non existen casos descritos de resistencia.
Algunhas vacinas están en desenvolvemento.
Efectos xenéticos nas poboacións afectadas
editarA anemia falciforme é unha doenza xenética recesiva (os dous alelos do xene en causa teñen de estar mutados) que ocorre nas mesma rexións de alta incidencia de malaria. Así e todo, os portadores da deficiencia (con só un alelo mutado e o outro normal), teñen altas taxas de supervivencia á malaria, sendo en parte resistentes a ela.
Outros portadores de doenzas xenéticas, como algunhas talasemias, ou deficiencias no xene da encima glicosa-6-fosfato dehidroxenasa, existentes no Mediterráneo tamén poderán ser o produto de selección natural positiva dos portadores debido á maior resistencia ao parasito. Algunhas desas mutacións aumentan os radicais libres nas hemacias, aos cales é susceptíbel o parasito.
Historia
editarOs seres humanos teñen sufrido malaria desde hai 50.000 anos [Cómpre referencia]. O baixo número anterior de casos en humanos, en comparación cos elevados índices noutros animais, implicaba que os mosquitos que se alimentan dos outros animais fosen moito máis frecuentes que o anófele, que ten predilección polos humanos. Só o inicio da agricultura, hai 10.000 anos (nalgunhas rexións, noutras só hai 5.000 anos) e co crecemento da poboación e destrución dos ambientes naturais deses outros animais e os seus mosquitos, permitiu que as poboacións de anófele se expandisen en número, iniciándose a verdadeira epidemia de malaria que existe hoxe.
A malaria foi unha das doenzas que máis atinxiron o Imperio romano e a súa base de poboación e económica, contribuíndo á súa caída [Cómpre referencia].
Admítese que a malaria foi unha das principais razóns da lenta penetración dos europeos no interior da África cando a época colonial.
Na América do Sur, os nativos (indios) dos Andes e outros tiñan usado desde tempos inmemoriais a casca da árbore da Cinchona para tratar a malaria, así como os chineses xa usaban a planta Artemisa (unha "nova" droga antimalárica revolucionaria "descuberta" só recentemente). En 1640 o español Juan del Vego usou a tintura da casca da cinchona para tratar con éxito a malaria. En 1820 os franceses Pierre Pelletier e Joseph Caventou extraeron con éxito a quinina, o principio activo antimalárico, da tintura.
O italiano Giovanni María Lancisi foi quen, en 1717, notando que eran os habitantes dos pantanos os que máis sufriron da doenza, renomeou o paludismo como malaria, significando "malos ares".
Co desenvolvemento da quinina (hoxe a resistencia do parasito é case universal debido ao mal uso), o primeiro fármaco antimalárico, os europeos puideron sobrevivir en gran número no interior africano, dando finalmente orixe, no fin do século XIX, á carreira polas colonias africanas e partición do continente entre Portugal, Reino Unido, Francia, Alemaña, Bélxica, Italia e España.
O causante da malaria, o Plasmodium, foi descuberto polo médico do Exército francés, Charles Louis Alphonse Laveran, traballando na Alxeria, que recibiu o Premio Nobel da Fisioloxía e Medicina polo seu traballo, en 1907.
A existencia de malaria e outras doenzas debilitantes como a Enfermidade do sono é, segundo moitos especialistas, a razón da falta de desenvolvemento de moitas civilizacións (houbo aínda así algunhas) preeminentes na África ao sur do Sáhara. África, como berce da humanidade, é tamén o berce de moitos parasitos e doenzas infecciosas humanas, moitas das cales non existen en ningún outro lado. O custo económico e social da malaria e outras doenzas africanas é inimaxinábel para un occidental ou mesmo un americano ou asiático da rexión tropical. Espérase que co desenvolvemento futuro de medicamentos e terapias eficaces contra a malaria así como outras doenzas, incluíndo a SIDA, o progreso económico e social dos africanos se acelere.
Notas
editar- ↑ Organización Mundial da Saúde (WHO) (ed.). "Paludismo. Datos y cifras" (en castelán). Arquivado dende o orixinal o 3 de setembro de 2014. Consultado o 5 de novembro de 2018.
- ↑ El País, ed. (22 de setembro de 2010). "La malaria viene de los gorilas" (en castelán). Consultado o 5 de novembro de 2018.
- ↑ 3,0 3,1 Breman, Joel G. (2001). American Society of Tropical Medicine and Hygiene, ed. "The ears of the hippopotamus: manifestations, determinants, and estimates of the malaria burden". The American Journal of Tropical Medicine and Hygiene (en inglés) 64 (1-2 Suppl.): 1–11. PMID 11425172. Arquivado dende o orixinal o 22 de novembro de 2007. Consultado o 5 de novembro de 2018.
- ↑ Aregawi, Maru (2008). Organización Mundial da Saúde (WHO), ed. World Malaria Report 2008 (en inglés). p. vii. ISBN 978-92-4-156369-7.
- ↑ Pan American Health Organization, ed. (2005). "Informe mundial sobre el paludismo 2005" (en castelán).
- ↑ Graves, P. M.; Gelband, H. (2009). "Vaccines for preventing malaria (SPf66) (Review)" (PDF). The Cochrane Library (en inglés) (John Wiley & Sons Ltd.) (2): 1–38. Arquivado dende o orixinal (PDF) o 20 de xullo de 2011. Consultado o 05 de novembro de 2018.
- ↑ Organización Mundial da Saúde, ed. (17 de xullo de 2017). "Tables of Malaria Vaccine Projects Globally" (en inglés). Consultado o 5 de novembro de 2018.
- ↑ Valerio, María (8 de agosto de 2013). El Mundo, ed. "Una nueva y prometedora vacuna contra la malaria" (en castelán). Consultado o 5 de novembro de 2018.
- ↑ Organización Mundial da Saúde (ed.). "Día Mundial del Paludismo 25 de abril de 2018" (en castelán).
- ↑ 10,0 10,1 Nadjm, B.; Behrens, R.H. (2012). "Malaria: An update for physicians". Infectious Disease Clinics of North America (en inglés) 26 (2): 243–259. PMID 22632637. doi:10.1016/j.idc.2012.03.010.
- ↑ Manguin, Sylvie; Foumane, Vincent; Besnard, Patrick; Fortes, Filomeno; Carnevale, Pierre (xullo de 2017). "Malaria overdiagnosis and subsequent overconsumption of antimalarial drugs in Angola: Consequences and effects on human health". Acta Tropica (en inglés) 171: 58–63. PMID 28356231. doi:10.1016/j.actatropica.2017.03.022.
- ↑ Orish, Verner N.; Ansong, Joseph Y.; Onyeabor, Onyekachi S.; Sanyaolu, Adekunle O.; Oyibo, Wellington A.; Iriemenam, Nnaemeka C. (outubro de 2016). "Overdiagnosis and overtreatment of malaria in children in a secondary healthcare centre in Sekondi-Takoradi, Ghana". Tropical Doctor (en inglés) 46 (4): 191–198. PMID 26738767. doi:10.1177/0049475515622861.
- ↑ Yegorov, Sergey; Galiwango, Ronald M.; Ssemaganda, Aloysious; Muwanga, Moses; Wesonga, Irene; Miiro, George; Drajole, David A.; Kain, Kevin C.; Kiwanuka, Noah (14 de novembro de 2016). "Low prevalence of laboratory-confirmed malaria in clinically diagnosed adult women from the Wakiso district of Uganda". Malaria Journal 15 (1): 555. PMC 5109652. PMID 27842555. doi:10.1186/s12936-016-1604-z.
- ↑ Abba, K.; Deeks, J.J.; Olliaro, P.; Naing, C.M.; Jackson, S.M.; Takwoingi, Y.; Donegan, S.; Garner, P. (2011). Abba, Katharine, ed. "Rapid diagnostic tests for diagnosing uncomplicated P. falciparum malaria in endemic countries". Cochrane Database of Systematic Reviews (en inglés) (7): CD008122. PMID 21735422. doi:10.1002/14651858.CD008122.pub2.
- ↑ Kattenberg, J.H.; Ochodo, E.A.; Boer, K.R.; Schallig, H.D.; Mens, P.F.; Leeflang, M.M. (2011). "Systematic review and meta-analysis: Rapid diagnostic tests versus placental histology, microscopy and PCR for malaria in pregnant women". Malaria Journal (en inglés) 10: 321. PMC 3228868. PMID 22035448. doi:10.1186/1475-2875-10-321.
- ↑ Abba, Katharine; Kirkham, Amanda J.; Olliaro, Piero L.; Deeks, Jonathan J.; Donegan, Sarah; Garner, Paul; Takwoingi, Yemisi (18 de decembro de 2014). "Rapid diagnostic tests for diagnosing uncomplicated non-falciparum or Plasmodium vivax malaria in endemic countries". Cochrane Database of Systematic Reviews (en inglés) (John Wiley & Sons) 12: CD011431. PMC 4453861. PMID 25519857. doi:10.1002/14651858.cd011431. Arquivado dende o orixinal o 26 de xaneiro de 2017. Consultado o 6 de novembro de 2018.
- ↑ 17,0 17,1 Wilson, M.L. (2012). "Malaria rapid diagnostic tests". Clinical Infectious Diseases (en inglés) 54 (11): 1637–1641. PMID 22550113. doi:10.1093/cid/cis228.
- ↑ Perkins, M.D.; Bell, D.R. (2008). "Working without a blindfold: The critical role of diagnostics in malaria control". Malaria Journal (en inglés) 1 (Suppl 1): S5. PMC 2604880. PMID 19091039. doi:10.1186/1475-2875-7-S1-S5.
Véxase tamén
editar| Wikimedia Commons ten máis contidos multimedia na categoría: Malaria |
Outros artigos
editarLigazóns externas
editar- "La malaria en diez datos" (El Mundo.es, 25.04.2011) (en castelán)
- ¿Qué es la malaria" (Infografía El Mundo.es, 16.11.2005) (en castelán)
- MALÁRIA - Aspectos clínicos e epidemiolóxicos (en portugués)
- Programa Nacional de Prevención e Control da Malaria (PNCM). Ministerio da Saúde – Brasil (en portugués)
