Plasmodium
- Non confundir coas células ameboides multinucleadas como as dos mofos mucosos, chamadas plasmodios.
| Plasmodium | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
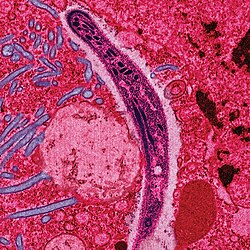 esporozoíto de Plasmodium | |||||||||||||||
| Clasificación científica | |||||||||||||||
| |||||||||||||||
| Especies | |||||||||||||||
Plasmodium é un extenso xénero de protozoos parasitos apicomplexos. A infección en humanos por estes protozoos denomínase malaria, unha doenza moi estendida nos trópicos. Os parasitos teñen dous hóspedes no seu ciclo vital: un mosquito, que é o vector, e un vertebrado. Distintas especies de Plasmodium infectan o ser humano, outros mamíferos, aves e réptiles. As formas máis comúns de malaria humana están causadas por catro especies: Plasmodium falciparum (a máis perigosa), P. vivax, P. ovale, e P. malariae.
O xénero Plasmodium foi descrito inicialmente en 1885. Actualmente contén unhas 200 especies divididas en varios subxéneros, e especies que antes estaban incluídas noutros xéneros foron agora engadidas a Plasmodium. O parasito crese que se orixinou a partir de dinoflaxelados fotosintéticos.
O ciclo vital destes organismos é moi complexo, e comprende unha secuencia de diferentes estadios tanto no vector coma no hóspede. Alterna entre un mosquito, no que se instala no intestino e nas glándulas salivares, e un vertebrado, no que infecta as células sanguíneas e do fígado. O mosquito inxecta o protozoo coas súas secrecións salivares e recólleo ao zugar sangue do vertebrado. O protozoo durante o seu ciclo de vida no vertebrado presenta distintas morfoloxías, que reciben o nome de esporozoítos, hipnozoítos latentes, merosomas e merozoítos, trofozoítos, esquizontes, gametocitos masculinos e femininos, que son captados por outros mosquitos ao zugar sangue. No intestino do mosquito os gametocitos desenvólvense orixinando gametos, que se fecundan formando cigotos móbiles, que se escapan do intestino, e crecen formando novos esporozoítos que se instalan nas glándulas salivares do mosquito, desde onde o mosquito os inxectará no hóspede vertebrado, iniciándose un novo ciclo.
Taxonomía e hóspedes
editarO xénero Plasmodium foi creado en 1885 por Marchiafava e Celli e comprende unhas 200 especies recoñecidas. Seguen a describirse novas especies.[1]
En 2006 o xénero precisaba unha reorganización, xa que parece que parasitos situados nos xéneros Haemocystis e Hepatocystis están moi relacionados con Plasmodium. Probablemente outras especies como Haemoproteus meleagridis poderían incluírse neste xénero cando se revise.
A gama de hóspedes utilizada por estes protozoos entre as ordes de mamíferos non é uniforme. Polo menos 29 especies infectan a primates non humanos; os roedores de fóra das zonas tropicais de África rara vez son afectados; unhas poucas especies infectan a morcegos, ourizos cacheiros e esquíos; pero non se coñecen carnívoros, insectívoros ou marsupiais que actúen como hóspedes. Tamén afectan a aves e réptiles.
En 1898 Ronald Ross demostrou a existencia de Plasmodium na parede do intestino e nas glándulas salivares do mosquito Culex (aínda que non é o transmisor normal en humanos). Por este descubrimento gañou o Premio Nobel en 1902. Porén, tamén foron moi importantes os traballos do profesor italiano Giovanni Battista Grassi, que demostrou que a malaria humana só podía transmitirse polos mosquitos do xénero Anopheles. Nalgunhas especies o vector pode non ser un mosquito.
Poden actuar como vectores os mosquitos dos xéneros Culex, Anopheles, Culiseta, Mansonia e Aedes. Porén, os vectores coñecidos para a malaria humana (máis de 100 especies) pertencen ao xénero Anopheles. A malaria das aves é normalmente transmitida por especies de mosquitos do xénero Culex. En todos os casos, só pican as femias dos mosquitos. Ademais de con sangue, os dous sexos poden alimentarse de néctar, pero a femia necesita alimentarse unha ou dúas veces de sangue para poñer os ovos, porque hai moi poucas proteínas no néctar.
Ciclo de vida
editarO ciclo de vida de Plasmodium é moi complexo. Os esporozoítos da saliva vertida por un mosquito femia que pica transmítense ao sangue e sistema linfático[2] do receptor. Os esporozoítos migran ao fígado e invaden os hepatocitos. Este estado latente ou dormente dos esporozoítos no fígado denomínase hipnozoíto, onde poden permanecer latentes moitos anos.
O desenvolvemento desde os estadios hepáticos aos estadios eritrocíticos non foi claro durante moito tempo. En 2006[3] demostrouse que o parasito sae dos hepatocitos en forma de merosomas que conteñen centos ou miles de merozoítos. Estes merosomas seguidamente[4] se aloxan nos capilares pulmonares e desintégranse alí lentamente nunhas 48–72 horas liberando merozoítos. A invasión dos eritrocitos está potenciada cando o fluxo sanguíneo é lento e as células están moi estreitamente unidas, condicións ambas que se dan nos capilares alveolares.
Dentro dos eritrocitos o merozoíto crece primeiro para formar unha forma anular e despois un trofozoíto máis grande. No estadio de esquizonte, o parasito divídese varias veces para producir merozoítos, os cales abandonan os eritrocitos e viaxan polo sangue para invadir a máis eritrocitos. A maioría dos merozoítos continúan este ciclo replicativo, pero algúns merozoítos diferéncianse en formas sexuais masculinas e femininas chamadas gametocitos, o que ocorre tamén no sangue. Os gametocitos son absorbidos por mosquitos ao zugar sangue.
No intestino do mosquito, os gametocitos desenvólvense a gametos, que se fecundan, formando cigotos móbiles chamados oocinetos. Os oocinetos atravesan a parede do intestino e pasan ao exterior do mesmo, onde se incrustan no exterior da membrana intestinal. Alí, divídense moitas veces para producir un gran número de esporozoítos alongados diminutos. Estes esporozoítos migran ás glándulas salivares do mosquito, desde onde serán inxectados no sangue do seguinte hóspede cando o mosquito lle pique, e o ciclo comeza de novo.
O patrón de alternancia de reprodución sexual e asexual é común en especies parasitas, porque ten certas vantaxes evolutivas. Baixo condicións favorables, a reprodución asexual é superior á sexual, xa que o proxenitor está ben adaptado ao seu ambiente e os seus descendentes comparten todos os seus xenes. Ao haber transferencia a un novo hóspede ou en momentos de estrés, a reprodución sexual é xeralmente superior, xa que intercambia xenes dos dous proxenitores, producindo unha variabilidade nos individuos, algúns dos cales estarán mellor adaptados ao novo ambiente.
A reactivación dos hipnozoítos latentes pode tardar ata 30 anos despois da infección inicial en humanos. Os factores que causan esta reactivación son descoñecidos. Sábese que forman hipnozoítos as especies Plasmodium malariae, Plasmodium ovale e Plasmodium vivax. Ao contrario, a reactivación non ocorre en infeccións por Plasmodium falciparum. Non se sabe se a reactivación do hipnozoíto pode ocorrer con calquera das demais especies que ocasionalmente poden infectar aos humanos.
Evolución
editarO ciclo vital dos Plasmodium compréndese mellor á luz da evolución do seu grupo.
Considérase que os Apicomplexa, o filo ao que pertence Plasmodium, se orixinaron a partir de dinoflaxelados, un grande grupo de protozoos fotosintéticos. Crese que os antepasados dos apicomplexos eran orixinalmente organismos depredadores nos que evolucionou a capacidade de invadir as células intestinais e seguidamente perderon a súa capacidade fotosintética. Porén, algúns dinoflaxelados extintos podían invadir os corpos de medusas e continuar fotosintetizando, o cal é posible debido a que o corpo das medusas é case transparente e deixa pasar a luz. Noutros organismos de corpos opacos esta capacidade probablemente se perdeu rapidamente.
Pénsase que Plasmodium evolucionou a partir dun parasito transmitido pola ruta fecal-oral que infectaba a parede intestinal. En certo momento, este parasito desenvolveu a capacidade de infectar o fígado. Este patrón vese no xénero Cryptosporidium co cal o Plasmodium está distantemente relacionado. Nun momento posterior, este antepasado desenvolveu a capacidade de infectar células sanguíneas e infectar e sobrevivir en mosquitos. Unha vez que a transmisión utilizando os mosquitos quedou firmemente establecida, a previa ruta fecal-oral de transmisión acabou perdéndose.
Unha teoría moderna (2007) suxire que os xéneros Plasmodium, Hepatocystis e Haemoproteus evolucionaron a partir de especies de Leukocytozoon. Os parasitos do xénero Leukocytozoan infectan as células brancas do sangue (leucocitos), e células do fígado e bazo e transmítense polas moscas Simulium, que é un amplo xénero de moscas relacionadas cos mosquitos.
Os leucocitos, os hepatocitos e a maioría das células do bazo fagocitan activamente materia particulada facendo que a entrada dentro da célula sexa máis doada para o parasito. O mecanismo de entrada das especies de Plasmodium nos eritrocitos aínda non está moi claro tendo en conta que dura menos de 30 segundos. Non se sabe aínda se este mecanismo evolucionou antes de que os mosquitos se fixesen os principais vectores para a transmisión de Plasmodium.
Plasmodium evolucionou hai uns 130 millóns de anos. Este período coincidiu co rápido espallamento das anxiospermas (plantas con flor). Parece probable que o incremento no número de flores levase ao incremento no número de mosquitos e o seu contacto cos vertebrados.
Os mosquitos evolucionaron no que hoxe é Suramérica hai uns 230 millóns de anos. Existen unhas 3500 especies recoñecidas pero ata agora a súa evolución non está ben resolta o que fai que haxa algunhas lagoas no noso coñecemento da evolución de Plasmodium. Parece probable que as aves foran o primeiro grupo infectado por Plasmodium, seguido dos réptiles, probablemente os lagartos. En determinado momento, os primates e os roedores foron infectados polo parasito. O resto das especies infectadas fóra destes grupos probablemente o foron como resultado de eventos relativamente recentes.
En 2007, dispoñiase de secuencias de ADN de case sesenta especies destes parasitos, e a maioría destas eran de especies que infectan hóspedes roedores ou primates. A evolución proposta aquí é en parte especulativa e debería revisarse conforme se obteñan novos datos.
Bioloxía celular
editarTodas as especies examinadas ata agora teñen 14 cromosomas, unha mitocondria e un plastidio (un orgánulo similar a un cloroplasto). Os cormosomas varían desde un tamaño de 500 kb a 3,5 Mb. Crese que este é o patrón xeral do xénero. O plástidio, a diferenza do atopado nas algas, non é fotosintético. A súa función non se coñece pero hai algunhas evidencias que suxiren que pode estar implicado na reprodución.
A nivel molecular, o parasito produce danos nos glóbulos vermellos do sangue utilizando os seus encimas plasmepsinas, que son aspartato proteases que degradan a hemoglobina.
Taxonomía
editar- Véxase tamén: Lista de especies de Plasmodium.
O xénero Plasmodium pertence á familia Plasmodiidae (Levine, 1988), da orde Haemosporidia, filo Apicomplexa. Neste orde hai 450 especies recoñecidas. A taxonomía de moitas das especies desta orde está sendo reexaminada por medio de análises de ADN. É probable que moitas das especies sexan reasignadas cando se completen estes estudos.[5][6] Indícanse a continuación os subxéneros en que se subdivide Plasmodium:
- Xénero Plasmodium
- Subxénero Asiamoeba (lagartos)
- Subxénero Bennettinia (aves)
- Subxénero Carinamoeba (réptiles)
- Subxénero Giovannolaia (aves)
- Subxénero Haemamoeba (aves)
- Subxénero Huffia (aves)
- Subxénero Lacertamoeba (réptiles)
- Subxénero Laverania (primates superiores)
- Subxénero Novyella (aves)
- Subxénero Paraplasmodium (lagartos)
- Subxénero Plasmodium (monos, primates superiores)
- Subxénero Sauramoeba (réptiles)
- Subxénero Vinckeia (mamíferos non primates)
Os xéneros da orde Hemaesporidia Plasmodium, Fallisia e Saurocytozoon causan todos malaria en lagartos. Todos son transportados por dípteros. Os pigmentos están ausentes no hemosporidio Garnia. Os gametocitos non pigmentados son normalmente as únicas formas que se encontran en Saurocytozoon, pero poden atoparse formas pigmentadas nos leucocitos ocasionalmente. Fallisia produce formas non pigmentadas asexuais e formas de gametocitos en leucocitos e trombocitos.
Especies que infectan a humanos
editarAs especies de Plasmodium que máis comunmente infectan aos humanos son:
- Plasmodium falciparum (causa a malaria terciaria maligna)
- Plasmodium vivax (causa máis frecuente da malaria terciaria benigna)
- Plasmodium ovale (causa menos frecuente de malaria terciaria benigna)
- Plasmodium malariae (causa da malaria cuartá benigna)
- Plasmodium knowlesi (casos máis raros en humanos; normalmente noutros primates)
Outras especies infecciosas para os humanos menos comúns son:
- Plasmodium brasilianum
- Plasmodium cynomolgi
- Plasmodium cynomolgi bastianellii
- Plasmodium inui
- Plasmodium rhodiani
- Plasmodium schweitzi
- Plasmodium semiovale
- Plasmodium simium
As primeiras catro especies da lista son as que máis comunmente infectan a humanos. Case todos os casos mortais de malaria en humanos son causados pola primeira especie, P. falciparum, principalmente na África subsahariana. Co uso da reacción en cadea da polimerase identificáronse novas especies que poden infectar a humanos.
Informouse dalgunhas posibles infeccións en humanos por Plasmodium eylesi e P. tenue, pero a identificación foi insegura.[7][8] P. tenue foi proposta no mesmo ano (1914) como especie atopada en aves.
O único hóspede coñecido de P. falciparum e P. malariae é o ser humano. Porén, P. vivax pode infectar chimpancés e orangutáns. A infección nestes simios tende a ser de baixo grao pero pode persistir e permanecer como unha fonte de parasitos para os humanos durante algún tempo.[9]
P. ovale pode ser transmitido a chimpancés. P. ovale ten unha distribución pouco común, xa que se atopa en África, as Filipinas e Nova Guinea. A pesar de que se admite unha pobre capacidade de transmisión a chimpancés, dada a súa descontinua distribución, sospéitase que P. ovale é unha zoonose con algún hóspede primate natural non identificado.
Plasmodium shortii e Plasmodium osmaniae son agora considerados sinónimos de Plasmodium inui
A taxonomía en parasitoloxía antes da aparición de métodos baseados no ADN foi sempre problemática, e as revisións son frecuentes, orixinando moitos nomes obsoletos de especies de Plasmodium que infectan a humanos.[10]
| Nomes obsoletos de especies de Plasmodium que infectan aos humanos |
|---|
| P. camerense P. causiasium |
Referencias xerais
editarLibros estándar de referencia para a identificación de especies de Plasmodium:
- Laird, M. (1998). Avian Malaria in the Asian Tropical Subregion. Singapore: Springer. ISBN 9813083190.
- Garnham, P.C.C. (1966). Malaria Parasites And Other Haemosporidia. Oxford: Blackwell. ISBN 0397601328. Este é o libro de referencia básico sobre a clasificación de especies maláricas.
- Hewitt, R.I. (1940). Bird Malaria. American Journal of Hygiene 15. Baltimore: Johns Hopkins Press.
Outras referencias útiles:
- Shortt HE (1951). "Life-cycle of the mammalian malaria parasite". Br. Med. Bull. 8 (1): 7–9. PMID 14944807.
- Baldacci P, Ménard R (October 2004). "The elusive malaria sporozoite in the mammalian host". Mol. Microbiol. 54 (2): 298–306. PMID 15469504. doi:10.1111/j.1365-2958.2004.04275.x.
- Bledsoe GH (December 2005). "Malaria primer for clinicians in the United States" (PDF). South. Med. J. 98 (12): 1197–204; quiz 1205, 1230. PMID 16440920. Arquivado dende o orixinal (PDF) o 18 de marzo de 2009. Consultado o 04 de xuño de 2014.
Historia da malaria:
- Slater LB (2005). "Malarial birds: modeling infectious human disease in animals". Bull Hist Med 79 (2): 261–94. PMID 15965289. doi:10.1353/bhm.2005.0092.
Notas
editar- ↑ Chavatte JM, Chiron F, Chabaud A, Landau I (March 2007). "[Probable speciations by "host-vector 'fidelity'": 14 species of Plasmodium from magpies]". Parasite (en French) 14 (1): 21–37. PMID 17432055.
- ↑ "Malaria Parasites Develop in Lymph Nodes". HHMI News. Howard Hughes Medical Institute. 22 January 2006. Arquivado dende o orixinal o 03 de outubro de 2012. Consultado o 04 de xuño de 2014.
- ↑ Sturm A, Amino R, van de Sand C; et al. (September 2006). "Manipulation of host hepatocytes by the malaria parasite for delivery into liver sinusoids". Science 313 (5791): 1287–90. PMID 16888102. doi:10.1126/science.1129720.
- ↑ Baer K, Klotz C, Kappe SH, Schnieder T, Frevert U (November 2007). "Release of hepatic Plasmodium yoelii merozoites into the pulmonary microvasculature". PLoS Pathog. 3 (11): e171. PMC 2065874. PMID 17997605. doi:10.1371/journal.ppat.0030171.
- ↑ Perkins SL, Schall JJ (October 2002). "A molecular phylogeny of malarial parasites recovered from cytochrome b gene sequences". J. Parasitol. 88 (5): 972–8. PMID 12435139. doi:10.1645/0022-3395(2002)088[0972:AMPOMP]2.0.CO;2.
- ↑ Yotoko, K.S.C.; Elisei C. (November 2006). "Malaria parasites (Apicomplexa, Haematozoea) and their relationships with their hosts: is there an evolutionary cost for the specialization?". J. Zoo. Syst. Evol. Res. 44 (4): 265–273. doi:10.1111/j.1439-0469.2006.00377.x.
- ↑ Tsukamoto M (1977). "An imported human malarial case characterized by severe multiple infections of the red blood cells". Ann. Trop. Med. Parasit. 19 (2): 95–104.
- ↑ Russel P.F. (1928). "Plasmodium tenue (Stephens): A review of the literature and a case report". Am. J. Trop. Med. s1–8 (5): 449–479.
- ↑ Reid MJ, Ursic R, Cooper D; et al. (December 2006). "Transmission of human and macaque Plasmodium spp. to ex-captive orangutans in Kalimantan, Indonesia". Emerging Infect. Dis. 12 (12): 1902–8. PMC 3291341. PMID 17326942. doi:10.3201/eid1212.060191. Arquivado dende o orixinal o 24 de abril de 2009. Consultado o 04 de xuño de 2014.
- ↑ Coatney G.R., Roudabush R.L. (1936). "A catalog and host-index of the genus Plasmodium". J. Parasitol. 22 (4): 338–353. doi:10.2307/3271859.
Outros artigos
editarLigazóns externas
editar| Wikispecies posúe unha páxina sobre: Plasmodium |
- Malaria Atlas Project
- "Plasmodium". NCBI Taxonomy Browser. 5820.