ATPase de Na+/K+
A ATPase de Na+
/K+
(sodio-potasio adenosina trifosfatase, ou Na+
/K+
-ATPase, tamén coñecida como bomba de Na+
/K+
ou bomba de sodio-potasio) é un encima co número EC 3.6.3.9 (unha ATPase transmembrana electroxénica) que se encontra na membrana plasmática de todas as células animais. O encima ATPase de Na+
/K+
é unha bomba de solutos que bombea sodio fóra das células á vez que bombea potasio ao interior da célula, ambos en contra dos seus gradientes de concentración. Este bombeo é activo (é dicir, usa enerxía do ATP) e é importante para a fisioloxía celular. Un exemplo da súa aplicación no organismo é a condución nerviosa.
| Bomba de Na+/K+ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
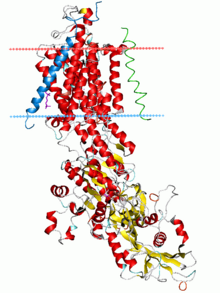
| |||||||||
| Bomba de sodio-potasio, estado E2-Pi. Os límites de hidrocarburos calculados da bicapa lipídica móstranse en planos azul (intracelular) e vermello (extracelular) | |||||||||
| Identificadores | |||||||||
| Número EC | 3.6.3.9 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| |||||||||
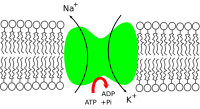

Ten unha actividade similar á dun antiportador, pero como despraza ambas as moléculas contra os seus gradientes de concentración non é un verdadeiro antiportador, o cal sempre necesita que un dos solutos se mova a favor do seu gradiente.
A súa función simple é bombear 3 ións sodio cara a fóra por cada 2 ións potasio que introduce na célula, e como ambos teñen igual carga iónica, isto crea un gradiente electroquímico entre a célula e o exterior. A proteína pode tamén facer que ocorra a operación inversa, empregando así a enerxía almacenada en forma de potencial de campo eléctrico. O proceso inverso é, a diferenza do anterior, espontáneo.
Bomba de sodio-potasio
editarA bomba de sodio é unha proteína de membrana que utiliza enerxía en forma de adenosín trifosfato (ATP) para realizar un transporte activo de ións sodio cara afóra da célula, que se intercambian por ións potasio que entran na célula. Por cada molécula de ATP que usa a bomba, expórtante 3 Na+ e impórtantse 2 K+, polo que hai unha exportación neta dunha carga positiva en cada ciclo da bomba. Todos os mamíferos teñen catro subtipos de bombas de sodio, ou isoformas, cada unha das cales ten propiedades únicas e padróns de expresións particulares nos tecidos.[1]
O seu funcionamento foi investigado seguindo o paso de ións etiquetados radioactivamente a través da membrana plasmática de certas células. Atopouse que as concentracións de ións sodio e potasio nos dous lados da membrana son interdependentes, o que suxiría que o mesmo transportador mobilizaba ambos os ións. Este transportador era unha ATPase.
A bomba de sodio-potasio foi descuberta na década de 1950 polo científico danés Jens Christian Skou, mentres estaba traballando como profesor axudante no Departamento de Fisioloxía da Universidade de Aarhus, Dinamarca. Publicou os seus traballos en 1957 .[2] Este descubrimento supuxo un importante paso adiante no coñecemento de como os ións entran e saen da célula e ten unha especial importancia nas células excitables como as neuronas, que dependen desta bomba para responder aos estímulos e transmitir impulsos. En 1997, Skou recibiu o Premio Nobel de Química compartido "polo primeiro descubrimento dun encima de transporte de ións Na+
, K+
-ATPase."[3]
Función
editarA ATPase de Na+
/K+
axuda a manter o potencial de repouso, efectuar o transporte e regular o volume celular.[4] Tamén funciona como transdutor/integrador de sinais para regular a vía MAPK, as especies reactivas do oxíxeno e o calcio intracelular. Na maioría das células animais, a ATPase de Na+
/K+
é responsable do 20 ao 40% do gasto de enerxía da célula. Nas neuronas esta cifra é de 2/3 do gasto total.[5]
Potencial de repouso
editar/K+
, xunto cos efectos da difusión dos ións implicados manteñen o potencial de repouso a través das membranas.
Para manter o potencial eléctrico das membranas celulares, a célula mentén unha concentración baixa de ións sodio e altos niveis de ións potasio dentro da célula. O mecanismo da bomba de sodio-potasio mobiliza tres ións sodio cara ao exterior e 2 ións potasio cara ao interior, polo que en total retira de forma neta unha carga positiva do espazo intracelular. (Ver Mecanismo para máis detalles).
Transporte
editarA exportación de sodio da célula proporciona a forza impulsora para varias proteínas de membrana transportadoras activas secundarias, que importan glicosa, aminoácidos, e outros nutrientes na célula utilizando o gradiente de sodio que se crea.
Outra importante tarefa da bomba de sodio-potasio é proporcionar un gradiente de Na+
que se utiliza en certos procesos de transporte. No intestino, por exemplo, o sodio é transportado desde a célula absorbente intestinal ao fluído intersticial do lado sanguíneo por medio da bomba de Na+
-K+
, mentres que, no lado reabsorbente (luminal), o simportador Na+
-glicosa usa o gradiente creado de Na+
como fonte de enerxía para importar tanto Na+
coma glicosa, o cal é moito máis eficente que unha difusión smple. Procesos similares localízanse no sistema tubular renal.
Control do volume celular
editarUnha insuficiencia no funcionamento da bomba de sodio-potasio pode orixinar o inchamento da célula. A osmolaridade dunha célula é a suma das concentracións de varias especies de ións e moitas proteínas e outros compostos orgánicos que hai dentro da célula. Cando esta é maior que a osmolaridade do exterior da célula, a auga flúe ao interior da célula debido á osmose. Isto pode causar que a célula se inche e se lise. A bomba de sodio-potasio axuda a manter as concentracións correctas de ións.
Función como transdutor de sinais
editarAdemais da clásica función de transporte de ións, desta bomba pode depender tamén a sinalización por unión de ouabaína extracelular na célula por medio da regulación da fosforilación de tirosina nas proteínas. Os sinais augas abaixo da ruta por medio de eventos de fosforilación de proteínas desencadeados pola ouabaína inclúen a activación das fervenzas de sinalización da proteína quinase activada por mitóxeno (MAPK), a produción de especies reactivas do oxíxeno, e a activación da fosfolipase C (PLC) e o receptor de inositol trifosfato (IP3R) en diferentes compartimentos intracelulares.[6]
As ìnteraccións proteína-proteína xogan un papel moi importante na transdución de sinais mediada pola bomba de sodio-potasio. Por exemplo, esta bomba interacciona directamente con Src, unha non receptor tirosina quinase, para formar un complexo receptor sinalizador.[7] A Src quinase é inhibida pola bomba de sodio-potasio, mentres que, por medio da unión de ouabaína, o dominio quinase da Src é liberado e despois activado. Baseándose neste escenario, desenvolveuse o NaKtide, un péptido inhibidor de Src derivado da bomba de sodio-potasio, que funciona como unha transdución de sinais mediada por unha bomba de ouabaína-Na+
-K+
funcional.[8] A bomba de sodio-potasio interacciona tamén coa anquirina, IP3R, PI3K, PLC-gamma e cofilina.[9]
Control dos estados de actividade das neuronas
editarA bomba de sodio-potasio tamén controla e fixa un modo de actividades intrínsecas das neuronas de Purkinje cerebelares[10], células mitrais do bulbo olfactorio accesorio[11] e probablemente outros tipos de neuronas.,[12] Isto suxire que a bomba podería non ser simplemente unha molécula homeostática de mantemento de gradientes iónicos, senón que podería ser un elemento de computación no cerebelo e cerebro.[13] De feito, unha mutación na bomba de sodio-potasio causa un comezo rápido do parkinsonismo distónico, que ten síntomas que indican que é unha patoloxía da computación cerebelar.[14] Ademais, un bloqueo por ouabaína das bombas de sodio-potasio no cerebelo dun rato vivo orixinan que este presente ataxia e distonía.[15] O alcohol inhibe as bombas de sodio-potasio no cerebelo e probablemente isto é o modo como se corrompe a computación cerebelar e a coordinación do corpo.[16][17] Demostrouse que a bomba de sodio-potasio en axóns mielinizados no cerebro humano está distribuída ao longo do axolema internodal e non no axolema nodal como se pensaba previamente.[18]
Mecanismo
editarA bomba funciona coa seguinte secuencia de acontecementos:
- Á bomba, únese primeiro unha molécula de ATP e despois 3 ións Na+
intracelulares.[4] - Hidrolízase o ATP, o que orixina a fosforilación da bomba nun residuo de aspartato moi conservado e a liberación do ADP.
- Un cambio conformacional na bomba expón os ións Na+
ao exterior da célula. A forma fosforilada da bomba ten unha baixa afinidade polos ións Na+
, polo que son liberados. - Á bomba únense 2 ións K+
extracelulares. Isto causa a desfosforilación da bomba, reverténdoa ao seu estado conformacional previo, transportando os ións K+
ao interior da célula. - A forma non fosforilada da bomba ten unha maior afinidade polos ións Na+
que polos ións K+
, e os 2 ións K+
unidos son liberados. O ATP únese á bomba de novo e o proceso empeza outra vez.
Regulación
editarEndóxena
editarA ATPase de Na+
/K+
está regulada á alza polo AMPc.[19] Así, as substancias que causan un incremento no AMPc regulan á alza a ATPase de Na+
/K+
. Estes inclúen os ligandos do GPCR acoplados á Gs. En contraste, as substancias que causan un decrecemento no AMPc regulan á baixa a ATPase de Na+
/K+
. Entre estas están os ligandos do GPCR acoplados á Gi.
Exóxena
editarA ATPase de Na+
-K+
pode ser farmacoloxicamente modificada administrando fármacos exoxenamente.
Por exemplo, a ATPase de Na+
-K+
que se encontrou na membrana das células do corazón é unha diana importante dos glicósidos cardíacos (por exemplo a digoxina e a ouabaína), drogas inotrópicas usadas para mellorar o rendemento do corazón incrementando a forza de contracción.
A contración muscular dependente de que se xere unha concentración de Ca2+
de 100 a 10 000 veces maior que no repouso, que está causada pola liberación de Ca2+
das células musculares do retículo sarcoplásmico. Inmediatamente despois da contracción muscular, o Ca2+
intracelular volve rapidamente á súa concentración normal por un encima transportador nunha membrana plasmática, e unha bomba de calcio no retículo sarcoplásmico, causando a relaxación do músculo.
Como o encima transportador (translocador de Na+
-Ca2+
) usa o gradiente de Na xerado pola bomba de Na+
-K+
para retirar o Ca2+
do espazo intracelular, o feito de diminuír a actividade da bomba de Na+
-K+
ten como resultado un nivel permanentemente elevado de Ca2+
no músculo, que pode ser o mecanismo dun efecto inotrópico a longo prazo dos glicósidos cardíacos como a digoxina.
Xenes
editarNotas
editar- ↑ Clausen MV, Hilbers F, Poulsen H (June 2017). "The Structure and Function of the Na,K-ATPase Isoforms in Health and Disease.". Frontiers in Physiology 8. PMC 5459889. PMID 28634454. doi:10.3389/fphys.2017.00371.
- ↑ Skou JC (February 1957). "The influence of some cations on an adenosine triphosphatase from peripheral nerves". Biochimica et Biophysica Acta 23 (2): 394–401. PMID 13412736. doi:10.1016/0006-3002(57)90343-8.
- ↑ "Chemistry 1997". Arquivado dende o orixinal o 16 de maio de 2008. Consultado o 11 de outubro de 2017.
- ↑ 4,0 4,1 Hall, John E.; Guyton, Arthur C. (2006). Textbook of medical physiology. St. Louis, Mo: Elsevier Saunders. ISBN 0-7216-0240-1.
- ↑ Howarth C, Gleeson P, Attwell D (July 2012). "Updated energy budgets for neural computation in the neocortex and cerebellum". J. Cereb. Blood Flow Metab. 32 (7): 1222–32. PMID 22434069. doi:10.1038/jcbfm.2012.35.
- ↑ Yuan Z, Cai T, Tian J, Ivanov AV, Giovannucci DR, Xie Z (September 2005). "Na/K-ATPase tethers phospholipase C and IP3 receptor into a calcium-regulatory complex". Molecular Biology of the Cell 16 (9): 4034–45. PMC 1196317. PMID 15975899. doi:10.1091/mbc.E05-04-0295.
- ↑ Tian J, Cai T, Yuan Z, et al. (January 2006). "Binding of Src to Na+/K+-ATPase forms a functional signaling complex". Molecular Biology of the Cell 17 (1): 317–26. PMC 1345669. PMID 16267270. doi:10.1091/mbc.E05-08-0735.
- ↑ Li Z, Cai T, Tian J, et al. (July 2009). "NaKtide, a Na/K-ATPase-derived peptide Src inhibitor, antagonizes ouabain-activated signal transduction in cultured cells". The Journal of Biological Chemistry 284 (31): 21066–76. PMC 2742871. PMID 19506077. doi:10.1074/jbc.M109.013821.
- ↑ Lee K, Jung J, Kim M, Guidotti G (January 2001). "Interaction of the alpha subunit of Na,K-ATPase with cofilin". The Biochemical Journal 353 (2): 377–85. PMC 1221581. PMID 11139403. doi:10.1042/0264-6021:3530377.
- ↑ Forrest MD, Wall MJ, Press DA, Feng J (December 2012). "The Sodium-Potassium Pump Controls the Intrinsic Firing of the Cerebellar Purkinje Neuron". PLoS ONE 7 (12): e51169. PMC 3527461. PMID 23284664. doi:10.1371/journal.pone.0051169.
- ↑ Zylbertal, Asaph; Kahan, Anat; Ben-Shaul, Yoram; Yarom, Yosef; Wagner, Shlomo (2015-12-16). "Prolonged Intracellular Na+ Dynamics Govern Electrical Activity in Accessory Olfactory Bulb Mitral Cells". PLOS Biology 13 (12): e1002319. ISSN 1545-7885. doi:10.1371/journal.pbio.1002319.
- ↑ Zylbertal, Asaph; Yarom, Yosef; Wagner, Shlomo (2017). "The Slow Dynamics of Intracellular Sodium Concentration Increase the Time Window of Neuronal Integration: A Simulation Study". Frontiers in Computational Neuroscience (en English) 11. ISSN 1662-5188. doi:10.3389/fncom.2017.00085.
- ↑ Forrest MD (December 2014). "The sodium-potassium pump is an information processing element in brain computation". Frontiers in Physiology 5 (472). doi:10.3389/fphys.2014.00472.
- ↑ Cannon C (July 2004). "Paying the Price at the Pump: Dystonia from Mutations in a Na+/K+-ATPase". Neuron 43 (2): 153–154. PMID 15260948. doi:10.1016/j.neuron.2004.07.002.
- ↑ Calderon DP, Fremont R, Kraenzlin F, Khodakhah K (March 2011). "The neural substrates of rapid-onset Dystonia-Parkinsonism". Nature Neuroscience 14 (3): 357–65. PMC 3430603. PMID 21297628. doi:10.1038/nn.2753.
- ↑ Forrest MD (April 2015). "Simulation of alcohol action upon a detailed Purkinje neuron model and a simpler surrogate model that runs >400 times faster". BMC Neuroscience 16 (27). doi:10.1186/s12868-015-0162-6.
- ↑ Forrest, Michael (April 2015). "the_neuroscience_reason_we_fall_over_when_drunk". Science 2.0. Consultado o May 2015.
- ↑ Young EA, Fowler CD, Kidd GJ, Chang A, Rudick R, Fisher E, Trapp BD (April 2008). "Imaging correlates of decreased axonal Na+/K+ ATPase in chronic multiple sclerosis lesions.". Ann Neurol 63 (4): 428–35. PMID 18438950. doi:10.1002/ana.21381.
- ↑ Burnier, Michel (2008). Sodium In Health And Disease. CRC Press. p. 15. ISBN 978-0-8493-3978-3.
Véxase tamén
editarOutros artigos
editarLigazóns externas
editar- Sodium, Potassium ATPase Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- RCSB Protein Data Bank : Sodium-Potassium PumpArquivado 06 de agosto de 2011 en Wayback Machine.
- vídeo Khan Academy.