Cortisol
O cortisol[1][2] (ou hidrocortisona[3]) é unha hormona esteroide do grupo dos glicocorticoides, producida na glándula adrenal.[4] Libérase en resposta ao estrés e a baixos niveis sanguíneos de glicocorticoides. As súas funcións principais son incrementar os niveis de azucre en sangue estimulando a glicoxenólise; suprime o sistema inmunitario; e intervén no metabolismo das graxas, proteínas e carbohidratos.[4] Ademais, fai diminuír a formación de tecido óseo. Durante o embarazo, o incremento da produción de cortisol entre as semanas 30 e 32 promove a maduración dos pulmóns fetais e o inicio da produción de surfactante. Utilízanse varias formas sintéticas do cortisol no tratamento de varias enfermidades.
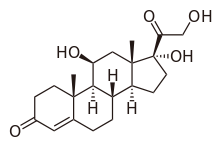
Nome IUPAC: (11β)-11,17,21-trihidroxipregn-4-eno-3,20-diona.
Número CAS: 50-23-7.
Fisioloxía
editarProdución e liberación
editarO cortisol prodúcese na zona fasciculada do córtex da glándula adrenal. A súa liberación está controlada polo eixe hipotalámico-hipofisario. O hipotálamo segrega hormona liberadora da corticotropina (CRH), a cal actúa sobre a adenohipófise ou pituitaria anterior estimulando a secreción de hormona adrenocorticotropa (ACTH), e esta hormona chega por vía sanguíneaáo córtex adrenal, onde activa a secreción de glicocorticoides.
Principais funcións
editarAs principais son:
- Incrementa os niveis de glicosa sanguíneos activando a glicoxenólise e reducindo a captación da glicosa nas células.
- Suprime o sistema inmunitario.
- Intervén no metabolismo de lípidos, proteínas e carbohidratos.
O cortisol regula á baixa o receptor de interleucina-2 (IL-2R) nas células Th (CD4+). Isto ten como resultado a imposibilidade de que a interleucina-2 active a resposta inmunitaria Th2 e orixina a dominancia inmunitaria das Th1. Isto orixina a diminución da produción de anticorpos polas células B. O cortisol impide a liberación de substancias que causan inflamación. Por esta razón o cortisol pode utilizarse no tratamento de enfermidades orixinadas por unha excesiva actividade da resposta humoral (produción de anticorpos) mediada polos linfocitos B como a que se dá en enfermidades inflamatorias e reumatoides e nas alerxias.
Estimula a gliconeoxénese no fígado e activa as vías antiinflamatorias e antiestrés.
Diminúe a formación de tecido óseo.
Niveis baixos de cortisol están asociados coa enfermidade de Addison.
Patróns
editarA cantidade de cortisol presente no sangue sofre unha variación diúrna; o pico máximo atínguese aproximadamente ás 8 da mañá, e chégase ao nivel mínimo pola noite aproximadamente ás 4 am, ou de 3 a 5 horas despois de comezar a durmir. Este patrón non se dá ao nacer, e vaise establecendo entre as dúas semanas e os 9 meses de vida.[5]
Observáronse cambios dos patróns normais nos niveis de cortisol sérico en casos de niveis anormais de ACTH, depresión, estrés, e de estresantes fisiolóxicos como hipoglicemia, enfermidades, febre, traumas, cirurxía, medo, dor, esforzos físicos ou temperaturas estremas. Os niveis de cortisol son tamén diferentes en individuos con autismo ou síndrome de Asperger.[6]
Niveis normais
editar| Rangos de referencia para o plasma sanguíneo do contido de cortisol libre | |||
|---|---|---|---|
| Tempo | Límite inferior | Límite superior | Unidade |
| 09:00 am | 140 | 700 | nmol/L |
| 5[7] | 25[7] | μg/dL | |
| Medianoite | 80 | 350 | nmol/L |
| 2.9[7] | 13[7] | μg/dL | |
Usando como peso molecular 362,460 g/mol, o factor de conversión para pasar de µg/dl a nmol/L é de aproximadamente 27,6; así, 10 µg/dl equivalen aproximadamente a 276 nmol/L.
| Rangos de referencia para análises de urina do cortisol libre | |||
|---|---|---|---|
| Límite inferior | Límite superior | Unidade | |
| 28[8] ou 30[9] | 280[8] ou 490[9] | nmol/24h | |
| 10[10] ou 11[11] | 100[10] ou 176[11] | µg/24 h | |
Unión a proteínas
editarA maioría do cortisol do soro sanguíneo (un 96%) está unido a proteínas, como a globulina que se une a corticosteroides (CBG) e a albumina sérica. O cortisol libre pasa facilmente a través das membranas celulares, e unha vez na célula únese a receptores intracelulares do cortisol.[12]
Regulación
editarO principal control da produción de cortisol exérceo a hormona ACTH da adenohipófise ou pituitaria anterior. A ACTH probablemente impulsa a produción de cortisol controlando o movemento de calcio nas células diana secretoras de cortisol.[13] A ACTH é á súa vez controlada pola hormona hipotalámica CRH, que está baixo control nervioso. A CRH actúa sinérxicamente coa arxinina vasopresina, anxiotensina II, e epinefrina.[14] Cando os macrófagos activados empezan a segregar interleucina-1 (IL-1), a cal sinerxicamente coa CRH incrementa a produción de ACTH,[15] as células T tamén segregan o factor modificador da resposta de glicosteroides (GRMF ou GAF) xunto con IL-1; ambas as substancias incrementan a cantidade de cortisol requirida para inhibir case todas as células inmunes.[16] As células inmunes asumen despois a súa propia regulación, pero a un punto de referencia de cortisol máis alto. O cortisol mesmo ten un efecto de retroalimentación negativa sobre a interleucina-1 [15], que é especialmente útil nas enfermidades nas que é beneficioso forzar o hipotálamo a segregar demasiada CRH, como nas doenzas causadas por bacterias endotóxicas. As células inmunitarias supresoras non son afectadas polo GRMF.[16] O GRMF (ou GAF) afecta principalmente ao fígado (máis cós riles) nalgúns procesos fisiolóxicos.[17]
Un alto nivel de potasio (que estimula a secreción de aldosterona in vitro) tamén estimula a secreción de cortisol na zona fasciculada das glándulas adrenais de can[18], a diferenza da corticosterona, sobre a cal o potasio non ten efecto.[19] A carga de potasio tamén incrementa a ACTH e o cortisol nos humanos.[20] Esta é probablemente a razón pola cal a deficiencia de potasio fai que os niveis de cortisol declinen e causa unha diminución na conversión do 11-desoxicortisol a cortisol.[21] Isto pode tamén exercer unha función na dor da artrite reumatoide, xa que os niveis de potasio celular son sempre baixos na artrite reumatoide.[22]
Trastornos da secreción de cortisol
editar- Hipercortisolismo: Niveis excesivos de cortisol no sangue. (Ver síndrome de Cushing.)
- Hipocortisolismo (insuficiencia adrenal): Niveis insuficientes de cortisol no sangue.
A relación entre os niveis de cortisol e de ACTH, e algúns dos trastornos que se poden producir son os da táboa:
| ACTH no plasma | |||
|---|---|---|---|
| ↓ | ↑ | ||
| Cortisol no plasma | ↑ | Hipercortisolismo primario (síndrome de Cushing) | Hipercortisolismo secundario (tumor hipofisario ou ectópico, enfermidade de Cushing, síndrome pseudo-Cushing) |
| ↓ | Hipocortisolismo secundario (tumor hipofisario, síndrome de Sheehan) | Hipocortisolismo primario (enfermidade de Addison, síndrome de Nelson) | |
Farmacoloxía
editarHidrocortisona é o termo farmacéutico que se utiliza para referirse ao cortisol usado para a súa administración oral, intravenosa ou tópica. Utilízase como fármaco inmunosupresor, administrado por inxección en casos de reaccións alérxicas graves como a anafilaxe e anxioedema, en lugar da prednisolona en pacientes que necesitan un tratamento de esteroides pero que non poden tomar a medicación por vía oral e en período perioperatorio en pacientes cun tratamento prolongado con esteroides para previr as crises da enfermidade de Addison. Tamén se pode usar topicamente para as erupcións alérxicas da pel, eccema, psoríase e outros trastornos inflamatorios da pel. Pode tamén administrarse por inxección en articulacións inflamadas debido a doenzas como a gota.
Bioquímica
editarBiosíntese
editarO cortisol sintetízase a partir do colesterol. A síntese ten lugar na zona fasciculada do córtex adrenal. A síntese de cortisol na glándula adrenal está estimulada pola hormona adrenocorticotropa (ACTH) da hipófise, a produción da cal está estimulada pola CRH do hipotálamo. A ACTH incrementa a concentración de colesterol na membrana mitocondrial interna, por medio da regulación da proteína STAR (steroidogenic acute regulatory, proteína regulatoria aguda esteroidoxénica). Tamén estimula o principal paso limitante da síntese do cortisol, no cal o colesterol se converte en pregnenolona, catalizado polo citocromo P450SCC (encima de corte da cadea lateral).
Metabolismo
editarO cortisol é metabolizado polo sistema da 11-beta hidroxiesteroide deshidroxenase (11-beta HSD), que consta de dous encimas: 11-beta HSD1 e 11-beta HSD2.
- A 11-beta HSD1 utiliza o cofactor NADPH para converter a cortisona bioloxicamente inerte en cortisol bioloxicamente activo.
- A 11-beta HSD2 utiliza o cofactor NAD+ para converter o cortisol en cortisona.
En conxunto, o efecto neto é que a 11-beta HSD1 serve para incrementar as concentracións locais de cortisol bioloxicamente activo nos tecidos; e a 11-beta HSD2 serve para reducir ditas concentracións.
O cortisol tamén se metaboliza a 5-alfa tetrahidrocortisol (5-alfa THF) ed 5-beta tetrahidrocortisol (5-beta THF), reaccións nas que os factores limitantes son, respectivamente, a 5-alfa redutase e a 5-beta redutase. A 5-beta redutase é tamén o factor limitante na conversión de cortisona a tetrahidrocortisona (THE).
Notas
editar- ↑ ChemSpider Cortisol Arquivado 23 de maio de 2012 en Wayback Machine.
- ↑ CHEBI Cortisol
- ↑ PubChem compound Hydrocortisone
- ↑ 4,0 4,1 Scott, Elizabeth (22 September 2011). "Cortisol and Stress: How Cortisol Affects Your Body, and How To Stay Healthy in the Face of Stress". Stress.about.com. Arquivado dende o orixinal o 01 de novembro de 2012. Consultado o 29 November 2011.
- ↑ de Weerth C, Zijl R, Buitelaar J (2003). "Development of cortisol circadian rhythm in infancy". Early Hum Dev 73 (1-2): 39–52. PMID 12932892. doi:10.1016/S0378-3782(03)00074-4.
- ↑ "Asperger's stress hormone 'link'". BBC News. 2009-04-02. Consultado o 2010-04-30.
- ↑ 7,0 7,1 7,2 7,3 Derivados dos valores molares usando como masa molar 362 g/mol
- ↑ 8,0 8,1 Convertido a partir dos valores en µg/24h, usando como masa molar 362,460 g/mol
- ↑ 9,0 9,1 Görges, R.; Knappe, G.; Gerl, H.; Ventz, M.; Stahl, F. (1999). "Diagnosis of Cushing's syndrome: Re-evaluation of midnight plasma cortisol vs urinary free cortisol and low-dose dexamethasone suppression test in a large patient group". Journal of endocrinological investigation 22 (4): 241–249. PMID 10342356.
- ↑ 10,0 10,1 MedlinePlus > Cortisol - urine. Update Date: 11/23/2009. Updated by: Ari S. Eckman. Also reviewed by David Zieve.
- ↑ 11,0 11,1 Convertido a partir de from nmol/24h, usando como masa molar 362,460 g/mol
- ↑ Boron and Boulpaep, Medical physiology 2009
- ↑ Davies E., Keyon C.J., Fraser R. (1985). "The role of calcium ions in the mechanism of ACTH stimulation of cortisol synthesis". Steroids 45 (6): 557. PMID 3012830.
- ↑ Plotsky PM, Otto S, Sapolsky RM (1986). "Inhibition of immunoreactive corticotropin-releasing factor secretion into the hypophysial-portal circulation by delayed glucocorticoid feedback". Endocrinology 119 (3): 1126–30. PMID 3015567. doi:10.1210/endo-119-3-1126.
- ↑ 15,0 15,1 Besedovsky, H.O.; Del Rey, A.; Sorkin, E. (1984) "Integration of Activated Immune Cell Products in Immune Endocrine Feedback Circuits." p. 200 in Leukocytes and Host Defense Vol. 5 [Oppenheim, J.J.; Jacobs, D.M., eds]. Alan R. Liss, New York,.
- ↑ 16,0 16,1 Fairchild SS, Shannon K, Kwan E, Mishell RI (February 1984). "T cell-derived glucosteroid response-modifying factor (GRMFT): a unique lymphokine made by normal T lymphocytes and a T cell hybridoma". J. Immunol. 132 (2): 821–7. PMID 6228602.
- ↑ Stith RD, McCallum RE (1986). "General effect of endotoxin on glucocorticoid receptors in mammalian tissues". Circ. Shock 18 (4): 301–9. PMID 3084123.
- ↑ Mikosha, A.S.; Pushkarov, I.S.; Chelnakova, I.S.; Remennikov, G.Y.A. (1991) “Potassium Aided Regulation of Hormone Biosynthesis in Adrenals of Guinea Pigs Under Action of Dihydropyridines: Possible Mechanisms of Changes in Steroidogenesis Induced by 1,4, Dihydropyridines in Dispersed Adrenocorticytes.” Fiziol. [Kiev] 37: 60,.
- ↑ Mendelsohn FA, Mackie C (1975). "Relation of intracellular K+ and steroidogenesis in isolated adrenal zona glomerulosa and fasciculata cells". Clin Sci Mol Med 49 (1): 13–26. PMID 168026.
- ↑ Ueda Y, Honda M, Tsuchiya M; et al. (1982). "Response of plasma ACTH and adrenocortical hormones to potassium loading in essential hypertension". Jpn. Circ. J. 46 (4): 317–22. PMID 6283190.
- ↑ Bauman K Muller J 1972 “Effect of potassium on the final status of aldosterone biosynthesis in the rat. I 18-hydroxylation and 18hydroxy dehydrogenation. II beta-hydroxylation.” Acta Endocrin. Copenh. 69; I 701-717, II 718-730.
- ↑ LaCelle PL et al. (1964) “An investigation of total body potassium in patients with rheumatoid arthritis.” Proceedings of the Annual Meeting of the American Rheumatism Association, Arthritis and Rheumatism 7; 321.
Véxase tamén
editarLigazóns externas
editar- Dosage Side Effects and Drug Interaction Warnings Arquivado 05 de marzo de 2012 en Wayback Machine.
- How to stay healthy with Cortisol Arquivado 01 de novembro de 2012 en Wayback Machine.