Metanosulfonato de etilo
O metanosulfonato de etilo ou etil metanosulfonato (EMS) é un composto orgánico que é o éster etílico do ácido metanosulfónico, con propiedades de mutáxeno, teratóxeno e carcinóxeno, coa fórmula C3H8SO3. Produce mutacións ao chou no material xenético por substitución de nucleótidos, especialmente transicións de G:C a A:T inducidas pola alquilación da guanina.[3] O EMS produce tipicamente só mutacións puntuais. Debido á súa potencia e espectro mutacional ben coñecido, o uso máis común do EMS é como mutáxeno químico en xenética experimental.[4] As mutacións inducidas pola exposición ao EMS poden ser estudadas despois en cribados xenéticos ou outros ensaios.
| Metanosulfonato de etilo[1] | |
|---|---|
 | |
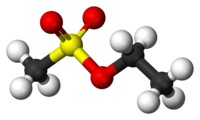 | |
Outros nomes Etil mesilato | |
| Identificadores | |
| Abreviaturas | EMS |
| Número CAS | 62-50-0 |
| PubChem | 6113 |
| ChemSpider | 5887 |
| UNII | 9H154DI0UP |
| KEGG | C19239 |
| ChEBI | CHEBI:23994 |
| ChEMBL | CHEMBL338686 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | CH3SO3C2H5 |
| Masa molecular | 124.16 g/mol |
| Aspecto | Líquido incoloro claro |
| Densidade | 1,1452 g/cm3 (22 °C) |
| Punto de fusión | < 25 °C |
| Punto de ebulición | 85–86 °C; 185–187 °F; 358–359 K |
| Presión de vapor | 0,044 kPa a 25˚C[2] |
| Perigosidade | |
| Pictogramas GHS |  
|
| Palabra sinal GHS | Danger (Perigo) |
| declaración de perigosidade GHS | 302 , 340, 351 |
| declaración de precaución GHS | 203 , 264 , 270 , 280 , 301+317 , 318 , 330 , 405 , 501 |
| NFPA 704 | |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
Uso en investigación biolóxica
editarO EMS pode inducir mutacións a unha taxa de 5·10−4 a 5·10−2 por xene sen producir unha mortalidade substancial. A taxa de mutación de 5·10−4 por xene observada nun experimento típico de mutaxénese por EMS do organismo modelo Caenorhabditis elegans corresponde a unha taxa de mutación crúa de ~7x10−6 mutacións por par de bases G/C, ou dunhas 250 mutacións nun gameto orixinalmente mutaxenizado (que contén un xenoma haploide de ~100 Mbp e 36% GC).[5] Tales gametos mutaxenizados terían en consecuencia unhas 9 mutación diferentes de perda de función nos xenes, e unha ou dúas destas mutacións estarían en xenes esenciais e, polo tanto, serían mortais. Porén, como é improbable que sufra mutación o mesmo xene esencial en gametos independentes, se a perda do xene esencial non mata o propio gameto, a posterior fusión con outro gameto adoita permitir a supervivencia do cigoto e organismo resultante, xa que o novo heterocigoto cun alelo mutado non funcional pode ser rescatado polo outro alelo de tipo silvestre que o acompaña procedente do outro gameto.[5]
Mecanismo da mutaxénese
editarO grupo etilo do EMS reacciona con guaninas do DNA, formando a base anormal O6-etilguanina. Durante a replicación do ADN, as ADN polimerases que catalizan o proceso sitúan frecuentemente timina en lugar de citosina en fronte dunha O6-etilguanina. Despois de máis roldas de replicación, o par de bases G:C orixinal pode converterse nun par A:T (unha mutación de transición). Estes cambios na información xenética adoitan ser daniños para as células e poden causar doenzas. A ARN polimerase pode tamén situar uridina (análogo no ARN da timina) fronte a unha lesión de O6-etilguanina.[6]
Reparación de lesións mutaxénicas
editarA O6-etilguanina pode ser reparada in vivo de maneira estequiométrica ao reaccionar co sitio activo de cisteína da proteína de reparación O-6-metilguanina-ADN metiltransferase.[7] A vida media in vivo da O6-etilguanina é duns 9 días no cerebro de rato, mentres que é de aproximadamente 1 día no fígado de rato.[8]
Indución da recombinación
editaro EMS induce a recombinación mitótica en Saccharomyces cerevisiae.[9] Sinalouse que os danos no ADN xerados polo EMS poden causar un proceso de reparación que conduce a un cambio xenético.[9]
Os mutantes do bacteriófago T4 defectivos en calquera dos seis xenes que se sabe cómpren para a recombinación xenética son máis sensibles á inactivación por EMS que os bacteriófagos de tipo silvestre.[10] Este descubrimento suxire que se emprega un proceso de recombinación catalizado polas proteínas codificadas por estes xenes na reparación de lesións mortais no ADN causadas polo EMS.[10]
Estabilidade
editarFalando en xeral, o EMS é inestable en auga e sofre hidrólise dando etanol e ácido metanosulfónico; porén, a pH neutro ou ácido á temperatura dunha habitación, ten unha vida media bastante longa de arredor dun día.[11][12] Por tanto, o EMS debe ser especificamente degradado antes de tiralo como refugallo. Os protocolos sinalan que hai que facer a degradación do EMS nun volume igual de "solución inactivante" de NaOH 0.1M e 20 % m/v de tiosulfato de sodio, durante polo menos seis vidas medias (>24 horas).[5] A vida media do EMS en NaOH 1M é de 6 horas á temperatura dunha habitación, mentres que nunha solución ao 10% m/v de tiosulfato de sodio ten unha vida media de 1,4 horas.[12]
Notas
editar- ↑ Merck Index, 11ª edición, 3782.
- ↑ "Ethyl Methanesulfonate" (PDF). Report on Carcinogens, Fourteenth Edition. NIEHS. Consultado o 18 de xuño de 2021.
- ↑ Sega, Gary A. (1984). "A review of the genetic effects of ethyl methanesulfonate". Mutation Research/Reviews in Genetic Toxicology (Elsevier BV) 134 (2–3): 113–142. ISSN 0165-1110. PMID 6390190. doi:10.1016/0165-1110(84)90007-1.
- ↑ Kutscher, Lena M.; Shaham, Shai (2014). "Forward and reverse mutagenesis in C. elegans". WormBook: The Online Review of C. Elegans Biology (WormBook): 1–26. PMC 4078664. PMID 24449699. doi:10.1895/wormbook.1.167.1. Consultado o 18 de xuño de 2021.
- ↑ 5,0 5,1 5,2 Anderson, Philip (1995). "Chapter 2 Mutagenesis". Caenorhabditis elegans: Modern Biological Analysis of an Organism. Methods in Cell Biology 48. Elsevier. pp. 31–58. ISBN 978-0-12-564149-4. ISSN 0091-679X. doi:10.1016/s0091-679x(08)61382-5.
- ↑ Gerchman, Lois L.; Ludlum, David B. (1973). "The properties of in templates for RNA polymerase". Biochimica et Biophysica Acta (BBA) - Nucleic Acids and Protein Synthesis (Elsevier BV) 308 (2): 310–316. ISSN 0005-2787. PMID 4706005. doi:10.1016/0005-2787(73)90160-3.
- ↑ Pegg, Anthony E (2000). "Repair of O6-alkylguanine by alkyltransferases". Mutation Research/Reviews in Mutation Research (Elsevier BV) 462 (2–3): 83–100. ISSN 1383-5742. PMID 10767620. doi:10.1016/s1383-5742(00)00017-x.
- ↑ Goth, R.; Rajewsky, M. F. (1974-03-01). "Persistence of O6-Ethylguanine in Rat-Brain DNA: Correlation with Nervous System-Specific Carcinogenesis by Ethylnitrosourea". Proceedings of the National Academy of Sciences 71 (3): 639–643. Bibcode:1974PNAS...71..639G. ISSN 0027-8424. PMC 388067. PMID 4522778. doi:10.1073/pnas.71.3.639.
- ↑ 9,0 9,1 Yost Jr, H. T.; Chaleff, R. S.; Finerty, J. P. (1967). "Induction of mitotic recombination in Saccharomyces cerevisiae by ethyl methane sulphonate". Nature 215 (5101): 660–661. Bibcode:1967Natur.215..660Y. PMID 6050236. doi:10.1038/215660a0.
- ↑ 10,0 10,1 Johns, V.; Bernstein, C.; Bernstein, H. (1978). "Recombinational repair of alkylation lesions in phage T4. II. Ethyl methanesulfonate". Molecular & General Genetics 167 (2): 197–207. PMID 215891. doi:10.1007/BF00266913.
- ↑ FROESE-GERTZEN, EDITH E.; KONZAK, C. F.; FOSTER, R.; NILAN, R. A. (1963). "Correlation between Some Chemical and Biological Reactions of Ethyl Methanesulphonate". Nature (Springer Science and Business Media LLC) 198 (4879): 447–448. Bibcode:1963Natur.198..447F. ISSN 0028-0836. doi:10.1038/198447a0.
- ↑ 12,0 12,1 Kodym, Andrea; Afza, Rownak (2003). "Chapter 12 Physical and Chemical Mutagenesis". Plant functional genomics. Totowa, N.J: Humana Press. pp. 189–203. ISBN 978-1-58829-145-5. OCLC 51445955.
