Anticorpo antinuclear
Os anticorpos antinucleares (ANAs polas súas siglas en inglés), tamén chamados factor antinuclear (ANF),[2] son autoanticorpos que se unen a contidos do núcleo celular. En individuos normais, o sistema inmunitario produce anticorpos contra as proteínas alleas (antíxenos alleos) pero non contra as proteínas humanas propias (autoantíxenos). Porén, en casos de autoinmunidade, o corpo produce anticorpos contra os antíxenos propios, como ocorre cos ANAs.[3]

Hai moitos subtipos de ANAs, como os anticorpos anti-Ro, anti-La, anti-Sm, anti-nRNP, anti-Scl-70, anti-dsDNA, antihistonas, anticorpos contra aos complexos dos poros nucleares, anticorpos anticentrómeros e anti-sp100. Cada un destes subtipos de anticorpos únese a diferentes proteínas ou complexos proteicos do interior do núcleo. Atopáronse en moitos trastornos como a autoinmunidade, o cancro e a infección, con diferentes prevalencias de anticorpos dependendo da condición. Isto permite o uso dos ANAs na diagnose dalgúns trastornos autoinmunes, como o lupus eritematoso sistémico, a síndrome de Sjögren,[4] esclerodermia,[5] enfermidade mixta do tecido conectivo,[6] polimiosite, dermatomiosite, hepatite autoinmune[7] e lupus inducido por fármacos.[8]
O test de ANAs detecta os autoanticorpos presentes no soro sanguíneo dun individuo. Os tests comúns usados para detectar e cuantificar os ANAs son a inmunofluorescencia indirecta e o ensaio inmunosorbente de encima ligado (ELISA). Na inmunofluorescencia, o nivel de anticorpos indícase como unha titulación. Esta é a maior dilución do soro á cal aínda se poden detectar os anticorpos. As titulacións positivas para os autoanticorpos a unha dilución igual ou maior de 1:160 adoitan considerarse como clinicamente significativas. As titulacións positivas de menos de 1:160 aparecen en ata o 20 % da poboación sa, especialmente nos vellos. Aínda que as titulacións positivas de 1:160 ou maiores están fortemente asociadas con trastornos autoinmunes, tamén se atopan nun 5 % dos individuos sans.[9][10] O cribado de autoanticorpos é útil no diagnóstico de trastornos autoinmunes e a monitorización dos niveis axuda a predicir a progresión da doenza.[8][11][12] Un test positivo de ANAs raramente é útil se non hai ademais outros datos de laboratorio ou clínicos que apoien o diagnóstico.[13]
Inmunidade e autoinmunidade
editarO corpo humano ten moitos mecanismos de defensa contra os patóxenos, un dos cales é a inmunidade humoral. Este mecanismo de defensa produce anticorpos (grandes glicoproteínas) en resposta a un estímulo inmune. Cómpre a actuación de moitas células do sistema inmune para este proceso funcione, como os linfocitos (células T e B) e células presentadoras de antíxenos. Ests células coordinan unha resposta inmune detectando as moléculas estrañas, normalmente proteínas (antíxenos), producindo anticorpos que se unen a estes antíxenos. Na fisioloxía normal, os linfocitos que recoñecen proteínas humanas (autoantíxenos) sofren unha morte celular programada (apoptose) ou convértense en non funcionais. Esta autotolerancia significa que os linfocitos non deberían incitar unha resposta inmune contra os antíxenos celulares humanos propios. Con todo, ás veces este proceso funciona mal e prodúcense anticorpos contra antíxenos propios (autoanticorpos), o cal orixina unha doenza autoinmune. Un grupo deses autoanticorpos son os ANAs.[3]
Subtipos de ANAs
editarOs ANAs encóntranse en moitos trastornos, pero tamén en individuos sans. Entre estes trastornos están: lupus eritematoso sistémico, artrite reumatoide, síndrome de Sjögren, esclerodermia, polimiosite, dermatomiosite, cirrose biliar primaria, lupus inducido por fármacos, hepatite autoimmune, esclerose múltiple, lupus discoide, enfermidade tiroide, síndrome antifosfolípidos, artrite idiopática xuvenil, artrite psoriática, dermatomiosite xuvenil, púrpura trombocitopénica idiopática, infeccións e cancro. Estes anticorpos poden subdividirse de acordo coa súa especificidade, e cada subgrupo ten diferentes propensións para tastornos específicos.[8][14]
Antíxenos nucleares extraíbles
editarOs antíxenos nucleares extraíbles son un grupo de autoantíxenos que foron orixinalmente identificados como dianas de anticorpos en persoas con trastornos autoinmunes. Denomínanse antíxenos nucleares extraíbles porque poden extraerse do núcleo celular con solución salina.[8][15] Os antíxenos nucleares extraíbles consisten en ribonucleoproteínas e proteínas non histonas, denominadas polo nome do doante que proporcionou o soro prototipo (Sm, Ro, La, Jo; por exemplo Sm significa Smith), ou o nome da da doenza no marco da cal se atoparon os anticorpos (SS-A, SS-B, Scl-70; por exemplo SS significa síndrome de Sjögren).[16]
Anti-Ro/SS-A e anti-La/SS-B
editarOs anticorpos anti-Ro e anti-La, tamén coñecidos como SS-A e SS-B, respectivamente, obsérvanse comunmente na síndrome de Sjögren primaria, unha doenza autoinmune que afecta as glándulas exócrinas. A presenza de ambos os anticorpos atópase nun 30–60 % dos casos de síndrome de Sjögren, os anticorpos anti-Ro sós atópanse no 50–70 % dos casos de síndrome de Sjögren e no 30 % dos casos de lupus eritematoso sistémico con afectación cutánea, e os anticorpos anti-La raramente se illan sós.[11][17] Os anticorpos anti-La tamén se atopan no lupus eritematoso sistémico; porén, eses pacientes adoitan ter tamén síndrome de Sjögren.[18] Os anticorpos anti-Ro tamén se atopan menos frecuentemente noutros trastornos incluíndo as enfermidades hepáticas autoinmunes, enfermidade celíaca, doenzas reumáticas autoinmunes, lupus eritematoso cardíaco neonatal e a polimiosite.[19][20] Durante o embarazo, os anticorpos anti-Ro poden cruzar a placenta e causar bloqueo cardíaco[21][22] e lupus neonatal en bebés.[23] Na síndrome de Sjögren, os anticorpos anti-Ro e anti-La correlaciónanse cun comezo temperán, aumento da duración da enfermidade, hipertrofia da glándula parótide, enfermidade fóra das glándulas e infiltración das glándulas por linfocitos.[12] Os anticorpos anti-Ro son específicos de compoñentes do complexo Ro-RNP, que comprende proteínas de 45 kDa, 52 kDa, 54 kDa e 60 kDa e ARN. A proteína de 60 kDa que se une ao ADN/ARN e a protéina regulatoria de 52 kDa de célula T son os antíxenos mellor caracterizados dos anticorpos anti-Ro. En conxunto, estas proteínas forman parte dun complexo de ribonucleoproteínas (RNP) que se asocian co ARN Y humano hY1-hY5. O antíxeno La é un factor de teminación da transcrición de 48 kDa da ARN polimerase III, que se asocia co complexo Ro-RNP.[16][17][24][25]
O mecanismo da produción de anticorpos na síndrome de Sjögren non se comprende totalmente, pero a apoptose (morte celular programada) e o mímetismo molecular poden xogar un papel.[12] Os antíxenos Ro e La exprésanse na superficie de células que están sufrindo apoptose e poden causar a inflamación das glándulas salivares pola interacción con células do sistema inmunitario. Os anticorpos poden tamén producirse por mimetismo molecular, no cal anticorpos con reactividade cruzada se unen tanto a virus coma a proteínas humanas. Isto pode ocorrer cun dos antíxenos, Ro ou La, e pode producir seguidamene anticorpos para outras proteínas por un proceso chamado extensión do epítopo. A proteína retroviral gag mostra semellanza coa proteína La e propúxose como posible exemplo de mimetismo molecular na síndrome de Sjögren.[12][20]
Anti-Sm
editarOa anticorpos anti-Smith (anti-Sm) son un marcador moi específico para o lupus eritematoso sistémico. Aproximadamente o 99 % dos individos sen lupus eritematoso sistémico carecen de anticorpos anti-Sm, pero só o 20 % das persosas que si teñen ese lupus teñen os anticorpos. Están asociados coa afectación do sistema nervioso central, enfermidade renal, fibrose pulmonar e pericardite no lupus eritematoso sistémico, pero non están asociados coa actividade da enfermidade. Os antíxenos dos anticorpos anti-Sm son as unidades centrais das ribonucleoproteínas nucleares pequenas (snRNPs), denominadas do A ao G, e únense ás snRNPs U1, U2, U4, U5 e U6. Normalmente, os anticorpos son específicos para as unidades B, B' e D.[26][27] Os estudos moleculares e epidemiolóxicos suxiren que os anticorpos anti-Sm poden ser inducidos por mimetismo molecular porque a proteína mostra algunha semellanza coas proteínas do virus de Epstein-Barr.[28][29]
Anti-nRNP/anti-U1-RNP
editarOs anticorpos anti-ribonucleoproteína nuclear (anti-nRNP), tamén coñecidos como anticorpos anti-U1-RNP encóntranse nun 30-40 % dos casos de lupus eritematoso sistémico. Adoitan encontrarse con anticorpos anti-Sm, pero poden estar ligados a diferentes asociacións clínicas. Ademais de co lupus eritemastoso sistémico, estes anticorpos están moi asociados coa enfermidade mixta do tecido conectivo. Os anticorpos anti-nRNP recoñecen as unidades centrais A e C das snRNPs e debido a isto únense principalmente ao snRNP U1.[26][30] A resposta inmune ás RNP pode ser causada pola presentación dos compoñentes nucleares na membrana celular en blebs apoptóticos. Tamén se sinalou que o mimetismo molecular é un posible mecanismo para a produción de anticorpos para estas proteínas debido á semellanza entre os polipéptidos snRNP U1 e os polipéptidos do virus de Epstein-Barr.[31]
Anti-Scl-70/anti-topoisomerase I
editarOs anticorpos anti-Scl-70 están ligados á esclerodermia.[32] A sensibilidaded aos antibióticos na esclerodermia é de aproximadamente o 34 %, pero é maior en casos con afectación cutánea difusa (40 %), e menor para a afectación cutánea limitada (10 %). A especificidade dos anticorpos é do 98 % e do 99,6 % noutras doenzas reumáticas e en individuos normais, respectivamente.[8][33] Ademais da esclerodermia, estes antcorpos atópanse en aproximadamente o 5 % dos individuos con lupus eritematoso sistémico.[34] A diana antixénica dos anticorpos anti-Scl-70 é a topoisomerase I.[35]
Anti-Jo-1
editarAínda que os anticorpos anti-Jo-1 se inclúen normalmente entre os ANAs, en realidade son anticorpos contra unha proteína citoplasmática, a histidil-ARNt sintetase, unha aminoacil-ARNt sintetase esencial para a síntese de ARNt cargado de histidina.[15] Están fortemente asociados coa polimiosite e a dermatomiosite, e encóntranse raramente noutras enfermidades do tecido conectivo. Arredor do 20–40 % dos casos de polimiosite son positivos para os anticorpos anti-Jo-1 e a maioría terán os marcadores do antíxeno leucocitario humano (HLA) HLA-DR3 e HLA-DRw52 de enfermidade pulmonar intersticial; o que se coñece en conxunto como síndrome Jo-1.[26][36]
Anti-ADN bicatenario (anti-dsDNA)
editarOs anticorpos anti-ADN bicatenario ou anti-dsDNA (do inglés double stranded DNA) están moi asociados co lupus eritematoso sistémico. Son un marcador moi específico para esa doenza, e nalgúns estudos cítase que o son case ao 100 %.[8] Os datos sobre a sensibilidade van do 25 ao 85 %. Os niveis de anticorpos anti-dsDNA, chamados titulacións, correlaciónanse coa actividade da enfermidade no lupus eritematoso sistémico; uns niveis altos indican un lupus máis activo. A presenza de anticorpos anti-dsDNA está tamén ligada á nefropatía lúpica e hai evidencias de que son a súa causa. Algúns anticorpos anti-dsDNA teñen reactividade cruzada con outros antíxenos atopados na membrana basal glomerular dos riles, como o heparán sulfato, coláxeno IV, fibronectina e laminina. A unión destes antíxenos nos riles podería causar inflamación e fixación do complemento, o que ten como resultado danos nos riles. A presenza dun alto grao de unión ao ADN e baixos niveis de C3 ten un valor altamente preditivo (94 %) para a diagnose de lupus eritematoso sistémico.[37] Tamén é posible que os anticorpos anti-dsDNA sexan internalizados polas células cando se unen a antíxenos de membrana e despois son presentados na superficie celular. Isto podería promover respostas inflamatorias das células T nos riles. É importante sinalar que non todos os anticorpos anti-dsDNA están asociados coa nefropatía lúpica e que outros factores poden causar estes síntomas na súa ausencia. O antíxeno dos anticorpos anti-dsDNA é o ADN bicatenario.[38][39]
Anticorpos antihistonas
editarOs anticorpos anti-histonas atópanse no soro do 75–95 % de persoas con lupus inducido por fármacos e do 75 % con lupus eritematoso sistémico idiopático. A diferenza dos anticorpos anti-dsDNA no lupus eritematoso sistémico, estes anticorpos non fixan o complemento.[Cómpre referencia] Aínda que se encontran comunmente no lupus inducido por fármacos, tamén se atopan nalgúns casos de lupus eritematoso sistémico, esclerodermia, artrite reumatoide e enfermidade do tecido conectivo indiferenciada. Moitos fármacos causan lupus inducido por fármacos e producen varias dianas antixénicas dentro do nucleosoma que a miúdo teñen reactividade cruzada con varias proteínas histonas e o ADN. A procainamida causa unha forma de lupus inducido por fármacos que produce anticorpos contra as histonas do complexo H2B e H2A.[40][41]
Anti-gp210 e anti-p62
editarTanto os anticorpos anti-glicoproteína-210 (anti-gp210) coma os anti-nucleoporina 62 (anti-p62) son anticorpos contra compoñentes da membrana nuclear e atópanse na cirrose biliar primaria (tamén chamada colanxite biliar primaria). Cada anticorpo está presente en aproximadamene o 25–30 % dos casos de dita cirrose. Os antíxenos de ambos os anticorpos son constituíntes da membrana nuclear. A gp210 é unha proteína de 200 kDa que intervén na ancoraxe dos compoñentes dos poros nucleares á membrana nuclear. O antíxeno p62 é un complexo do poro de 60 kDa.[42][43]
Anticorpos anticentrómero
editarOs anticorpos anticentrómero están asociados coa esclerose sistémica cutánea limitada, tamén coñecida como síndrome CREST, así como coa cirrose biliar primaria e a esclerodermia.[44] Coñécense seis antíxenos asociados co centrómero; denominados de CENP-A a CENP-F. CENP-A é unha proteína similar a histona H3 de 17 kDa. CENP-B é unha proteína que se une ao ADN de 80 kDa implicada no pregamento da heterocromatina. CENP-C é unha proteína de 140 kDa que intervén na ensamblaxe do cinetocoro. CENP-D é unha proteína de 50 kDa de función descoñecida, pero pode ser homóloga doutra proteína que participa na condensación da cromatina chamada RCC1. CENP-E é unha proteína de 312 kDa da familia da proteína motora quinesina. CENP-F é unha proteína de 367 kDa da matriz nuclear que se asocia co cinetocoro na fase G2 tardía durante a mitose. Os anticorpos para CENP-A, B e C atópanse normalmente (no 16–42 % dos casos de esclerose sistémica) e están asociados co fenómeno de Raynaud, telanxiectasias, afectación pulmonar e comezo temperán da esclerose sistémica.[33][45][46]
Anti-sp100
editarOs anticorpos anti-sp100 atópanse en aproximadamente o 20–30 % dos casos de cirrose biliar primaria. Encóntranse en poucos individuos que non teñan esa doenza, e, polo tanto, son un marcador moi específico da doenza. O antíxeno sp100 atópase nos corpos nucleares, que son grandes complexos proteicos do núcleo celular que poden ter un papel no crecemento e diferenciación celulares.[47]
Anti-PM-Scl
editarOs anticorpos anti-PM-Scl están presentes no 50 % dos casos de síndrome de solapamento de polimiosite/esclerose sistémica (PM/SSc). Arredor do 80 % dos individuos con anticorpos no seu soro sanguíneo presentan esta síndrome. A presenza destes anticorpos está ligada á afectción cutánea limitda da síndrome de solapamento PM/SSc. As dianas antixénicas dos anticorpos son compoñentes do complexo exosoma de procesamento do ARN do nucléolo.[33] Hai dez proteínas nese complexo e atópanse anticorpos contra oito delas con frecuencias diversas; son: PM/Scl-100 (70–80 %), PM/Scl-75 (46–80 %), hRrp4 (50 %), hRrp42 (21 %), hRrp46 (18 %), hCs14 (14 %), hRrp41 (10 %) e hRrp40 (7 %).[48]
Anticorpos anti-DFS70
editarOs anticorpos anti-DFS70 xeran un denso padrón de manchas finas con inmunofluorescencia indirecta e atópanse en individuos normais e en varias condicións médicas, pero non está asociados coa patoloxía autoinmune sistémica. Xa que logo, poden utilizarse para axudar a descartar esas condicións en individuos positivos para ANAs. Un número significativo de pacientes diagnostícanse de lupus eritematoso sistémico ou enfermidade do tecido conectivo indiferenciada bseándose en gran medida nun test de ANAs positivo. En caso de que se poida detectar un autoanticorpo definido (por exemplo, anticorpos anti-ENA), recoméndase facer o test de anticorpos anti-DFS70 para verificar o diagnóstico. Os tests de anticorpos anti-DFS70 están dispoñibles como test marcados con certificado CE[49] para a súa comercialización na Unión Europea. Ata agora non se dispón de ensaios aprobados pola FDA norteamericana.[50]
Test de ANAs
editarA presenza de ANAs no sangue pode ser confirmada por un test de cribado. Aínda que hai moitos tests para a detección de ANAs, os tests máis comúns usados para o cribado son a inmunofluorescencia indirecta e o ensaio inmunosorbente de encima ligado (ELISA).[51] Despois da detección de ANAs, determínanse os diversos subtipos.[8]
Inmunofluorescencia indirecta
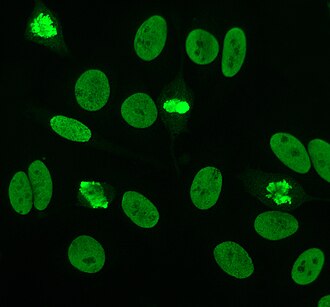
editarA inmunofluorescencia indirecta é un dos tests que se usan máis frecuentemente para detectar ANAs. Utilízanse células HEp-2 como substrato para detectar os anticorpos no soro humano. Cúbrense portaobxectos de microscopia con células HEp-2 e incúbase o soro coas células. Se os anticorpos diana están presentes, entón uniranse aos antíxenos nas células; no caso dos ANAs, os anticorpos únense ao núcleo. Estes poden visualizarse engadindo un anticorpo antihumano con marcaxe fluorescente (xeralmente FITC ou rodopsina B) que se une aos anticorpos. A molécula emitirá fluorescencia cando unha luz de lonxitude de onda específica incide sobre ela, a cal pode verse cun microscopio. Dependendo do anticorpo presente no soro humano e a localización do antíxeno na célula, poderanse ver padróns definidos de fluorescencia nas céllas HEp-2.[52][53] Os niveis de anticorpos analízanse realizando dilucións do soro sanguíneo. Un test de ANAs considérase positivo se a hai fluorescencia visible a unha titulación de 1:40/1:80. As titulacións maiores son máis significativas clinicamente, xa que os positivos baixos (≤1:160) se observan nun 20 % dos individuos sans, especialmente se son vellos. Só arredor dun 5 % da poboación sa ten titulacións de ANAs de 1:160 ou maiores.[8][54]
HEp-2
editarAta aproximadamente o ano 1975, cando se introduciron as células HEp-2, os tecidos animais eran usados como un substrato estándar para a inmunofluorescencia.[11] As células HEp-2 son actualmente un dos substratos máis comúns para a detección de ANAs por inmunofluorescencia.[55]
Esta liña celular, orixinalmente creada a partir dunha cepa de carcinoma larínxeo, quedou contaminada por células HeLa, que acabaron desprazándoa, e agora é identificada como verdadeiras células HeLa.[56]
Son superiores aos tecidos animais usados previamente debido ao seu gran tamaño e a alta taxa de mitoses de dita liña cellar. Isto permite a detección de anticorpos para antíxenos específicos da mitose, como anticorpos para o centrómero. Estas células tamén permiten a identificación de anticorpos anti-Ro, porque se usa a acetona para a fixación das células (outros fixadores poden arrastrar por lavado o antíxeno).[57]
Hai moitos padróns de marcaxe nuclear observados en células HEp-2: homoxénea, a manchas, nucleolar, de membrana nuclear, centromérica, de punto nuclear e pleomórfica. O padrón homoxéneo é o que se observa cando se tinguen os cromosomas condensados e a cromatina interfásica. Este padrón está asociado con anticorpos anti-dsDNA, anticorpos contra compoñentes nucleosómicos, e anticorpos anti-histonas. Hai dous padróns a manchas: fino e groso. O padrón de manchas finas presenta unha tinguidura nuclear fina coa cromatina non tinguida, o cal está asociado con anticorpos anti-Ro e anti-La. O padrón de manchas grosas presenta unha tinguidura granular grosa, causada por anticorpos anti-U1-RNP e anti-Sm. O padrón de tinguidura nucleolar está asociado con moitos anticorpos incluíndo os anticorpos anti-Scl-70, anti-PM-Scl, anti-fibrilarina e anti-Th/To. A marcaxe da membrana nuclear aparece como un anel fluorescente arredor do núcleo da célula producido por anticorpos anti-gp210 e anti-p62. O padrón centromérico mostra puntos nucleares múltiples en interfase e en células mitóticas, correspondendo ao número de cromosomas na célula. Os padróns de punto nuclear mostran entre 13 e 25 puntos no núcleo nas células en interfase e producense por anticorpos anti-sp100. O padrón pleomórfico é causado por anticorpos para o antíxeno nuclear de célula proliferante.[26][54][58][59] A inmunofluorescencia indirecta é lixeiramene superior comparada co ELISA na detección de ANAs en células HEp-2.[55]
Crithidia luciliae
editarCrithidia luciliae é un protista hemoflaxelado unicelular. Utilízase como substrato para a inmunofluorescencia para a detección de anticorpos anti-dsDNA. Estes microorganismos posúen un orgánulo chamado cinetoplasto, que é unha mitocondria grande que contén unha rede de moléculas circulares de dsDNA entrelazadas. Despois da súa incubación con soro que conteña anticorpos anti-dsDNA e anticorpos antihumanos marcados fluorescentemente, o cinetoplasto emite fluorescencia. Debido á falta doutros antixenos nucleares no orgánulo, usar C. luciliae como substrato permite a detección específica de anticorpos anti-dsDNA.[8][60][61]
ELISA
editarO ensaio inmunosorbente de encima ligado (ELISA) utiliza placas de microtitulación cubertas de antíxeno para a detección de ANAs.[62] Cada pozo dunha placa de microtitulación está cuberto ou ben cun só antíxeno ou ben con múltiples antíxenos para detectar anticorpos específicos ou para cribar os ANAs, respectivamente. Os antíxenos poden proceder de extractos celulares ou son recombinantes. Incúbase o soro sanguíneo nos pozos da placa e despois faise un lavado. Se están presentes anticorpos que se unen ao antíxeno entón permanecerán no pozo despois do lavado. Engádese un anticorpo antihumano secundario conxugado a un encima como a peroxidase do ravo picante. A reacción encimática que se produce orixina un cambio de cor na solución que é proporcional á cantidade de anticorpo unido ao antíxeno.[11][53][63] Hai diferenzas significativas entre a detección de ANAs por inmunofluorescencia e por diferentes kits de ELISA, e hai só un acordo marxinal entre eles. Un médico debe estar familiarizado coas diferenzas para avaliar os resultados dos diversos ensaios.[62]
Sensibilidade
editarA seguinte táboa é unha lista das sensibilidades de diferentes tipos de ANAs para diferentes enfermidades.
| Tipo de ANA | Antíxeno diana | Sensibilidade (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Lupus eritematoso sistémico (SLE) | Lupus eritemtoso inducido por fármacos | Esclerose sistémica difusa | Esclerodermia sistémica limitada | Síndrome de Sjögren | Miopatía inflamatoria | Enfermidade mixta do tecido conectivo (MCTD) | ||
| Todos os ANAs (por inmunofluorescencia indirecta) |
Varios | 95[64] | 100[64] | 80[64] | 80[64] | 70[64] | 40–60 | 95[64] |
| Anti-dsDNA | ADN | 60[64] | –[64] | –[64] | –[64] | 30[64] | – | -[64] |
| Anti-Sm | Proteinas centrais das snRNPs | 40[64] | –[64] | –[64] | –[64] | –[64] | – | -[64] |
| Antihistonas | Histonas | 60[64] | 90[64] | –[64] | –[64] | –[64] | – | -[64] |
| Anti Scl-70 | Topoisomerase de tipo I | –[64] | –[64] | 20[64] | 10[64] | –[64] | – | -[64] |
| Anticentrómero | Proteínas centroméricas | –[64] | –[64] | 30[64] | 80[64] | –[64] | – | -[64] |
| SS-A (Ro) | RNPs | 40[64] | –[64] | –[64] | –[64] | 50[64] | 10 | -[64] |
| SS-B (La) | RNPs | 10–15 | – | – | – | 60–90 | – | |
| – = menos do 5 % de sensibilidade | ||||||||
Algúns ANAs aparecen en varios tipos de doenzas, o que ten como resultado unha menor especificidade do test. Por exemplo, o IgM-factor reumatoide (IgM-RF) ten reaccións cruzadas con ANAs dando lugar a falsos positivos na inmunofluorescencia.[65] Test de ANAs positivos xunto con anticorpos anti-dsDNA obsérvanse en pacientes con tiroidite autoinmune.[66][67] Pode haber un resultdo positivo no test de ANAs no 45 % das persoas con condicións tiroides autoinmunes ou artrite reumatoide, e no 15 % das persoas con infección por VIH ou hepatite C.[67][68][69][70] Segundo a Lupus Foundation of America, "aproximadamente o 5 % da poboación xeral terá un ANA positivo. Porén, polo menos o 95 % das persoas que teñen un ANA positivo non teñen lupus. Un test de ANAs positivo pode ás veces darse en familias, incluso se os membros da familia non teñen evidencias de lupus."[10] Por outra parte, afirman que aínda que o 95 % dos pacientes que realmente teñen lupus dan positivo no test de ANAs, "só unha pequena porcentaxe teñen un ANA negativo, e moitos deles teñen outros anticorpos (como anticorpos antifosfolípidos, anti-Ro, anti-SSA) ou os seus ANA pasaron de ser positivos a negativos por causa de esteroides, medicacións citotóxicas ou uremia (insuficiencia renal)."[10]
Historia
editarHargraves et al. descubriron as células LE (célula de lupus eritematoso, un leucocito) na medula ósea en 1948.[71] En 1957 Holborow et al. demostraron por primeira vez a presenza de ANAs usando inmunofluorescencia indirecta.[72] Esta foi a primeira indicación de que procesos que afectan o núcleo celular eran responsables do lupus eritematoso sistémico. En 1959 descubriuse que o soro de individuos con lupus eritematoso sitémico contiña anticorpos que precipitaban con extractos salinos do núcleo, coñecidos como antíxenos nucleares extraíbles (ENAs). Isto levou á caracterización de antíxenos ENA e dos seus anticorpos respectivos. Deste xeito, descubríronse os anticorpos anti-Sm e anti-RNP en 1966 e 1971, respectivamente. Na décsda de 1970 descubríronse os anticorpos anti-Ro/anti-SS-A e anti-La/anti-SS-B. Sóubose que o anticorpo Scl-70 era un anticorpo específico da esclerodermia en 1979; porén, o antíxeno (topoisomerase I) non se caracterizou ata 1986. O antíxeno Jo-1 e o anticorpo caracterizáronse en 1980.[8][20]
Notas
editar- ↑ Al-Mughales JA (2022). "Anti-Nuclear Antibodies Patterns in Patients With Systemic Lupus Erythematosus and Their Correlation With Other Diagnostic Immunological Parameters.". Front Immunol 13: 850759. PMC 8964090. PMID 35359932. doi:10.3389/fimmu.2022.850759.
Pequenas modificacións de Mikael Häggström, MD
- Attribution 4.0 International (CC BY 4.0) license - ↑ "Medical Subject Headings (MeSH)". National Library of Medicine. Consultado o 12 de febreiro de 2013.
- ↑ 3,0 3,1 Reece, Jane; Campbell, Neil (2005). Biology (7ª ed.). San Francisco: Pearson/Benjamin-Cummings. ISBN 978-0805371468.[cómpre nº de páxina]
- ↑ Cervera, R; Font, J; Ramos-Casals, M; García-Carrasco, M; Rosas, J; Morlà, RM; Muñoz, FJ; Artigues, A; Pallarés, L; Ingelmo, M (2000). "Primary Sjögren's syndrome in men: clinical and immunological characteristics". Lupus 9 (1): 61–4. PMID 10713648. doi:10.1177/096120330000900111.
- ↑ Barnett, AJ; McNeilage, LJ (maio de1993). "Antinuclear antibodies in patients with scleroderma (systemic sclerosis) and in their blood relatives and spouses". Annals of the Rheumatic Diseases 52 (5): 365–8. PMC 1005051. PMID 8323384. doi:10.1136/ard.52.5.365.
- ↑ Burdt, Mark A.; Hoffman, Robert W.; Deutscher, Susan L.; Wang, Grace S.; Johnson, Jane C.; Sharp, Gordon C. (1 de maio de 1999). "Long-term outcome in mixed connective tissue disease: Longitudinal clinical and serologic findings". Arthritis & Rheumatism 42 (5): 899–909. PMID 10323445. doi:10.1002/1529-0131(199905)42:5<899::AID-ANR8>3.0.CO;2-L.
- ↑ Obermayer-Straub, P; Strassburg, CP; Manns, MP (2000). "Autoimmune hepatitis". Journal of Hepatology 32 (1 Suppl): 181–97. PMID 10728804. doi:10.1016/S0168-8278(00)80425-0.
- ↑ 8,00 8,01 8,02 8,03 8,04 8,05 8,06 8,07 8,08 8,09 Kavanaugh A, Tomar R, Reveille J, Solomon DH, Homburger HA (xaneiro de 2000). "Guidelines for clinical use of the antinuclear antibody test and tests for specific autoantibodies to nuclear antigens. American College of Pathologists". Archives of Pathology & Laboratory Medicine 124 (1): 71–81. PMID 10629135. doi:10.5858/2000-124-0071-GFCUOT.
- ↑ Tan, EM; Feltkamp, TE; Smolen, JS; Butcher, B; Dawkins, R; Fritzler, MJ; Gordon, T; Hardin, JA; Kalden, JR; Lahita, RG; Maini, RN; McDougal, JS; Rothfield, NF; Smeenk, RJ; Takasaki, Y; Wiik, A; Wilson, MR; Koziol, JA (setembro de 1997). "Range of antinuclear antibodies in "healthy" individuals". Arthritis and Rheumatism 40 (9): 1601–11. PMID 9324014. doi:10.1002/art.1780400909.
- ↑ 10,0 10,1 10,2 "The Antinuclear Antibody Test: What It Means". Lupus Foundation of America. Consultado o 7 de xuño de 2013.[Ligazón morta]
- ↑ 11,0 11,1 11,2 11,3 Kumar, Y; Bhatia, A; Minz, RW (2 de xaneiro de 2009). "Antinuclear antibodies and their detection methods in diagnosis of connective tissue diseases: a journey revisited". Diagnostic Pathology 4: 1. PMC 2628865. PMID 19121207. doi:10.1186/1746-1596-4-1.
- ↑ 12,0 12,1 12,2 12,3 Yamamoto K (xaneiro de 2003). "Pathogenesis of Sjögren's syndrome". Autoimmun Rev 2 (1): 13–8. PMID 12848970. doi:10.1016/S1568-9972(02)00121-0.
- ↑ Richardson, B; Epstein, WV (setembro de 1981). "Utility of the fluorescent antinuclear antibody test in a single patient". Annals of Internal Medicine 95 (3): 333–8. PMID 7023311. doi:10.7326/0003-4819-95-3-333.
- ↑ Malleson PN, Mackinnon MJ, Sailer-Hoeck M, Spencer CH (2010). "Review for the generalist: The antinuclear antibody test in children – When to use it and what to do with a positive titer". Pediatr Rheumatol Online J 8: 27. PMC 2987328. PMID 20961429. doi:10.1186/1546-0096-8-27.
- ↑ 15,0 15,1 Damoiseaux, JG; Tervaert, JW (xaneiro de 2006). "From ANA to ENA: how to proceed?". Autoimmunity Reviews 5 (1): 10–7. PMID 16338206. doi:10.1016/j.autrev.2005.05.007.
- ↑ 16,0 16,1 Wenzel, J; Gerdsen, R; Uerlich, M; Bauer, R; Bieber, T; Boehm, I (decembro de 2001). "Antibodies targeting extractable nuclear antigens: historical development and current knowledge". The British Journal of Dermatology 145 (6): 859–67. PMID 11899137. doi:10.1046/j.1365-2133.2001.04577.x.
- ↑ 17,0 17,1 Hernández-Molina, G; Leal-Alegre, G; Michel-Peregrina, M (xaneiro de 2011). "The meaning of anti-Ro and anti-La antibodies in primary Sjögren's syndrome". Autoimmunity Reviews 10 (3): 123–5. PMID 20833272. doi:10.1016/j.autrev.2010.09.001.
- ↑ Kassan, SS; Moutsopoulos, HM (xuño de 2004). "Clinical manifestations and early diagnosis of Sjögren syndrome". Arch Intern Med 164 (12): 1275–84. PMID 15226160. doi:10.1001/archinte.164.12.1275.
- ↑ Defendenti, C; Atzeni, F; Spina, MF; Grosso, S; Cereda, A; Guercilena, G; Bollani, S; Saibeni, S; Puttini, PS (xaneiro de 2011). "Clinical and laboratory aspects of Ro/SSA-52 autoantibodies". Autoimmunity Reviews 10 (3): 150–4. PMID 20854935. doi:10.1016/j.autrev.2010.09.005.
- ↑ 20,0 20,1 20,2 Venables, PJ (xuño de 2004). "Sjögren's syndrome". Best Practice & Research. Clinical Rheumatology 18 (3): 313–29. PMID 15158743. doi:10.1016/j.berh.2004.02.010.
- ↑ Clowse, Megan E. B.; Eudy, Amanda M.; Kiernan, Elizabeth; Williams, Matthew R.; Bermas, Bonnie; Chakravarty, Eliza; Sammaritano, Lisa R.; Chambers, Christina D.; Buyon, Jill (1 de xullo de 2018). "The prevention, screening and treatment of congenital heart block from neonatal lupus: a survey of provider practices". Rheumatology 57 (suppl_5): v9–v17. ISSN 1462-0332. PMC 6099126. PMID 30137589. doi:10.1093/rheumatology/key141.
- ↑ Sonesson, Sven-Erik; Hedlund, Malin; Ambrosi, Aurélie; Wahren-Herlenius, Marie (1 de outubro de 2017). "Factors influencing fetal cardiac conduction in anti-Ro/SSA-positive pregnancies". Rheumatology 56 (10): 1755–1762. ISSN 1462-0332. PMID 28957562. doi:10.1093/rheumatology/kex263.
- ↑ Scofield, RH (8 de maio de 2004). "Autoantibodies as predictors of disease". Lancet 363 (9420): 1544–6. PMID 15135604. doi:10.1016/S0140-6736(04)16154-0.
- ↑ Deshmukh, US; Bagavant, H; Lewis, J; Gaskin, F; Fu, SM (novembro de 2005). "Epitope spreading within lupus-associated ribonucleoprotein antigens". Clinical Immunology (Orlando, Fla.) 117 (2): 112–20. PMID 16095971. doi:10.1016/j.clim.2005.07.002.
- ↑ Ben-Chetrit, E (maio de 1993). "The molecular basis of the SSA/Ro antigens and the clinical significance of their autoantibodies". British Journal of Rheumatology 32 (5): 396–402. PMID 8495261. doi:10.1093/rheumatology/32.5.396.
- ↑ 26,0 26,1 26,2 26,3 von Mühlen, CA; Tan, EM (abril de 1995). "Autoantibodies in the diagnosis of systemic rheumatic diseases". Seminars in Arthritis and Rheumatism 24 (5): 323–58. PMID 7604300. doi:10.1016/S0049-0172(95)80004-2.
- ↑ Lyons, R; Narain, S; Nichols, C; Satoh, M; Reeves, WH (xuño de 2005). "Effective use of autoantibody tests in the diagnosis of systemic autoimmune disease". Annals of the New York Academy of Sciences 1050 (1): 217–28. Bibcode:2005NYASA1050..217L. PMID 16014537. doi:10.1196/annals.1313.023.
- ↑ Zieve, GW; Khusial, PR (setembro de 2003). "The anti-Sm immune response in autoimmunity and cell biology". Autoimmunity Reviews 2 (5): 235–40. PMID 12965173. doi:10.1016/S1568-9972(03)00018-1.
- ↑ Migliorini, P; Baldini, C; Rocchi, V; Bombardieri, S (febreiro de 2005). "Anti-Sm and anti-RNP antibodies". Autoimmunity 38 (1): 47–54. PMID 15804705. doi:10.1080/08916930400022715.
- ↑ Benito-Garcia, E; Schur, PH; Lahita, R; American College of Rheumatology Ad Hoc Committee on Immunologic Testing, Guidelines (15 de decembro de 2004). "Guidelines for immunologic laboratory testing in the rheumatic diseases: anti-Sm and anti-RNP antibody tests". Arthritis and Rheumatism 51 (6): 1030–44. PMID 15593352. doi:10.1002/art.20836.
- ↑ Venables PJ (2006). "Mixed connective tissue disease". Lupus 15 (3): 132–7. PMID 16634365. doi:10.1191/0961203306lu2283rr.
- ↑ Jimenez, SA; Derk, CT (6 de xaneiro de 2004). "Following the molecular pathways toward an understanding of the pathogenesis of systemic sclerosis". Annals of Internal Medicine 140 (1): 37–50. PMID 14706971. doi:10.7326/0003-4819-140-2-200401200-00013.
- ↑ 33,0 33,1 33,2 Ho, KT; Reveille, JD (2003). "The clinical relevance of autoantibodies in scleroderma". Arthritis Research & Therapy 5 (2): 80–93. PMC 165038. PMID 12718748. doi:10.1186/ar628.
- ↑ Mahler M, Silverman ED, Schulte-Pelkum J, Fritzler MJ (setembro de 2010). "Anti-Scl-70 (topo-I) antibodies in SLE: Myth or reality?". Autoimmun Rev 9 (11): 756–60. PMID 20601198. doi:10.1016/j.autrev.2010.06.005.
- ↑ Guldner, HH; Szostecki, C; Vosberg, HP; Lakomek, HJ; Penner, E; Bautz, FA (1986). "Scl 70 autoantibodies from scleroderma patients recognize a 95 kDa protein identified as DNA topoisomerase I". Chromosoma 94 (2): 132–8. PMID 2428564. doi:10.1007/BF00286991.
- ↑ Schmidt, WA; Wetzel, W; Friedländer, R; Lange, R; Sörensen, HF; Lichey, HJ; Genth, E; Mierau, R; Gromnica-Ihle, E (2000). "Clinical and serological aspects of patients with anti-Jo-1 antibodies—an evolving spectrum of disease manifestations". Clinical Rheumatology 19 (5): 371–7. PMID 11055826. doi:10.1007/s100670070030.
- ↑ Weinstein, A; Bordwell, B; Stone, B; Tibbetts, C; Rothfield, NF (febreiro de 1983). "Antibodies to native DNA and serum complement (C3) levels. Application to diagnosis and classification of systemic lupus erythematosus". The American Journal of Medicine 74 (2): 206–16. PMID 6600582. doi:10.1016/0002-9343(83)90613-7.
- ↑ Mok, CC; Lau, CS (xullo de 2003). "Pathogenesis of systemic lupus erythematosus". Journal of Clinical Pathology 56 (7): 481–90. PMC 1769989. PMID 12835292. doi:10.1136/jcp.56.7.481.
- ↑ Yung, S; Chan, TM (febreiro de 2008). "Anti-DNA antibodies in the pathogenesis of lupus nephritis—the emerging mechanisms". Autoimmunity Reviews 7 (4): 317–21. PMID 18295737. doi:10.1016/j.autrev.2007.12.001.
- ↑ Vasoo, S (2006). "Drug-induced lupus: an update". Lupus 15 (11): 757–61. PMID 17153847. doi:10.1177/0961203306070000.
- ↑ Katz, U; Zandman-Goddard, G (novembro de 2010). "Drug-induced lupus: an update". Autoimmunity Reviews 10 (1): 46–50. PMID 20656071. doi:10.1016/j.autrev.2010.07.005.
- ↑ Hu, T; Guan, T; Gerace, L (agosto de 1996). "Molecular and functional characterization of the p62 complex, an assembly of nuclear pore complex glycoproteins". The Journal of Cell Biology 134 (3): 589–601. PMC 2120945. PMID 8707840. doi:10.1083/jcb.134.3.589.
- ↑ Mackay, IR; Whittingham, S; Fida, S; Myers, M; Ikuno, N; Gershwin, ME; Rowley, MJ (abril de 2000). "The peculiar autoimmunity of primary biliary cirrhosis". Immunological Reviews 174: 226–37. PMID 10807519. doi:10.1034/j.1600-0528.2002.017410.x.
- ↑ Kallenberg, CG (marzo de 1990). "Anti-centromere antibodies (ACA)". Clinical Rheumatology 9 (1 Suppl 1): 136–9. PMID 2203592. doi:10.1007/BF02205562.
- ↑ Rattner, JB; Mack, GJ; Fritzler, MJ (xullo de 1998). "Autoantibodies to components of the mitotic apparatus". Molecular Biology Reports 25 (3): 143–55. PMID 9700050. doi:10.1023/A:1016523013819.
- ↑ Renz, Harald (2012). Autoimmune diagnostics. Berlin: De Gruyter. ISBN 978-3-11-022864-9.
- ↑ Worman, HJ; Courvalin, JC (xuño de 2003). "Antinuclear antibodies specific for primary biliary cirrhosis". Autoimmunity Reviews 2 (4): 211–7. PMID 12848948. doi:10.1016/S1568-9972(03)00013-2.
- ↑ Mahler, M; Raijmakers, R (agosto de 2007). "Novel aspects of autoantibodies to the PM/Scl complex: clinical, genetic and diagnostic insights". Autoimmunity Reviews 6 (7): 432–7. PMID 17643929. doi:10.1016/j.autrev.2007.01.013.
- ↑ Comunidade Europea CE marking
- ↑ Mahler, Michael; Meroni, Pier Luigi; Andrade, Luis E.; Khamashta, Munther; Bizzaro, Nicola; Casiano, Carlos A.; Fritzler, Marvin J. (2016). "Towards a better understanding of the clinical association of anti-DFS70 autoantibodies". Autoimmunity Reviews 15 (2): 198–201. PMID 26588998. doi:10.1016/j.autrev.2015.11.006.
- ↑ Granito A, Muratori P, Quarneti C, Pappas G, Cicola R, Muratori L (xaneiro de 2012). "Antinuclear antibodies as ancillary markers in primary biliary cirrhosis". Expert Review of Molecular Diagnostics 12 (1): 65–74. PMID 22133120. doi:10.1586/erm.11.82.
- ↑ Klein, Wulf B. Storch. Transl. by R. A. (2000). Immunofluorescence in clinical immunology : a primer and atlas. Basel [u.a.]: Birkhäuser. ISBN 978-3764361822.
- ↑ 53,0 53,1 González-Buitrago, JM; González, C (marzo de 2006). "Present and future of the autoimmunity laboratory". Clinica Chimica Acta; International Journal of Clinical Chemistry 365 (1–2): 50–7. PMID 16126186. doi:10.1016/j.cca.2005.07.023.
- ↑ 54,0 54,1 Tozzoli R, Bizzaro N, Tonutti E, Villalta D, Bassetti D, Manoni F, Piazza A, Pradella M, Rizzotti P (febreiro de 2002). Italian Society of Laboratory Medicine Study Group on the Diagnosis of Autoimmune Diseases. "Guidelines for the laboratory use of autoantibody tests in the diagnosis and monitoring of autoimmune rheumatic diseases". American Journal of Clinical Pathology 117 (2): 316–24. PMID 11863229. doi:10.1309/Y5VF-C3DM-L8XV-U053.
- ↑ 55,0 55,1 Ulvestad, E (marzo de 2001). "Performance characteristics and clinical utility of a hybrid ELISA for detection of ANA". APMIS 109 (3): 217–22. PMID 11430499. doi:10.1034/j.1600-0463.2001.090305.x.
- ↑ Lacroix M (xaneiro de 2008). "Persistent use of "false" cell lines". Int. J. Cancer 122 (1): 1–4. PMID 17960586. doi:10.1002/ijc.23233.
- ↑ Keren, DF (xuño de 2002). "Antinuclear antibody testing". Clinics in Laboratory Medicine 22 (2): 447–74. PMID 12134471. doi:10.1016/S0272-2712(01)00012-9.
- ↑ Nesher, G; Margalit, R; Ashkenazi, YJ (abril de 2001). "Anti-nuclear envelope antibodies: Clinical associations". Seminars in Arthritis and Rheumatism 30 (5): 313–20. PMID 11303304. doi:10.1053/sarh.2001.20266.
- ↑ Sack, U; Conrad, K; Csernok, E; Frank, I; Hiepe, F; Krieger, T; Kromminga, A; Landenberg, Pv; Messer, G; Witte, T; Mierau, R (xuño de 2009). die deutsche EASI-Gruppe (European Autoimmunity Standardization, Initiative). "Autoantibody detection by indirect immunofluorescence on HEp-2 cells" (PDF). Deutsche Medizinische Wochenschrift 134 (24): 1278–82. PMID 19499499. doi:10.1055/s-0029-1225278.
- ↑ Slater, NG; Cameron, JS; Lessof, MH (setembro de 1976). "The Crithidia luciliae kinetoplast immunofluorescence test in systemic lupus erythematosus". Clinical and Experimental Immunology 25 (3): 480–6. PMC 1541410. PMID 786521.
- ↑ Shapiro, TA; Englund, PT (1995). "The structure and replication of kinetoplast DNA". Annual Review of Microbiology 49: 117–43. PMID 8561456. doi:10.1146/annurev.mi.49.100195.001001.
- ↑ 62,0 62,1 Emlen, W; O'Neill, L (setembro de 1997). "Clinical significance of antinuclear antibodies: comparison of detection with immunofluorescence and enzyme-linked immunosorbent assays". Arthritis and Rheumatism 40 (9): 1612–8. PMID 9324015. doi:10.1002/art.1780400910.
- ↑ Deshpande, S. S. (1996). Enzyme immunoassays: from concept to product development. Londres: Chapman & Hall. ISBN 978-0-412-05601-7.
- ↑ 64,00 64,01 64,02 64,03 64,04 64,05 64,06 64,07 64,08 64,09 64,10 64,11 64,12 64,13 64,14 64,15 64,16 64,17 64,18 64,19 64,20 64,21 64,22 64,23 64,24 64,25 64,26 64,27 64,28 64,29 64,30 64,31 64,32 64,33 64,34 64,35 64,36 64,37 64,38 64,39 64,40 64,41 Table 6-2 in: Elizabeth D Agabegi; Agabegi, Steven S. (2008). Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 978-0-7817-7153-5.
- ↑ Frokjaer, Vibe G.; Mortensen, Erik L.; Nielsen, Finn Å.; Haugbol, Steven; Pinborg, Lars H.; Adams, Karen H.; Svarer, Claus; Hasselbalch, Steen G.; Holm, Soeren; Paulson, Olaf B.; Knudsen, Gitte M. (29 de febreiro de 2008). "Frontolimbic Serotonin 2A Receptor Binding in Healthy Subjects Is Associated with Personality Risk Factors for Affective Disorder". Biological Psychiatry 63 (6): 569–576. PMID 17884017. doi:10.1016/j.biopsych.2007.07.009.
- ↑ Tektonidou, M G; Anapliotou, M; Vlachoyiannopoulos, P; Moutsopoulos, HM (1 de setembro de 2004). "Presence of systemic autoimmune disorders in patients with autoimmune thyroid diseases". Annals of the Rheumatic Diseases 63 (9): 1159–1161. PMC 1755126. PMID 15308528. doi:10.1136/ard.2004.022624.
- ↑ 67,0 67,1 Petri, M; Karlson, EW; Cooper, DS; Ladenson, PW (outubro de 1991). "Autoantibody tests in autoimmune thyroid disease: a case-control study". The Journal of Rheumatology 18 (10): 1529–31. PMID 1765977.
- ↑ Charles, P. J.; Smeenk, R. J. T.; De Jong, J.; Feldmann, M.; Maini, R. N. (1 de novembro de 2000). "Assessment of antibodies to double-stranded DNA induced in rheumatoid arthritis patients following treatment with infliximab, a monoclonal antibody to tumor necrosis factor α: Findings in open-label and randomized placebo-controlled trials". Arthritis & Rheumatism 43 (11): 2383–2390. PMID 11083258. doi:10.1002/1529-0131(200011)43:11<2383::AID-ANR2>3.0.CO;2-D.
- ↑ Cassani, F; Cataleta, M; Valentini, P; Muratori, P; Giostra, F; Francesconi, R; Muratori, L; Lenzi, M; Bianchi, G; Zauli, D; Bianchi, F B (1 de setembro de 1997). "Serum autoantibodies in chronic hepatitis C: Comparison with autoimmune hepatitis and impact on the disease profile". Hepatology 26 (3): 561–566. PMID 9303483. doi:10.1002/hep.510260305.
- ↑ Medina-Rodriguez, F; Guzman, C; Jara, LJ; Hermida, C; Alboukrek, D; Cervera, H; Miranda, JM; Fraga, A (novembro de 1993). "Rheumatic manifestations in human immunodeficiency virus positive and negative individuals: a study of 2 populations with similar risk factors". The Journal of Rheumatology 20 (11): 1880–4. PMID 8308773.
- ↑ Hargraves M, Richmond H, Morton R. Presentation of two bone marrow components, the tart cell and the LE cell. Mayo Clin Proc 1948;27:25–28.
- ↑ Holborow, E. J.; Weir, D. M.; Johnson, G. D. (28 de setembro de 1957). "A Serum Factor in Lupus Erythematosus with Affinity for Tissue Nuclei". BMJ 2 (5047): 732–734. PMC 1962253. PMID 13460368. doi:10.1136/bmj.2.5047.732.
Véxase tamén
editarOutros artigos
editarLigazóns externas
editar- Autoimmunityblog – HEp-2 ANA
- Antinuclear antibodies Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- Greidinger, Eric L.; Hoffman, DO; Robert W. (31 de xaneiro de 2003). "CE update [chemistry | immunology]: Antinuclear Antibody Testing: Methods, Indications, and Interpretation". Laboratory Medicine 34 (2): 113–117. doi:10.1309/VUB90VTPMEWV3W0F.