SDS-PAGE
A SDS-PAGE (do inglés sodium dodecyl sulfate–polyacrylamide gel electrophoresis ou electroforese en xel de poliacrilamida con dodecil sulfato sódico) é unha das variantes da electroforese en xel de poliacrilamida, un método analítico usado en bioquímica para a separación de moléculas cargadas en mesturas pola súa masa molecular nun campo eléctrico. Utiliza o dodecil sulfato sódico (SDS) para axudar a identificar e illar moléculas de proteínas.
A SDS-PAGE é un sistema electroforético descontinuo desenvolvido por Ulrich K. Laemmli, que se utiliza habitualmente como método para separar proteínas de masas moleculares entre 5 e 250 KDa.[1] A publicación que a describe é o artigo máis frecuentemente citado dun só autor e o segundo máis citado globalmente.[2]
Propiedades
editarA SDS-PAGE é un método electroforético co que se poden separar proteínas pola súa masa. O medio (ou matriz) no que se realiza é un xel descontinuo baseado na poliacrilamida. Ademais úsase o surfactante SDS (dodecil sulfato sódico). A cada gramo de proteína únense uns 1,4 gramos de SDS,[3][4][5] o que corresponde a unha molécula de SDS por cada dous aminoácidos da proteína. O SDS actúa como un surfactante, que cobre as proteínas dándolles unha proporción moi similar de carga-masa. As cargas intrínsecas que tiñan as proteínas son desprezables en comparación coas que ten o SDS que as cobre, e as cargas positivas son tamén reducidas no rango de pH básico dun xel separador. Coa aplicación dun campo eléctrico constante, as proteínas migran cara ao ánodo, cada unha cunha diferente mobilidade, dependendo da súa masa. Este procedemento simple permite a separación precisa das proteínas pola masa sen que inflúan as cargas intrínsecas orixinais da proteína.
O SDS tende a formar micelas esféricas en solucións acuosas por riba de certa concentración chamadas concentración micelar crítica (CMC). Por riba dunha concentración micelar crítica de 7 a 10 milimolar en solucións acuosas, o SDS aparece como moléculas separadas (monómero) e como micelas, pero por debaixo da CMC o SDS parece só como monómero en solucións acuosas. Á CMC, unha micela consta dunhas 62 moléculas de SDS.[6] Porén, só os monómeros de SDS se unen a proteínas e fano por medio de interaccións hidrófobas, mentres que as micelas de SDS son aniónicas na parte exterior e non se adsorben a ningunha proteína.[3] O SDS é de natureza anfipática, o que permite que se despreguen tanto os segmentos polares coma non polares da estrutura das proteínas.[7] A concentracións de SDS superiores a 0,1 milimolar, empeza o despregamento das proteínas,[3] e por riba de 1 mM, a maioría das proteínas son desnaturalizadas.[3] Debido ao forte efecto desnaturalizador do SDS e a disociación subseguinte dos complexos proteicos, xeralmente non poden determinarse as estruturas cuaternarias usando SDS. Son excepcións, por exemplo, as proteínas que foron previamente estabilizadas por enlaces cruzados covalentes e os complexos proteicos resistentes ao SDS, que son estables mesmo en presenza de SDS (isto último só a temperatura dunha habitación). Para desnaturalizar os complexos resistentes ao SDS cómpre unha alta enerxía de activación, que se consegue quentando. A resistencia ao SDS está baseada na metaestabilidade do pregamento das proteínas. Aínda que a proteína nativa completamente pregada resistente ao SDS non ten suficiente estabilidade en presenza de SDS, o equilibrio químico da desnaturalización a temperatura dunha habitación ocorre lentamente. Os complexos de proteínas estables caracterízanse non só pola resistencia ao SDS senón tamén pola estabilidade contra as proteases e un incremento da vida media biolóxica.[8]
Alternativamente, a electroforese en xel de poliacrilamida pode realizarse tamén cos surfactantes catiónicos CTAB nunha CTAB-PAGE,[9][10][11] ou o 16-BAC nunha BAC-PAGE.[12]
Procedemento
editarO método SDS-PAGE comprende as seguintes etapas: preparación do xel, preparación da mostra, electroforese, tinguidura das proteínas ou western blotting e análise do padrón de bandas xerado.
Produción do xel
editarCando se usan diferentes tampóns no xel (xel de electroforese descontinuo), os xeles prepáranse un día antes de realizar a electroforese, para que a difusión non orixine unha mestura dos tampóns. O xel prodúcese por polimerización de radicais nun molde que consiste en dúas placas de vidro seladas con espazadores entre as placas de vidro. Nun típico molde de minixel, os espazadores teñen un grosor de 0,75 mm ou 1,5 mm, o cal determina a capacidade de carga do xel. Para verter a solución do xel, as placas son xeralmente suxeitadas cunha abrazadeira que sela temporalmente a parte inferior das placas de vidro (que doutro modo estarían abertas) cos dous espazadores. Para facer a solucion do xel mestúrase a acrilamida como formador do xel (usualmente ao 4% V/V no xel de concentración ou stacking e ao 10-12 % no xel separador), a metilenobisacrilamida como axente formador de enlaces cruzados, o tampón do xel separador ou de concentración, a auga e o SDS. Ao engadir o catalizador TEMED e o iniciador de radicais persulfato amónico empeza a polimerización. A solución é despois vertida entre as placas de cristal sen crear burbullas. Dependendo da cantidade de catalizador e iniciador de radicais e dependendo da temperatura, a polimerización dura entre un cuarto de hora e varias horas. O xel inferior (xel separador) vértese primeiro e cóbrese cunhas poucas pingas dun alcohol escasamente hidrosoluble (xeralmente tampón de butanol saturado ou isopropanol), que elimina as burbullas do menisco e protexe a solución do xel do oxíxeno eliminador de radicais. Despois da polimerización do xel separador, o alcohol desbótase e o alcohol residual é eliminado con papel de filtro. Despois da adición do persulfato amónico e o TEMED á solución do xel de concentración (stacking gel), vértese sobre o xel de separación solidificado. Despois, insírese un peite de mostra adecuado entre as placas de cristal sen crear burbullas. O peite de mostras extráese coidadosamente despois da polimerización, deixando petos ou pozos formados para a aplicación da mostra. Para o uso posterior de proteínas para secuenciación de proteínas, os xeles prepáranse a miúdo o día anterior antes da electroforese para reducir as reaccións da acrilamida non polimerizada coas cisteínas nas proteínas.
Usando un mesturador de gradiente, pódense preparar xeles de gradiente cun gradiente de acrilamida (xeralmente do 4 ao 12%), que teñen un rango de separación maior das masas moleculares.[13] Os sistemas de xeles comerciais (denominados xeles pre-moldeado) xeralemnte usan o tampón Bis-tris metano cun valor de pH entre 6,4 e 7,2 tanto no xel de concentración coma no separador.[14][15] Estes xeles entréganse moldeados e listos para usar. Como usan un só tampón (electroforese en xel continua) e teñen un pH case neutro, poden ser almacenados durante varias semanas. O pH máis neutro ralentiza a hidrólise e así a descomposición da poliacrilamida. Ademais, na proteína hai poucas cisteínas que foran modificadas pola acrilamida.[14] Debido ao pH constante nos xeles colector e separador non hai efecto de amontoamento (stacking). As proteínas de xeles BisTris non se poden tinguir con complexos de rutenio.[16] Este sistema de xel ten un rango de separación comparativamente grande, que pode variarse usando MES ou MOPS no tampón para correr o xel.[14]
Preparación da mostra
editarDurante a preparación das mostras, o tampón da mostra, e con el o SDS, engádense en exceso con respecto ás proteínas, e a mostra é despois quentada a 95 °C durante cinco minutos, ou alternativamente a 70 °C durante dez minutos. O quentamento altera as estruturas secundaria e terciaria das proteínas ao distorsionar os enlaces de hidróxeno e estirar as moléculas. Opcionalmente, as pontes disulfuro poden ser clivadas por redución. Para este propósito, engádense ao tampón da mostra tiois redutores como o β-mercaptoetanol (β-ME, 5% por volume), ditiotreitol (DTT, 10 milimolar) ou ditioeritritol (DTE, 10 milimolar). Despois de arrefrialo ata a temperatura dunha habitación, cada mostra é pipeteada no seu propio pozo no xel, que foi previamente mergullado no tampón electroforético no aparello de electroforese.
Ademais das mostras, xeralmente cárgase no xel un marcador de tamaño de peso molecular. Este consta de proteínas de tamaños coñecidos e así permite a estimación (cun erro de ± 10%) do tamaño das proteínas nas mostras reais, o cal migra en paralelo en diferentes carreiros do xel.[17] O marcador de tamaño adoita pipetearse no primeiro ou no último dos petos ou pozos do xel.
Electroforese
editarPara a separación, as mostras desnaturalizadas cárganse nun xel de poliacrilamida, que se sitúa nun tampón electroforético con electrólitos adecuados. Despois aplícase unha voltaxe (xeralmente duns 100 V, 10-20 V por cm de lonxitude do xel), que causa a migrción das moléculas cargadas negativamente a través do xel na dirfección do ánodo cargado positivamente. O xel actúa como un baruto. As pequenas proteínas migran de forma relativamente doada a través da rede do xel, mentres que as proteínas mais grandes é máis probable que queden retidas e migren máis lentamente polo xel, o que permite que as proteínas sexan separadas por tamaño molecular. A electroforese tarda entre media hora e varias horas dependendo da voltaxe e a lonxitude do xel usado.
As proteínas que migran máis rápido (cun peso molecular de menos de 5 KDa) forman a fronte do tampón xunto cos compoñentes aniónicos do tampón electroforético, que tamén migra a través do xel. A área da fronte do tampón faise visible ao engadir ao tampón da mostra a tinguidura aniónica comparativamente pequena azul de bromofenol. Debido ao tamaño molecular relativamente pequeno do azul de bromofenol, este migra máis rápido que as proteínas. Facendo un control óptico da banda coloreada migrante, pode pararse a electroforese antes de que a tinguidura e tamén as mostras migren completamente a través do xel e saian del.
O método máis comunmente usado é a SDS-PAGE descontinua. Neste método, as proteínas migran primeiro no xel colector (de concentración ou stacking gel) con pH neutro, no cal son concentrados e despois migran no xel separador con pH básico, no cal ten lugar a separación real. Os xeles de concentración e o separador difiren no tamaño do poro (4-6 % T e 10-20 % T), forza iónica e valor do pH (pH 6,8 ou 8,8). O electrólito máis frecuentemente usado é o sistema tampón Tris-glicina-cloruro que contén SDS. A pH neutro a glicina forma predominantemente un zwitterión, a pH alto as glicinas perden cargas positivas e fanse predominantemente aniónicas. No xel colector, os ións cloruro cargados negativamente e máis pequenos migran por diante das proteínas (como ións que van en cabeza) e os ións glicinato cargados negativamente e en parte positivamente, que son lixeiramente máis grandes, migran por detrás das proteínas (como ións de cola iniciais), mentres que no comparativamente básico xel separador ambos os ións migran por diante das proteínas. O gradiente de pH entre os tampóns dos xeles de concentración e separador crea un efecto de amontoamento no bordo entre o xel de concentración e o xel de separación, xa que o glicinato perde parcialmente as súas cargas positivas a medida que se incrementa o pH e despois, a medida que o anterior ión de cola adianta as proteínas, convértese no ión que vai en cabeza, o que causa que as bandas das diferentes proteínas (visibles despois de tinguir) se fagan máis estreitas e nítidas (o que se chama efecto de amontoamento ou stacking). Para a separación de proteínas e péptidos máis pequenos, utilízase o sistema tampón TRIS-Tricina de Schägger e von Jagow debido ao maior espallamento das proteínas no rango de 0,5 a 50 KDa.[18]
Tinguidura do xel
editarAo final da separación electroforética, todas as proteínas son clasificadas por tamaño e poden despois ser analizadas por outros métodos, por exemplo a tinguidura de proteínas con azul Coomassie (o máis común e doado de utilizar),[19][20] a tinguidura de prata (o de maior sensibilidade),[21][22][23][24][25][26] tinguidura Stains-all, tinguidura Amido Black 10B,[20] tinguidura Fast green FCF,[20] tinguiduras fluorescentes como a tinguidura con epicocconona[27] e a tinguidura laranxa SYPRO,[28] e a detección inmunolóxica como o western blot.[29][30] As tinguiduras fluorescentes teñen unha linearidde comparativamente máis alta entre a cantidade de proteínas e a intensidade de cor de aproximadamente unhas tres ordes de magnitude por riba do límite de detección, é dicir, a cantidade de proteína pode ser estimada pola intensidade de cor. Cando se usa a tinguidura de proteínas fluorescente tricloroetanol, omítese facer seguidamente outra tinguidura se este foi engadido á solución do xel e o xel foi irradiado con luz UV despois da electroforese.[31][32]
Análise
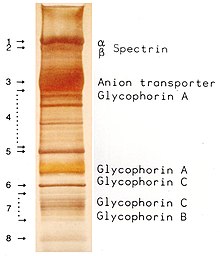
editarA tinguidura de proteínas no xel crea un padrón de bandas documentable das varias proteínas. As glicoproteínas teñen niveis diferenciais de glicosilacións e adsorben SDS máis desigualmente nos puntos de glicosilacións, o que ten como resultado a formación de bandas máis anchas e difuminadas.[33] As proteínas de membrana, a causa do seu dominio transmembrana, están a miúdo compostas de aminoácidos máis hidrófobos, teñen unha menor solubilidade en solucións acuosas, tenden a unirse a lípidos, e adoitan precipitar en solucións acuosas debido a efectos hidrófobos cando non están presentes cantidades suficientes de deterxente. Esta precipitación maniféstase no caso das proteínas de membrana nunha SDS-PAGE ao "formar colas" nos bordos ("tailing") da banda da proteína transmembrana. Neste caso, pode usarse máis cantidade de SDS (usando máis ou usando un tampón da mostra máis concentrado) e a cantidade de proteína na aplicación da mostra pode ser reducida. Unha sobrecarga do xel cunha proteína soluble crea unha banda semicircular desta proteína (por exemplo, no carreiro do marcador nos 66 KDa), o que permite que outras proteínas con pesos moleculares similares queden cubertas. Un baixo contraste (como no carreiro do marcador da imaxe) entre bandas dun carreiro indican a presenza de moitas proteínas (baixa pureza) ou, se se usan proteínas purificadas e aparece un contraste escaso só por debaixo dunha banda, iso indica unha degradación proteolítica da proteína, que primeiro causa bandas de degradación, e despois unha degradación aínda maior produce unha cor homoxénea ("untado") baixo a banda.[34] A documentación do padrón de bandas faise xeralmente fotografándoas ou escaneándoas. Para unha recuperación posterior das moléculas en bandas individuais, pode realizarse un xel de extracción.
Arquivación
editarDespois da tinguidura das proteínas e a documentación do padrón de bandas, o xel de poliacrilamida pode secarse para o seu almacenemento nun arquivo. Poden extraerse del as proteínas en datas posteriores. O xel pode situarse nun armazón para o secado (usando ou non calor) ou nun secador de baleiro. O armazón para o secado consta de dúas partes, unha que serve como unha base para unha pelíucula de celofán húmido ao cal se engaden o xel e unha solución de glicerol ao 1%. Despois aplícase unha segunda película de celofán sen formar burbullas, a segunda parte do armazón ponse enriba e sélase o armazón con clips. A eliminación das burbullas de aire evita a fragmentación do xel durante o secado. A auga evapórase a través da película do celofán. En contraste co armazón de secado, os armazóns de baleiro xeran un baleiro e quentan o xel a uns 50 °C.
Determinación da masa molecular
editarPara unha determinación precisa dos pesos moleculares, as distancias de migración relativas das bandas de cada proteína mídense no xel separdor.[35][36] As medidas son realizadas xeralmene por triplicado para aumentr a exactitude. A mobilidade relativa (chamada valor Rf ou valor Rm) é o cociente da distancia da banda da proteína e a distancia da fronte do tampón. As distancias das bandas e a fronte do tampón mñidense todas desde o principio do xel separador. A distancia da fronte do tampón corresponde grosso modo á distancia á que chega o azul de bromofenol contido no tampón da mostra. As distancias relativas das proteínas do marcador de tamaño son representadas semilogaritmicamente con respecto aos seus pesos moleculares coñecidos. Por comparación coa parte liñal do gráfico xerado por unha análise de regresión, o peso molecular dunha proteína descoñecida pode determinarse pola súa mobilidade relativa. As bandas de proteínas con glicosilacións poden estar difuminadas.[33] As proteínas con moitos aminoácidos básicos (por exemplol, as histonas)[37] poden causar unha sobreestimación dos pesos moleculares ou mesmo non migran no xel en absoluto, porque se moven lentamente na electroforese debido ás cargas positivas ou incluso na dirección oposta. En consecuencia, moitos aminoácidos ácidos poden causar unha migración acelerada dunha proteína e unha subestimación da súa masa molecular.[38]
Aplicacións
editarA SDS-PAGE en combinación cunha tinguidura de protreínas utilízase amplamente en bioquímica para unha separación exacta e rápida e a posterior análise das proteínas. Ten un custo comparativamente baixo en instrumentos e reactivos e é un método doado de usar. Debido á súa baixa escalabilidade, é usada principalmente para propósitos analíticos e en menor medida para propósitos preparativos, especialmente cando hai que illar grandes cantidades dunha proteína.
Ademais, a SDS-PAGE utilízase co western blot para a determinación da presenza dunha proteína específica nunha mestura de proteínas ou para a análise de modificacións postraducionais. As modificacións postraducionais de proteínas poden orixinar unha mobilidade relativa diferente (é dicir, un corremento da banda) ou un cambio na unión dun anticorpo de detección usado no western blot (é dicir, unha banda desaparece e aparece).
Na espectroscopia de masas de proteínas, a SDS-PAGE é un método amplamente usado para a preparción de mostras antes da espectrometría, principalmente usando dixestión en xel. En canto á determinación da masa molecular dunha proteína, a SDS-PAGE é un pouco máis exacta que unha ultracentrifugación analítica, pero menos exacta que unha espectroscopia de masas (ignorando as modificacións postraducionais) ou un cálculo da masa molecular da proteína a partir da secuencia de ADN.
En diagnósticos médicos, a SDS-PAGE utilízase como parte dun test de VIH e para avaliar a proteinuria. No test de VIH, as proteínas do VIH sepáranse por SDS-PAGE e seguidamente son detectadas por western blot con anticorpos específicos para o VIH do paciente, se están presentes no seu soro sanguíneo. A SDS-PAGE para a proteinuria avalía os niveis de varias proteínas do soro na urina, por exemplo a albumina, alfa-2-macroglobulina e IgG.
Variantes
editarA SDS-PAGE é o método máis utilizado de separación electroforética en xel de proteínas. A electroforese en xel bidimensional combina secuencialmente o isoelectroenfoque ou BAC-PAGE cunha SDS-PAGE. A PAGE nativa utilízase cando se debe manter o pregamento nativo da proteína. Para a separación de proteínas de membrana, a BAC-PAGE ou a CTAB-PAGE pode ser utilizado como unha alternativa á SDS-PAGE. Para a separación electroforética de grandes complexos proteícos pode utilizarse a electroforese en xel de agarosa, por exemplo a SDD-AGE. Algúns encimas poden ser detectados pola súa actividade encimática por zimografía.
Alternativas
editarAínda que é unha das formas de separción de proteínas máis precisa e de menor custo, a SDS-PAGE desnaturaliza as proteínas. Cando son necesarias condicións non desnaturalizantes, as proteínas son separadas por PAGE nativa ou diferentes métodos cromatográficos seguidos de cuantificación fotométrica, por exemplo cromatografía de afinidade (ou mesmo purificación de afinidade en tándem), cromatografía de exclusión por tamaños, cromatografía de intercambio iónico.[39] As proteínas poden tamén separarse por tamaño nunha filtración de fluxo tanxencial[40] ou unha ultrafiltración.[41] Unha proteína determinada pode ser illada da mestura por cromatografía de afinidade ou por un ensaio pull-down. Algúns métodos de separación historicamente temperáns e efectivos en canto a custo pero en cru están xeralmente baseados nunha serie de extraccións e precipitacións usando moléculas cosmotrópicas, como por exemplo a precipitación por sulfato amónico e a precipitación por polietileneglicol.
Historia
editarEn 1948 Arne Tiselius foi galardoado co Premio Nobel de Química polo descubrimento do principio da electroforese como migración de átomos ou moléculas cargadas disoltas nun campo eléctrico.[42] O uso dunha matriz sólida (inicialmente eran discos de papel) nunha electroforese en zona melloraba a separación. A electroforese descontinua de 1964 ideada por L. Ornstein e B. J. Davis fixo posible mellorar a separación polo efecto de amontoamento (stacking).[43] O uso de hidroxeles de poliacrilamida con enlaces cruzados, a diferenza dos anteriormente usados discos de papel ou xeles de amidón, proporcionaron unha maior estabilidade do xel e ningunha descomposición microbiana. O efecto de desnaturaliación do SDS en xeles continuos de poliacrilamida o consecuente aumento da resolución foi descrito primeiro en 1965 por David F. Summers no grupo de traballo de James E. Darnell para separar proteínas de poliovirus.[44] A versión actual da SDS-PAGE foi descrita en 1970 por Ulrich K. Laemmli e usada inicialmente para caracterizar proteínas da cabeza do bacteriófago T4.[1]
Notas
editar- ↑ 1,0 1,1 Laemmli, U. K. (1970). "Cleavage of Structural Proteins during the Assembly of the Head of Bacteriophage T4". Nature 227 (5259): 680–685. ISSN 0028-0836. doi:10.1038/227680a0.
- ↑ Neue Zürcher Zeitung: Interview with Ulrich Lämmli in German. NZZ Folio, No. 11, 2005. Accessed March 4, 2012.
- ↑ 3,0 3,1 3,2 3,3 Reynolds JA, Charles Tanford (1970). "Binding of dodecyl sulfate to proteins at high binding ratios. Possible implications for the state of proteins in biological membranes.". Proc Natl Acad Sci U S A 66 (3): 1002–7. PMC 283150. PMID 5269225. doi:10.1073/pnas.66.3.1002.
- ↑ Smith, B. J. (1984). "SDS Polyacrylamide Gel Electrophoresis of Proteins" 1: 41–56. doi:10.1385/0-89603-062-8:41.
- ↑ Staikos, Georgios; Dondos, Anastasios (2009). "Study of the sodium dodecyl sulphate–protein complexes: evidence of their wormlike conformation by treating them as random coil polymers". Colloid and Polymer Science 287 (8): 1001–1004. ISSN 0303-402X. doi:10.1007/s00396-009-2059-3.
- ↑ Turro, Nicholas J.; Yekta, Ahmad (1978). "Luminescent probes for detergent solutions. A simple procedure for determination of the mean aggregation number of micelles". Journal of the American Chemical Society 100 (18): 5951–5952. ISSN 0002-7863. doi:10.1021/ja00486a062.
- ↑ 1958-, Berg, Jeremy M. (Jeremy Mark),. Biochemistry. Tymoczko, John L., 1948-, Gatto, Gregory J., Jr. (Gregory Joseph), Stryer, Lubert. (Eighth ed.). New York. ISBN 9781464126109. OCLC 913469736.
- ↑ Manning M, Colón W (2004). "Structural basis of protein kinetic stability: resistance to sodium dodecyl sulfate suggests a central role for rigidity and a bias toward beta-sheet structure.". Biochemistry 43 (35): 11248–54. PMID 15366934. doi:10.1021/bi0491898.
- ↑ Buxbaum, Engelbert (2003). "Cationic electrophoresis and electrotransfer of membrane glycoproteins". Analytical Biochemistry 314 (1): 70–76. ISSN 0003-2697. doi:10.1016/S0003-2697(02)00639-5.
- ↑ Akin, Dianne T.; Shapira, Raymond; Kinkade, Joseph M. (1985). "The determination of molecular weights of biologically active proteins by cetyltrimethylammonium bromide-polyacrylamide gel electrophoresis". Analytical Biochemistry 145 (1): 170–176. ISSN 0003-2697. doi:10.1016/0003-2697(85)90343-4.
- ↑ Simpson, R. J. (2010). "CTAB-PAGE". Cold Spring Harbor Protocols 2010 (4): pdb.prot5412–pdb.prot5412. ISSN 1559-6095. doi:10.1101/pdb.prot5412.
- ↑ Hartinger, Joachim; Stenius, Katinka; Högemann, Dagmar; Jahn, Reinhard (1996). "16-BAC/SDS–PAGE: A Two-Dimensional Gel Electrophoresis System Suitable for the Separation of Integral Membrane Proteins". Analytical Biochemistry 240 (1): 126–133. ISSN 0003-2697. doi:10.1006/abio.1996.0339.
- ↑ Margolis J, Kenrick KG (1969). "2-dimensional resolution of plasma proteins by combination of polyacrylamide disc and gradient gel electrophoresis.". Nature 221 (5185): 1056–7. PMID 5774398. doi:10.1038/2211056a0.
- ↑ 14,0 14,1 14,2 Hachmann, John P.; Amshey, Joseph W. (2005). "Models of protein modification in Tris–glycine and neutral pH Bis–Tris gels during electrophoresis: Effect of gel pH". Analytical Biochemistry 342 (2): 237–245. ISSN 0003-2697. doi:10.1016/j.ab.2005.04.015.
- ↑ Wiltfang, Jens; Arold, Norbert; Neuhoff, Volker (1991). "A new multiphasic buffer system for sodium dodecyl sulfate-polyacrylamide gel electrophoresis of proteins and peptides with molecular masses 100 000-1000, and their detection with picomolar sensitivity". Electrophoresis 12 (5): 352–366. ISSN 0173-0835. doi:10.1002/elps.1150120507.
- ↑ Moebius, Jan; Denker, Katrin; Sickmann, Albert (2007). "Ruthenium (II) tris-bathophenanthroline disulfonate is well suitable for Tris-Glycine PAGE but not for Bis-Tris gels". Proteomics 7 (4): 524–527. ISSN 1615-9853. doi:10.1002/pmic.200600642.
- ↑ Ian M. Rosenberg (22 December 2006). Protein Analysis and Purification: Benchtop Techniques. Springer Science & Business Media. pp. 103–. ISBN 978-0-8176-4412-3.
- ↑ Schägger, Hermann; von Jagow, Gebhard (1987). "Tricine-sodium dodecyl sulfate-polyacrylamide gel electrophoresis for the separation of proteins in the range from 1 to 100 kDa". Analytical Biochemistry 166 (2): 368–379. ISSN 0003-2697. doi:10.1016/0003-2697(87)90587-2.
- ↑ Fazekas de St. Groth, S.; Webster, R. G.; Datyner, A. (1963). "Two new staining procedures for quantitative estimation of proteins on electrophoretic strips". Biochimica et Biophysica Acta 71: 377–391. PMID 18421828. doi:10.1016/0006-3002(63)91092-8.
- ↑ 20,0 20,1 20,2 Wilson CM (1979). "Studies and critique of Amido Black 10B, Coomassie Blue R, and Fast Green FCF as stains for proteins after polyacrylamide gel electrophoresis.". Anal Biochem 96 (2): 263–78. PMID 89822. doi:10.1016/0003-2697(79)90581-5.
- ↑ C. R. Merril, R. C. Switzer, M. L. Van Keuren: Trace polypeptides in cellular extracts and human body fluids detected by two-dimensional electrophoresis and a highly sensitive silver stain. En: Proc Natl Acad Sci U S A. 76(9), 1979, S. 4335–4339. PMID 92027.
- ↑ R. C. Switzer, C. R. Merril, S. Shifrin (1979-09). "A highly sensitive silver stain for detecting proteins and peptides in polyacrylamide gels". Anal Biochem (en German) 98 (1): 231–237. PMID 94518. doi:10.1016/0003-2697(79)90732-2.
- ↑ H. Blum, H. Beier, H. J. Gross: Improved silver staining of plant protein, RNA & DNA in PAA gels. En: Electrophoresis. 8, 1987, S. 93–99.
- ↑ T. Rabilloud et. al.: Improvement and simplification of low-background silver staining of proteins by using sodium dithionite. En: Electrophoresis. 9(6), 1998, S. 288–291. PMID 2466660.
- ↑ T. Rabilloud: A comparison between low background silver diammine and silver nitrate protein stains. In: Electrophoresis. 13, 1992, S. 429–439. PMID 1425556.
- ↑ C. Lelong, M. Chevallet, S. Luche, T. Rabilloud: Silver staining of proteins in 2DE gels. In: Methods Mol Biol. 519, 2009, S. 339–350. PMID 19381593.
- ↑ Christian P. Moritz, Sabrina X. Marz, Ralph Reiss, Thomas Schulenborg, Eckhard Friauf: Epicocconone staining: a powerful loading control for Western blots. In: Proteomics. PMID 24339236.
- ↑ Aleksandr Petrovich Demchenko: Advanced Fluorescence Reporters in Chemistry and Biology III: Applications in Sensing and Imaging Band 3 von Advanced Fluorescence Reporters in Chemistry and Biology. Springer 2011, ISBN 978-3-642-18035-4, S. 179ff.
- ↑ Gallagher, Sean; Chakavarti, Deb (2008). "Staining Proteins in Gels". Journal of Visualized Experiments (17). ISSN 1940-087X. PMC 3253607. doi:10.3791/760.
- ↑ Wilson CM (1983). "Staining of proteins on gels: comparisons of dyes and procedures.". Methods Enzymol 91: 236–47. PMID 6190068.
- ↑ Ladner CL, Yang J, Turner RJ, Edwards RA (2004). "Visible fluorescent detection of proteins in polyacrylamide gels without staining.". Anal Biochem 326 (1): 13–20. PMID 14769330. doi:10.1016/j.ab.2003.10.047.
- ↑ Gilda JE, Gomes AV (2013). "Stain-Free total protein staining is a superior loading control to β-actin for Western blots.". Anal Biochem 440 (2): 186–8. PMC 3809032. PMID 23747530. doi:10.1016/j.ab.2013.05.027.
- ↑ 33,0 33,1 Cryo-EM Part A: Sample Preparation and Data Collection. Academic Press. 30 September 2010. p. 28. ISBN 978-0-08-095695-4.
- ↑ Richard R Burgess; Murray P. Deutscher (3 November 2009). Guide to Protein Purification. Academic Press. pp. 184–. ISBN 978-0-08-092317-8.
- ↑ Philip L.R. Bonner; Alan J. Hargreaves (24 August 2011). Basic Bioscience Laboratory Techniques: A Pocket Guide. John Wiley & Sons. pp. 140–. ISBN 978-1-119-95644-0.
- ↑ Martin Holtzhauer (13 September 2006). Basic Methods for the Biochemical Lab. Springer Science & Business Media. pp. 243–. ISBN 978-3-540-32786-8.
- ↑ W.J. van Venrooij; Ravinder N. Maini (6 December 2012). Manual of Biological Markers of Disease. Springer Science & Business Media. pp. 50–. ISBN 978-94-011-1670-1.
- ↑ Guan, Yihong; Zhu, Qinfang; Huang, Delai; Zhao, Shuyi; Jan Lo, Li; Peng, Jinrong (2015). "An equation to estimate the difference between theoretically predicted and SDS PAGE-displayed molecular weights for an acidic peptide". Scientific Reports 5 (1). ISSN 2045-2322. doi:10.1038/srep13370.
- ↑ Jan-Christer Janson (3 January 2012). Protein Purification: Principles, High Resolution Methods, and Applications. John Wiley & Sons. ISBN 978-1-118-00219-3.
- ↑ Mohamed A. Desai (2000). Downstream Processing of Proteins: Methods and Protocols. Springer Science & Business Media. p. 35. ISBN 978-1-59259-027-8.
- ↑ Ghosh Raja (11 June 2003). Protein Bioseparation Using Ultrafiltration: Theory, Applications And New Developments. World Scientific. p. 142. ISBN 978-1-78326-126-0.
- ↑ Pederson, T. (2007). "Turning a PAGE: the overnight sensation of SDS-polycrylamide gel electrophoresis". The FASEB Journal 22 (4): 949–953. ISSN 0892-6638. doi:10.1096/fj.08-0402ufm.
- ↑ Ornstein, L., Davis, B. J.: Disc Electrophoresis –1. Background and Theory. In: Ann NY Acad Sci. 121, 1964, pp. 321–349.
- ↑ Summers DF, Maizel JV, Darnell JE (1965). "Evidence for virus-specific noncapsid proteins in poliovirus-infected HeLa cells.". Proc Natl Acad Sci U S A 54 (2): 505–13. PMC 219696. PMID 4285933. doi:10.1073/pnas.54.2.505.
Véxase tamén
editarOutros artigos
editarLigazóns externas
editar- OpenWetWare: Protocolo para BisTris SDS-PAGE