L-DOPA
A L-DOPA ou L-3,4-dihidroxifenilalanina, tamén chamada L-dopa[1] ou levodopa[2][3] (Nome Internacional Non propietario, INN) é un composto químico do grupo dos aminoácidos producido e utilizado de forma natural por algúns animais e plantas. Algúns animais, entre eles os humanos, biosintetízano a partir do aminoácido L-tirosina. A L-DOPA é o precursor na ruta biosintética dos neurotransmisores do grupo das catecolaminas dopamina, noradrenalina (norepinefrina), e adrenalina (epinefrina). A L-DOPA pode producirse nos laboratorios farmacéuticos para o seu uso terapéutico como droga psicoactiva, e a esta L-DOPA sintética é á que se lle dá o nome de levodopa (INN) e outros nomes comerciais. Utilízase no tratamento da enfermidade de Parkinson e da distonía sensible á dopamina. O seu isómero óptico é a D-DOPA, que non ten actividade biolóxica.
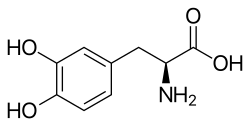
Nome IUPAC: (S)-2-amino-3-(3,4-dihidroxifenil)
ácido propanoico
Número CAS: 59-92-7.
Masa molecular: 197,19 g/mol.
Uso terapéutico
editarA L-DOPA pode cruzar a barreira hematoencefálica protectora do sistema nervioso central, mentres que a dopamina non pode. Deste modo, a L-DOPA utilízase para incrementar as concentracións de dopamina no tratamento da enfermidade de Parkinson e a distonía sensible á dopamina. Este tratamento foi desenvolvido orixinariamente por George Cotzias e os seus colegas. Unha vez que a L-DOPA entrou no sistema nervioso central, convértese en dopamina pola acción do encima L-aminoácido aromático descarboxilase, tamén chamada DOPA descarboxilase (DDC). O fosfato de piridoxal (vitamina B6) requírese como cofactor nesta reacción química, e pode ser administrada ocasionalmente xunto con L-DOPA, xeralmente en forma de piridoxina.
Ademais de no sistema nervioso central, a L-DOPA tamén se converte en dopamina no sistema nervioso periférico. A hiperdopaminerxia resultante causa moitos dos efectos secundarios adversos observados cando se administra só L-DOPA. Para evitar estes efectos, é unha práctica clínica estándar coadministrar (xunto coa L-DOPA) un inhibidor da DOPA descarboxilase (DDCI) periférico como a carbidopa ou unha benserazida, para previr a síntese periférica de dopamina a partir de L-DOPA. A coadministración de piridoxina sen un DDCI acelera a descarboxilación periférica de L-DOPA ata o punto que anula os efectos da administración da L-DOPA, un fenómeno que historicamente causou gran confusión.
Ademais, a L-DOPA, coadministrada cun DDCI periférico, foi investigada como un tratamento potencial para a síndrome das pernas inquietas. Porén, os estudos realizados non demostraron "nigún cadro claro de redución de síntomas".[4]
Os dous tipos de resposta observados coa administración de L-DOPA son:
- Resposta de curta duración, a cal está relacionado coa vida media da droga.
- Resposta de maior duración, a cal depende da acumulación de efectos durante polo menos dúas semanas. Esta resposta é evidente só na terapia inicial, xa que a incapacidade do cerebro para almacenar dopamina non é aínda preocupante.
Suplemento dietario
editarEstán á venda extractos de herbas que conteñen L-DOPA. A fonte vexetal máis común de L-DOPA comercializada son as sementes da planta fabácea Mucuna pruriens.[5] A L-DOPA está tamén presente en sementes de Vicia faba (faballóns).[6] O aminoácido tirosina, precursor da levodopa, tamén se comercializa, e ademais convértese no corpo en dopamina, noradrenalina e adrenalina.
Papel biolóxico
editarA L-DOPA orixínase a partir do aminoácido L-tirosina por acción do encima tirosina hidroxilase (TH). Tamén é o precursor dos neurotransmisores monoaminas ou catecolaminas dopamina, noradrenalina (norepinefrina), e adrenalina (epinefrina). A dopamina orixínase pola descarboxilación de L-DOPA.
A L-DOPA pode ser metabolizada directamente pola catecol-O-metil transferase (COMT) a 3-O-metildopa (3-OMD), e despois a ácido vainiláctico (VLA). Esta vía metabólica non existe no corpo san, pero faise importante despois da administración periférica de L-DOPA en pacientes con enfermidade de Parkinson ou nos raros casos de pacientes con deficiencia do encima L-aminoácido aromático descarboxilase (AADC).[7]
O prefixo L- neste composto refírese á súa propiedade de levorrotación (desvía á esquerda o plano da luz polarizada que atravesa unha disolución do composto). Existe tamén un isómero D dextrorrotatorio, a D-DOPA.
A L-fenilalanina, a L-tirosina, e a L-DOPA, son todos precursores do pigmento biolóxico melanina. O encima tirosinase cataliza a oxidación de L-DOPA ao seu reactivo intermediario dopaquinona, que reacciona ulteriormente dando lugar finalmente aos oligómeros de melanina.
Historia
editarO científico sueco Arvid Carlsson, nun traballo que posteriormente lle valeu o premio Nobel de Medicina de 2000, foi o primeiro que mostrou na década de 1950 que a administración de L-DOPA a animais con síntomas do párkinson causaba unha diminución da súa intensidade. Este tratamento estendeuse máis tarde ao envelenamento por manganeso e despois George Cotzias e colegas aplicárono á enfermidade de Parkinson[8] aumentando notablemente a dose. O neurolólogo Oliver Sacks describiu este tratamento en pacientes humanos con encefalite letárxica no seu libro Awakenings, sobre o que se fixo unha película.
O Premio Nobel de Química de 2001 estivo relacionado coa L-DOPA. Un dos que o Comité Nobel galardoou co premio dese ano foi William S. Knowles polo seu traballo sobre reaccións de hidroxenación catalizadas quiralmente, cuxo exemplo máis importante é a síntese da L-DOPA:[9]
Moléculas adhesivas
editarA L-DOPA é un composto esencial para a formación de proteínas adhesivas mariñas, como as que ten o mexillón no seu biso (filamentos cos que se pega ás rochas). Crese que é responsable da resistencia á auga e a rapidez de secado destas proteínas. A L-DOPA pode tamén usarse para impedir que as superficies de barcos e outros materiais sufran bioincrustación (biofouling), o que se consegue unindo polímeros antiincrustación aos substratos susceptibles.[10]
D-DOPA
editarNome IUPAC: (R)-2-amino-3-(3,4-dihidroxifenil)ácido propiónico.
Número CAS: 5796-17-8.
A D-DOPA[11] ou D-3,4-dihidroxifenilalanina ou dextrodopa é un composto similar á L-DOPA (levodopa), pero con quiralidade oposta. Os compostos levorrotatorios e dextrorrotatorios fan xirar o plano da luz polarizada en sentidos opostos (a esquerda e dereita, respectivamente), os mesmos graos. Aínda que a L-DOPA ten certa efectividade no tratamento do párkinson e da distonia sensible á dopa, a D-DOPA é bioloxicamente inactiva e sen usos terapéuticos.
Notas
editar- ↑ CHEBI
- ↑ PubChem compound. Levodopa
- ↑ "Chem Spider. Levodopa". Arquivado dende o orixinal o 15 de marzo de 2013. Consultado o 01 de febreiro de 2013.
- ↑ "L-dopa for RLS". Bandolier. 1 April 2007. Arquivado dende o orixinal o 20 de abril de 2016. Consultado o 2008-10-16.
- ↑ "Copia arquivada". Arquivado dende o orixinal o 27 de xaneiro de 2013. Consultado o 01 de febreiro de 2013.
- ↑ "Copia arquivada". Arquivado dende o orixinal o 22 de xullo de 2018. Consultado o 01 de febreiro de 2013.
- ↑ Hyland K, Clayton PT (1992). "Aromatic L-amino acid decarboxylase deficiency: diagnostic methodology" (PDF). Clinical chemistry 38 (12): 2405–10. PMID 1281049. Arquivado dende o orixinal (PDF) o 07 de xuño de 2011. Consultado o 01 de febreiro de 2013.
- ↑ Cotzias, GC; Papavasiliou, PS; Gellene, R (1969). "L-dopa in parkinson's syndrome". The New England Journal of Medicine 281 (5): 272. PMID 5791298. doi:10.1056/NEJM196907312810518.
- ↑ http://www.chem.wisc.edu/areas/reich/syntheses/dopa-monsanto-knowles.htm
- ↑ "Mussel Adhesive Protein Mimetics". Arquivado dende o orixinal o 29 de maio de 2006. Consultado o 01 de febreiro de 2013.
- ↑ PubChem compound. D-DOPA