Neurotransmisor monoamina
Os neurotransmisores monoaminas son compostos químicos que funcionan como neurotransmisores e neuromoduladores, que conteñen un grupo amino conectado a un anel aromático por medio dunha cadea de dous carbonos (como -CH2-CH2-). Exemplos son a dopamina, a norepinefrina e a serotonina.

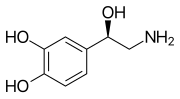
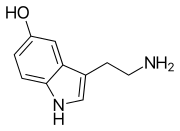
Todas as monoaminas derivan de aminoácidos aromáticos como a fenilalanina, tirosina e triptófano pola acción de encimas aminoácido aromático descarboxilases. Son desactivadas no corpo polos encimas monoamino oxidases, que separan o grupo amino.
Sistemas monoaminérxicos, por exemplo as redes neuronais que usan neurotransmisores monoaminas, están implicados na regulación de procesos como a emoción, excitación e certos tipos memoria. Tamén desempeñan un importante papel na secreción e produción de neurotrofina-3 realizada polos astrocitos, un composto químico que mantén a integridade das neuronas e proporciona a estas soporte trófico.[1]
As drogas que incrementan ou reducen o efecto de neurotransmisores monoamina utilízanse para tratar pacientes con trastornos psiquiátricos e neurolóxicos, incluíndo a depresión, ansiedade, esquizofrenia e párkinson.[2]
Exemplos
editarMonoaminas clásicas
editar- Imidazolaminas:
- Catecolaminas:
- Adrenalina (Ad; Epinefrina, Epi)
- Dopamina (DA)
- Noradrenalina (NAd; Norepinefrina, NE)
- Indolaminas:
- Serotonina (5-HT)
- Melatonina (MT)
Aminas traza
editarEntre as aminas traza humanas están as seguintes:
- Fenetilaminas (relacionadas coas catecolaminas):
- Compostos de tironamina:
- Triptamina[7][5][6]
Existen unhas proteínas transportadoras específicas chamadas transportadores de monoaminas que transportan monoaminas cara a dentro e a fóra da célula. Son o transportador de dopamina (DAT), o transportador de serotonina (SERT) e o transportador de norepinefrina (NET), situados na membrana plasmática externa,[9][10] e os transportadores de monoaminas vesiculares (VMAT1 e VMAT2), situados en membranas intracelulares de vesículas.[11]
Despois da súa liberación na fenda sináptica, a acción dos neurotransmisores monoaminas acaba na recaptación no terminal presináptico.[10] Alí, poden ser reempaquetados en vesículas sinápticas ou degradados polo encima monoamino oxidase (MAO), que é a diana dos inhibidores da monoamina oxidase, un tipo de antidepresivos.[12]
Evolución
editarOs sistemas de neurotransmisores monoaminas aparecen en virtualmente todos os vertebrados, nos cales a evolucionabilidade destes sistemas serviu para promover a adaptabilidade das especies de vertebrados a diferentes ambientes.[13][14]
Notas
editar- ↑ Mele, Tina; Čarman-Kržan, Marija; Jurič, Damijana Mojca (2010). "Regulatory role of monoamine neurotransmitters in astrocytic NT-3 synthesis". International Journal of Developmental Neuroscience 28 (1): 13–9. PMID 19854260. doi:10.1016/j.ijdevneu.2009.10.003.
- ↑ Kurian, Manju A; Gissen, Paul; Smith, Martin; Heales, Simon JR; Clayton, Peter T (2011). "The monoamine neurotransmitter disorders: An expanding range of neurological syndromes". The Lancet Neurology 10 (8): 721–33. PMID 21777827. doi:10.1016/S1474-4422(11)70141-7.
- ↑ Romero-Calderón R, Uhlenbrock G, Borycz J, Simon AF, Grygoruk A, Yee SK, Shyer A, Ackerson LC, Maidment NT, Meinertzhagen IA, Hovemann BT, Krantz DE (novembro de 2008). "A glial variant of the vesicular monoamine transporter is required to store histamine in the Drosophila visual system". PLOS Genet. 4 (11): e1000245. PMC 2570955. PMID 18989452. doi:10.1371/journal.pgen.1000245.
A diferenza doutros neurotransmisores monoamina, o mecanismo polo cal se regula o contido de histamina do cerebro segue estando pouco claro. En mamíferos, os transportadores de monoamina vesiculares (VMATs) exprésanse exclusivamente en neuronas e son mediadores no almacenamento de histamina e outras monoaminas.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 Broadley KJ (marzo de 2010). "The vascular effects of trace amines and amphetamines". Pharmacol. Ther. 125 (3): 363–375. PMID 19948186. doi:10.1016/j.pharmthera.2009.11.005.
As aminas traza son metabolizadas no corpo dos mamíferos pola monoamino oxidase (MAO; EC 1.4.3.4) (Berry, 2004) (Fig. 2) ... Esta desamina aminas primarais e secundarias que están libres no citoplasma neuronal mais que non se unen a vesículas de almacenamento das neuronas simpáticas ... De xeito similar, a β-PEA non sería desaminada no tracto dixestivo, xa que é un substrato selectivo da MAO-B, que non se encontra no tracto dixestivo ...
Os niveis cerebrais de aminas traza endóxenas son varios centos de veces menores que os dos neurotransmisores clásicos noradrenalina, dopamina e serotonina, pero as súas taxas de síntese son equivalentes ás da noradrenalina e dopamina e teñen unha taxa de recambio moi rápida (Berry, 2004). Os niveis en tecidos extracelulares endóxenos de aminas traza medidos no cerebro están no rango nanomolar baixo. Estas baixas concentracións orixínanse debido ás súas vidas medias curtas ... - ↑ 5,0 5,1 5,2 Miller GM (xaneiro de 2011). "The emerging role of trace amine-associated receptor 1 in the functional regulation of monoamine transporters and dopaminergic activity". J. Neurochem. 116 (2): 164–176. PMC 3005101. PMID 21073468. doi:10.1111/j.1471-4159.2010.07109.x.
- ↑ 6,00 6,01 6,02 6,03 6,04 6,05 6,06 6,07 6,08 6,09 6,10 6,11 Khan MZ, Nawaz W (outubro de 2016). "The emerging roles of human trace amines and human trace amine-associated receptors (hTAARs) in central nervous system". Biomed. Pharmacother. 83: 439–449. PMID 27424325. doi:10.1016/j.biopha.2016.07.002.
- ↑ 7,0 7,1 7,2 7,3 7,4 Lindemann L, Hoener MC (maio de 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends Pharmacol. Sci. 26 (5): 274–281. PMID 15860375. doi:10.1016/j.tips.2005.03.007.
Ademais da principal vía metabólica, as TAs [aminas traza] poden tamén ser convertidas por N-metiltransferases (NMT) [22] e feniletanolamina N-metiltransferases (PNMT) non específicas nas correspondentes aminas secundarias (por exemplo a sinefrina, N-metilfeniletilamina e N-metiltiramina), que presentan actividades similares sobre TAAR1 (TA1) como os seus precursores de amina primaria...Tanto a dopamina coma a 3-metoxitiramina, que non sofren unha maior N-metilación, son agonistas parciais de TAAR1 (TA1). ...
A desregulación dos niveis de TA foi ligada a varias doenzas, o cal salienta os membros correspondentes da familia de TAAR como dianas potenciais para o desenvolvemento de fármacos. Neste artigo centrámonos na relevancia das TAs e os seus receptores para os trastornos relacionados co sistema nervioso, concretamente a esquizofrenia e a depresión; porén, as TAs foron tamén ligadas a outras doenzas como as migrañas, o trastorno por déficit de atención con hiperactividade, abuso de drogas e trastornos da alimentación. Os estudos clínicos informan dun incremento dos niveis plasmáticos de β-PEA en pacientes de esquizofrenia aguda e elevada excreción urinaria de β-PEA en esquizofrénicos paranoides, o cal apoia que as TAs teñan un papel na esquizofrenia. Como resultado destes estudos, a β-PEA foi denominada a "anfetamina endóxena" do corpo. - ↑ Wainscott DB, Little SP, Yin T, Tu Y, Rocco VP, He JX, Nelson DL (xaneiro de 2007). "Pharmacologic characterization of the cloned human trace amine-associated receptor1 (TAAR1) and evidence for species differences with the rat TAAR1". The Journal of Pharmacology and Experimental Therapeutics 320 (1): 475–85. PMID 17038507. doi:10.1124/jpet.106.112532.
- ↑ Ramamoorthy, Sammanda; Shippenberg, Toni; Jayanthi, Lankupalle (2010). "Regulation of monoamine transporters: Role of transporter phosphorylation". Pharmacology & Therapeutics 129 (2): 220–238. PMC 3031138. PMID 20951731. doi:10.1016/j.pharmthera.2010.09.009.
- ↑ 10,0 10,1 Torres, Gonzalo E.; Raul R. Gainetdinov; Marc G. Caron (xaneiro de 2003). "Plasma Membrane Monoamine Transporters: Structure, Regulation and Function". Nature Reviews Neuroscience 4 (1): 13–25. PMID 12511858. doi:10.1038/nrn1008.
- ↑ Wimalasena K (2010). "Vesicular monoamine transporters: structure-function, pharmacology and medicinal chemistry". Medicinal Research Reviews 31 (4): 483–19. PMC 3019297. PMID 20135628. doi:10.1002/med.20187.
- ↑ Yeung AW, Georgieva MG, Atanasov AG, Tzvetkov NT (2019). "Monoamine Oxidases (MAOs) as Privileged Molecular Targets in Neuroscience: Research Literature Analysis". Frontiers in Molecular Neuroscience 12: 143. PMC 6549493. PMID 31191248. doi:10.3389/fnmol.2019.00143.
- ↑ Callier S, Snapyan M, Le Crom S, Prou D, Vincent JD, Vernier P (2003). "Evolution and cell biology of dopamine receptors in vertebrates". Biology of the Cell 95 (7): 489–502. PMID 14597267. doi:10.1016/s0248-4900(03)00089-3.
Esta "evolucionabilidade" dos sistemas de dopamina foi un instrumento para adaptar as especies de vertebrados a case todos os posibles ambientes.
- ↑ Vincent JD, Cardinaud B, Vernier P (1998). "[Evolution of monoamine receptors and the origin of motivational and emotional systems in vertebrates]". Bulletin de l'Académie Nationale de Médecine (en francés) 182 (7): 1505–14; discussion 1515–6. PMID 9916344.
Estes datos suxiren que foi necesaria unha duplicación do xene do receptor D1/beta para elaborar novas respostas adaptativas psicomotaras de catecolaminas e que xurdiu expecificacmente un sitema noradrenérxico na orixe da evolución dos vertebrados.
Véxase tamén
editarOutros artigos
editar- Inhibidor da recaptación de monoaminas
- Receptor de monoaminas
- Monoamino oxidase
- Transportador de monoaminas
- Amina bioxénica
Ligazóns externas
editar- Biogenic monoamines Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.