Terpeno
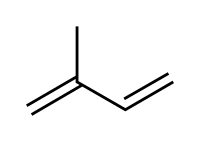
Un terpeno[1] ou isoprenoide é un tipo de lípido insaponificable derivado do isopreno (ou 2-metil-1,3-butadieno), un hidrocarburo de 5 átomos de carbono que se polimeriza. O nome procede da palabra inglesa turpentine (augarrás ou esencia de trementina), xa que os primeiros que se obtiveron derivaban dese produto.[2] Cando os terpenos son modificados quimicamente, por exemplo por oxidación ou reorganización do esqueleto hidrocarbonado, adoitan denominarse terpenoides (como a vitamina A ou retinol, que contén un átomo de osíxeno).


Os terpenos son produtos principalmente vexetais, especialmente das coníferas, pero hainos en todos os grandes grupos de seres vivos.[3]. Algúns animais como térmites ou certas bolboretas emítenos no seu osmeterio. Os terpenos máis importantes das plantas son os carotenoides, que interveñen na captación de enerxía luminosa durante a fotosíntese.
Xeneralidades
editarOs terpenos orixínanse por polimerización encimática de dúas ou máis unidades de isopreno, ensambladas e modificadas de moitos xeitos diferentes. A maioría dos terpenos teñen estruturas multicíclicas, que difiren non só nos grupos funcionais senón tamén no seu esqueleto básico de carbono. En realidade o isopreno non é o precursor biolóxico dos terpenos, senón o pirofosfato de isopentenilo (isopreno activo), pero considérase que o isopreno é a súa unidade básica porque a descomposición por calor de moitos terpenos orixina isopreno, e porque se pode inducir ao isopreno a polimerizarse en múltiplos de 5 carbonos, xerando numerosos esqueletos de terpenos.[2]
Nas plantas os terpenos cumpren moitas funcións primarias: algúns pigmentos carotenoides son terpenos, tamén forman parte da clorofila e as hormonas xiberelina e ácido abscísico. Os terpenos tamén cumpren a función de aumentar a fixación dalgunhas proteínas ás membranas celulares, o que se coñece como isoprenilación. Os esteroides e esterois prodúcense a partir de terpenos precursores.
Os terpenos das plantas son moi utilizados polas súas cualidades aromáticas (esencias de eucalipto, menta, limón, xeranio...) e na medicina tradicional, e estanse a investigar os seus posibles efectos antibacterianos e outros usos farmacéuticos.
A formación de terpenos en plantas, animais e microorganismos realízana encimas moi similares, pero hai importantes diferenzas nos procesos. En particular, as plantas producen unha variedade moitísimo maior cós animais ou os microbios, e esta diferenza reflíctese na complexa organización da biosíntese dos terpenos das plantas a nivel tisular, celular, subcelular, e xenético. A biosíntese dos terpenos está compartimentalizada, como tamén o está a formación do seu precursor o pirofosfato de isopentenilo. A produción de grandes cantidades de terpenos así como a súa acumulación, emisión ou secreción está case sempre asociada coa presenza de estruturas moi especializadas anatomicamente. Por exemplo os tricomas glandulares e as cavidades secretoras das follas, e a epiderme glandular dos pétalos xeran e almacenan ou emiten terpenos que son aceites esenciais importantes para a polinización por insectos. Os condutos e ampolas de resina das coníferas producen e acumulan unha resina defensiva consistente en augarrás (olefinas monoterpénicas) e rosina (ácidos resinosos diterpénicos). As ceras superficiais triterpénicas son formadas e excretadas por unha epiderme especialiada, e os laticíferos producen certos triterpenos e politerpenos como o caucho. Estas estruturas especializadas secuestran aos metabolitos secundarios lonxe dos procesos metabólicos sensibles e así preveñen a autotoxicidade. Moitas estruturas deste tipo son non fotosintéticas e, por tanto, dependen de células adxacentes para fornecerse do carbono e a enerxía necesarios para biosintetizar os terpenos.
Clasificación
editarOs terpenos son hidrocarburos que poden considerarse como unha combinación de numerosas unidades de isopreno, en xeral unidas de forma cabeza-cola, pero tamén poden darse combinacións cabeza-cabeza e mesmo cabeza-medio. Os terpenoides poden ser considerados como terpenos modificados nos que os grupos metilo foron cambiados de posición ou eliminados ou aos que se lles engadiu átomos de osíxeno.
A clasificación dos terpenos segundo a súa estrutura química depende do número de unidades de isopreno de que consten e de se están ciclados ou non. Clasifícanse en:
- Hemiterpenos. Son os terpenos máis pequenos, cunha soa unidade de isopreno. Posúen 5 carbonos. O hemiterpeno máis coñecido é o propio isopreno, un produto volátil que se desprende dos tecidos fotosinteticamente activos. Derivados que conteñen osíxeno (hemiterpenoides) son o prenol e o ácido isovalérico.
- Monoterpenos. Terpenos de 10 carbonos (equivalente a dous isoprenos). Chamados así porque os primeiros terpenos illados do augarrás en 1850, foron considerados a unidade básica de todos eles. Os monoterpenos mellor coñecidos son compoñentes das esencias volátiles das flores e dos aceites esenciais de herbas e especias. Son exemplos o xeraniol, limoneno e terpineol.
- Sesquiterpenos. Terpenos de 15 carbonos (é dicir, conteñen un monoterpeno e medio, o que equivale a 3 isoprenos). Moitos están presentes en aceites esenciais ou actúan como fitoalexinas (non todas sesquiterpenos), compostos antibióticos producidos polas plantas en resposta á aparición de microbios, ou como repelentes da alimentación dos herbívoros oportunistas. A hormona das plantas chamada ácido abscísico é estruturalmente un sesquiterpeno, aínda que o seu precursor de 15 carbonos, a xantosina, non se sintetiza directamente de 3 unidades isopreno senón que se produce pola escisión asimétrica dun carotenoide de 40 unidades. Un exemplo de sesquiterpeno é o farnesol.
- Diterpenos. Terpenos de 20 carbonos (equivalen a 2 monoterpenos ou 4 isoprenos). Entre eles inclúese o cafestol, o fitol, que forma a cadea hidrófoba da clorofila, as hormonas xiberelinas, os ácidos das resinas das coníferas e dos legumes, as fitoalexinas, e unha serie de metabolitos farmacoloxicamente importantes, incluíndo o taxol, un axente anticanceríxeno atopado no teixo, e a forskolina, un composto usado para tratar o glaucoma. Algunhas xiberelinas teñen 19 átomos de carbono polo que non son consideradas diterpenos porque perderon un átomo de carbono durante unha reacción de escisión. derivan de diterpenos o retinol e o retinal.
- Triterpenos. Terpenos de 30 carbonos (equivalen a 3 monoterpenos ou 6 isoprenos). Son xeralmente compostos formados pola unión cabeza-cabeza de dúas cadeas de 15 carbonos, pero cada unha delas formada por unidades de isopreno unidas cabeza-cola. Nesta gran clase de moléculas poderiamos incluír os brassinoesteroides, compoñentes da membrana que son fitosterois, algunhas fitoalexinas, varias toxinas e repelentes de herbívoros, e compoñentes das ceras da superficie das plantas, como o ácido oleanólico das uvas. O triterpeno escualeno é precursor dos esteroides.
- Tetraterpenos. Terpenos de 40 carbonos (equivalen a 4 monoterpenos ou 8 unidades de isopreno). Os máis abundantes son os pigmentos carotenoides (carotenos e xantofilas) accesorios na absorción de luz na fotosíntese.
- Politerpenos. Conteñen máis de 8 unidades de isopreno. Entre eles están transportadores de electróns como a plastoquinona e a ubiquinona, e outros como o dolicol), ou o caucho do látex de certas plantas, que pode ter miles de unidades de isopreno con enlaces cis. A gutapercha é outro politerpeno con enlaces trans, o que a fai moito menos elástica ca o caucho.
Ademais destes grandes grupos poden considerarse outros, como os meroterpenos, que son metabolitos secundarios das plantas que teñen unha orixe só parcialmente derivada dos terpenos. Por exemplo, tanto as citoquininas coma moitos fenilpropanoides conteñen cadeas laterais dun isoprenoide de 5 carbonos. Os cannabinoides (principio activo da marihuana) teñen unha porción molecular orixinada a partir dun policétido e outra de orixe terpénica. Algúns alcaloides, como as drogas anticáncer vincristina e vinblastina, conteñen fragmentos terpénicos nas súas estruturas. Ademais algunhas proteínas modificadas inclúen unha cadea lateral de 15 ou 20 carbonos que é un terpeno, que ancora a proteína á membrana.
Os esteroides están moi relacionados cos terpenos, xa que derivan do escualeno. Poderían considerarse como triterpenos cunha estrutura de catro ciclos, pero xeralmente clasifícanse á parte[2].
Biosíntese
editarOs terpenos poden obterse a partir de acetil-CoA, que orixina as moléculas iniciais mevalonato e pirofosfato de isopentenilo. A molécula básica na síntese de todos os terpenos é o pirofosfato de isopentenilo (IPP, chamado isopreno activo). A unión de dous monómeros de pirofosfato de isopentenilo orixina o precursor pirofosfato de xeranilo (GPP). O pirofosfato de xeranilo é o precursor dos monoterpenos. A incorporación doutra unidade isoprénica orixina pirofosfato de farnesilo (FPP), precursor dos sesquiterpenos. Unha unidad máis forma o pirofosfato de xeranilxeranilo (GGPP), a partir do cal se orixinan os diterpenos. O escualeno, precursor de triterpenos e esteroides, fórmase pola dimerización de dúas unidades de FPP, mentres que o fitofluoeno, composto base para os carotenoides, obtense por dimerización do GGPP. Os politerpenos fórmanse por unións isoprénicas múltiples e repetitivas, e xeralmente non presentan ciclacións.
As unidades de pirofosfato de isopentenilo poden biosintetizarse por dúas vías:
- A través de intermediarios da vía do ácido mevalónico (MVA) (ou mevalonato). Esta é a vía normal utilizada pola gran maioría dos seres vivos.
- A partir de compostos derivados da vía alternativa á do mevalonato ou vía do 2-C-metil-D-eritritol 4-fosfato, denominada tamén vía da 5-Fosfono-1-Desoxi-D-Xilulosa (DXP ou DOXP). Pensábase orixinalmente que os precursores biosintéticos de todos os terpenos proviñan da vía do mevalonato, ata que recentemente se descubriu que diversos terpenos en plantas e bacterias se producen mediante a ruta DXP.[4]
Vía do mevalonato
editar- Artigo principal: Vía do mevalonato.
Esta vía biosintética parte de dúas unidades de acetil coencima A (Ac-CoA), que se condensan por medio dunha condensación de Claisen para dar acetoacetil-CoA (AcAcCoA). Esta molécula volve a se condensar cunha terceira unidade de acetil-CoA para dar como produto o 3-hidroxi-3-metilglutaril-CoA (HMG-CoA). O tioéster do coencima A redúcese para formar o aldehido correspondente, o mevaldehido (MVA), o cal se reduce a ácido mevalónico (MEV) (mevalonato). Por acción de dúas moléculas de ATP o mevalonato fosforílase orixinando MEV-P e MEV-PP, e descarboxílase para dar como produtos os precursores dos terpenos, o pirofosfato de isopentenilo (IPP) e o seu isómero, o pirofosfato de dimetilalilo (DMAPP). A vía do mevalonato é practicamente universal e ten lugar no citosol. Por esta vía sintetízanse principalmente sesquiterpenos, triterpenos e politerpenos.[5]
Encimas:
- EC 6.2.1.16 Acetoacetil-CoA sintetase (AACoAS).
- EC 4.1.3.5 3-Hidroxi-3-metilglutaril-CoA sintase (HMGCoAS).
- EC 1.1.1.88 3-hidroxi-3-metilglutaril-CoA redutase (HMGCoAR).
- EC 2.7.1.36 Mevalonato quinase (MEVK).
- EC 2.7.4.2 Fosfomevalonato quinase (PMK).
- EC 4.1.1.33 Mevalonato 5-difosfato descarboxilase (MDD).
- EC 5.3.3.2 Difosfato de isopentenilo isomerase (IPPI)
Vía alternativa á do mevalonato ou non do mevalonato
editarDenomínase vía da 5-Fosfono-1-Desoxi-D-Xilulosa (vía DXP) ou vía do 2-C-metil-D-eritrol 4-fosfato. Esta vía ten lugar sobre todo nos plastos das plantas e en moitas células procariotas. Por esta ruta sintetízanse sobre todo monoterpenos, diterpenos e carotenoides. Descubriuse cando Flesch observou en 1988 que os patróns de marcaxe isotópica en terpenos hopanoides das bacterias Rhodopseudomonas non coincidían cos correspondentes a unha biosíntese pola vía do mevalonato.[6] Estudos posteriores encontraron que existía unha segunda alternativa independente do mevalonato para biosintetizar unidades isoprénicas en bacterias e plantas. Nesta vía, unha unidade de ácido pirúvico (Pyr), procedente da degradación de carbohidratos, condénsase nunha reacción entre o grupo carbonilo do piruvato co grupo carbonilo do D-gliceraldehido 3-fosfato (G3P), para dar a 5-Fosfono-1-desoxi-D-xilulosa (DXP). Por medio dunha condensación aldólica inversa, xérase o 4-fosfono-2-C-metil-D-eritritol (MEP). Este intermediario conxúgase por medio dunha substitución nucleofílica cunha unidade de citidilribósido, por acción do CTP, para formar 4-(CDP)-2-C-metil-D-eritritol (CDP-ME). Este composto fosforílase no carbono 2, onde se forma o intermediario fosforilado CDP-EMP e despraza o citidilribósido para obter o 2-C-metil-D-eritritol-2,4-ciclofosfato (MEcPP). Por rotura redutiva do ciclo dáse unha reacción de eliminación para formar o pirofosfato de 4-hidroxi-3-metil-but-2-enilo (HMB-PP). O paso final consiste na eliminación do grupo hidroxilo para obter o catión alílico correspondente, o cal pode transpoñerse de tal forma que se isomerizan de maneira reversible o IPP e o DMAPP.
Encimas:
- EC 2.2.1.7: 5-Fosfono-1-desoxi-D-xilulosa sintase (DXS)
- EC 1.1.1.267 5-Fosfono-1-desoxi-D-xilulosa redutoisomerase (DXR)
- EC 2.7.7.60 2-C-metil-D-eritritol 4-fosfato citidililtransferase (CMS)
- EC 2.7.1.148. 4-difosfocitidil-2-C-metil-D-eritritol quinase. (CMK)
- EC 4.6.1.12 2-C-metil-D-eritritol 2,4-ciclodifosfato sintase (MCS)
- EC 1.17.4.3 4-hidroxi-3-metilbut-2-en-1-il difosfato sintase (HDS)
- EC 1.17.1.2 4-hidroxi-3-metilbut-2-enil difosfato redutase (HDR).
Funcións
editarDan cor aos vexetais. Por exemplo a cor laranxa da cenoria débese aos carotenos.
Orixinan diversas substancias olorosas que atraen insectos e aceites esenciais. Por exemplo, limoneno, xeraniol. Tamén hai insectos que segregan terpenos volátiles desde un órgano chamado osmeterio.
Teñen acción defensiva: repelen insectos, herbívoros, microbios e a outras plantas, curan feridas. Por exemplo, fitoalexinas, os compoñentes de resinas, o caucho.
Algúns terpenos son precursores de vitaminas liposolubles: retinaldehido, o retinol (da vitamina A), os carotenos (da vitamina A), os tocoferois (da vitamina E), as quinonas e as ubiquinonas (da vitamina K).
Diversas substancias como os esteroides orixínanse a partir de terpenos (escualeno), e estes forman parte de substancias como as clorofilas e hormonas vexetais, e mesmo de proteínas de membrana isopreniladas.
Notas
editar- ↑ Devlin, T. M. 2004. Bioquímica, 4ª edición. Reverté, Barcelona. ISBN 84-291-7208-4
- ↑ 2,0 2,1 2,2 R. Croteau, T. M. Kutchan, N. G. Lewis. "Natural Products (Secondary Metabolites)". En: Buchanan, Gruissem, Jones (editores). Biochemistry and Molecular Biology of Plants. American Society of Plant Physiologists. Rockville, Maryland, Estados Unidos. 2000. Capítulo 24.
- ↑ Goodwin, T.W. 1971. Aspects of terpenoid chemistry and biochemistry. Academic Press, Londres.
- ↑ Eisenreich W, Rohdich F, Bacher A. (2001). "Deoxyxylulose phosphate pathway to terpenoids.". Trends Plant Sci. 6 (2): 78–84. doi:10.1016/S1360-1385(00)01812-4.
- ↑ Paul M. Dewick (2009). Medicinal natural products: a biosynthetic approach. John Wiley and Sons. ISBN 9780470741689.
- ↑ Flesch, G.; Rohmer, M. (1988). "Prokaryotic hopanoids: the biosynthesis of the bacteriohopane skeleton". European Journal of Biochemistry 175 (2): 405–411. doi:10.1111/j.1432-1033.1988.tb14210.x.