Ácido fumárico
O ácido fumárico ou ácido trans-butenodioico é un ácido orgánico de catro carbonos con fórmula HO2CCH=CHCO2H moi importante no metabolismo. A pH celular está ionnizado formando o anión fumarato. Os seus sales e ésteres chámanse tamén fumaratos.
| Ácido fumárico | |
|---|---|
 | |
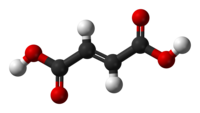 | |
Ácido (E)-butenodioico | |
Outros nomes Ácido trans-1,2-etilenodicarboxílico | |
| Identificadores | |
| Número CAS | 110-17-8 |
| ChemSpider | 10197150 |
| UNII | 88XHZ13131 |
| Número CE | 203-743-0 |
| DrugBank | DB04299 |
| KEGG | C00122 |
| ChEBI | CHEBI:18012 |
| ChEMBL | CHEMBL503160 |
| Código ATC | D05 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C4H4O4 |
| Masa molecular | 116,07 g/mol |
| Aspecto | Sólido branco |
| Densidade | 1,635 g/cm³, sólido |
| Punto de fusión | 287 °C |
| Solubilidade en auga | 0,63 g/100 mL |
| Acidez (pKa) | pka1 = 3,03, pka2 = 4,44 |
| Perigosidade | |
| Clasificación da UE | Irritante (Xi) |
| Frases R | R36 |
| Frases S | S2, S26 |
| NFPA 704 | |
| Compostos relacionados | |
| ácidos carboxílicos relacionados | ácido maleico ácido succínico ácido crotónico |
| Compostos relacionados | cloruro de fumarilo fumaronitrilo dimetil fumarato fumarato de ferro(II) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
É un ácido dicarboxílico, é dicir, con dous grupos carboxilo (-COOH), un en cada extremo da molécula, e un dobre enlace. O ácido fumárico ten os carboxilos na configuración trans, e existe un isómero seu en configuración cis chamado ácido maleico. Úsase como aditivo alimentario (E297), que funciona como regulador da acidez.
O ácido fumárico é abundante na planta Fumaria officinalis, en certos fungos boletos (Boletus fomentarius var. pseudo-igniarius), liques, e musgos de Islandia.
Química
editarO ácido fumárico obtívose por primeira vez a partir do ácido succínico.[1] A síntese tradicional consiste na oxidación do furfural (obtido do procesamento do millo) utilizando clorato en presenza dun catalizador baseado no vanadio.[2] Actualmente, a síntese industrial de ácido fumárico baséase principalmente na isomerización catalítica do ácido maleico en disolución acuosa a pH baixo. Pode dispoñerse de ácido maleico en grandes volumes como produto de hidrólise do anhídrido maleico, producido por oxidación catalítica do benceno ou do butano.[3]
As propiedades químicas do ácido fumárico dependen dos seus grupos funcionais. É un ácido feble, que forma un diéster, e sofre adicións no seu dobre enlace, e é un excelente dienófilo. O ácido fumárico non é combustible nunha bomba calorimétrica en condicións nas que o ácido maleico produciría unha suave deflagración. Cristalizado ten aspecto branco. Densidade 1,635 g/cm3 (sólido). Solubilidade 0,63 g/100 mL. Punto de fusión 287 °C. pKa = pka1 = 3,03, pka2 = 4,44. O ácido fumárico convértese no irritante anhídrido maleico cunha combustión parcial.
Metabolismo
editarO fumarato é un dos intermediarios do ciclo do ácido cítrico, polo que colabora na produción de enerxía (ATP) da respiración celular. Fórmase pola oxidación do succinato catalizada pola succinato deshidroxenase, con produción de FADH2 unido ao encima como grupo prostético, que cede electróns á cadea de transporte electrónico. Na seguinte reacción do ciclo, o fumarato, pola acción da fumarase, convértese en malato por hidratación na que se perde o dobre enlace e se engade un grupo OH.
O fumarato é tamén un produto do ciclo da urea, xa que se libera na transformación do arxininosuccinato en arxinina, catalizada pola arxininosuccinato liase.
Na degradación oxidativa dos aminoácidos tirosina e fenilalanina orixínase fumarato [4], que se incorpora ao ciclo do ácido cítrico para producir enerxía ou pode ser desviado (transformándose en varios pasos en fosfoenolpiruvato) á gliconeoxénese, polo que estes aminoácidos son glicoxénicos (e tamén cetoxénicos).
Usos
editarTerapéutica
editarOs ésteres do ácido fumárico utilízanse para combater a psoríase, xa que se pensa que esta doenza podería estar relacionada coa imposibilidade de producir ácido fumárico na pel.[5][6]
Un éster do ácido fumárico está sendo investigado para aplicalo ao tratamento da esclerose múltiple.[6]
Aditivo alimentario
editarO ácido fumárico é un acidulante utilizado desde 1946. Non é tóxico. Úsase xeralmente en bebidas e formentos de panadaría para o que se usa puro. Úsase tamén como substituto do ácido tartárico e ocasionalmente do ácido cítrico, nunha proporción de 1,36 g de ácido cítrico por cada 0,91 g de ácido fumárico para engadir acidez. Tamén se usa como coagulante en pudins.
Outros usos
editarO ácido fumárico utilízase na manufactura de resinas de poliéster e alcohois polihídricos e como mordente para colorantes. A título experimental probouse a adición de ácido fumárico ao alimento das vacas para diminuír a produción no tracto dixestivo de metano[7]
Notas
editar- ↑ Volhard, J. "Darstellung von Maleïnsäureanhydrid" Justus Liebig's Annalen der Chemie 1892, volume 268, page 255-6. DOI: 10.1002/jlac.18922680108
- ↑ Milas, N. A. "Fumaric Acid" Organic Synthesis 1943, Collective Volume 2, page 302. Online version
- ↑ British Patent No. 775,912, publicated on the May 29, 1957, by Monsanto Chemical Company.
- ↑ Lehninger A. (1988). Omega, ed. Principios de Bioquímica.
- ↑ Br J Dermatol 05; 152(4):597-615), BR J Dermatol 98;138(3): 456-460
- ↑ 6,0 6,1 Moharregh-Khiabani D., Linker R.A., Gold R., Stangel M. Fumaric Acid and its esters: an emerging treatment for multiple sclerosis. pmid 19721818
- ↑ "Scientists look to cut cow flatulence". phys.org (en inglés). Consultado o 13 de decembro 2018.
Véxase tamén
editarOutros artigos
editar- Ciclo do ácido cítrico
- Ácido maleico, o isómero cis do ácido fumárico
