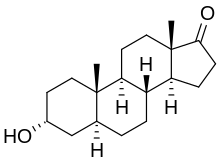
Androsterona
A androsterona ou 5α-androstan-3α-ol-17-ona é unha hormona esteroide endóxena, neurosteroide e posible feromona.[1] É un andróxeno débil cunha potencia que é aproximadamente 1/7 do da testosterona.[2] A androsterona é un metabolito da testosterona e da dihidrotestosterona (DHT). Ademais, pode volver a converterse en dihidrotestosterona pola acción da 3α-hidroxiesteroide deshidroxenase e a 17β-hidroxiesteroide deshidroxenase, sorteando a formación de intermediarios convencionais como a androstenediona e a testosterona, polo que pode considerarse que é un intermediario metabólico.[3][4]

A androsterona tamén é un androstano neurosteroide inhibidor,[5][6] que actúa como modulador alostérico positivo do receptor GABAA,[7] e posúe efectos anticonvulsivos.[8] O enantiómero non natural da androsterona é máis potente como modulador alostérico positivo dos receptores GABAA e como anticonvlsivo que a forma natural.[9] o isómero 3β da androsterona é a epiandrosterona, e o seu epímero 5β é a etiocholanolona. O isómero 3β,5β é a epietiocholanolona.
Función biolóxica
editarA androsterona é xeralmente considerada un metabolito inactivo da testosterona, o cal cando se conxuga por glucuronidación e sulfatación permite que a testosterona sexa eliminada do corpo, pero é un neuroesteroide débil que pode cruzar o cerebro e podería ter efectos sobre a función cerebral.[8]
Feromona
editarA androsterona encóntrase na axila humana e pel e tamén aparece na urina.[10] Pode ademais ser segregada polas glándulas sebáceas humanas.[10] Describiuse como molécula con olor almiscrado similar ao do androstenol.[10] A androsterona afecta á conduta humana cando se cheira.[10]
Bioquímica
editarBiosíntese
editarA androsterona e o seu isómero 5β, a etiocholanolona, prodúceas o corpo como metabolitos da testosterona. A testosterona é convertida en 5α-dihidrotestosterona e 5β-dihidrotestosterona pola 5α-redutase e a 5β-redutase, respectivamente. O encima 3α-hidroxiesteroide deshidroxenase converte as formas reducidas a 5α-androstanediol e 5β-androstanediol, que son seguidamente convertidas pola 17β-hidroxiesteroide deshidroxenase a androsterona e etiocholanolona, respectivamente. A androsterona e a etiocholanolona poden tamén formarse a partir da androstenediona por medio da acción da 5α-redutase e a 5β-redutase formando a 5α-androstanediona e a 5β-androstanediona, que son despois convertidas en androsterona e etiocholanolona pola 3α-hidroxiesteroide deshidroxenase e a 3β-hidroxiesteroide deshidroxenase, respectivamente.[8]
Metabolismo
editarA androsterona é sulfatada a androsterona sulfato e glucuronidado en androsterona glicurónido e estes conxugados son excretados na urina.
Fontes
editarA androsterona aparece de forma natural no pole de piñeiro e en moitas especies animais.[11]
Historia
editarA androsterona foi illada primeiramente en 1931 por Adolf Friedrich Johann Butenandt e Kurt Tscherning. Destilaron uns 17 000 litros de urina humana, dos cales obtiveron 50 mg de androsterona cristalina, que era suficiente para que encontraran que a fórmula química era moi similar á estrona.
Notas
editar- ↑ Motofei, Ion G. (2011). "A dual physiological character for cerebral mechanisms of sexuality and cognition: common somatic peripheral afferents". BJU International 108 (10): 1634–1639. ISSN 1464-4096. doi:10.1111/j.1464-410X.2011.10116.x.
- ↑ Scott T (1996). Concise Encyclopedia Biology. Walter de Gruyter. p. 49. ISBN 978-3-11-010661-9. Consultado o 25 May 2012.
- ↑ Henderson BE; Ponder BAJ; Ross RK (13 March 2003). Hormones, Genes, and Cancer. Oxford University Press. p. 23. ISBN 978-0-19-513576-3. Consultado o 25 May 2012.
- ↑ Kamrath C, Hochberg Z, Hartmann MF, Remer T, Wudy SA (March 2012). "Increased activation of the alternative "backdoor" pathway in patients with 21-hydroxylase deficiency: evidence from urinary steroid hormone analysis". The Journal of Clinical Endocrinology and Metabolism 97 (3): E367–75. PMID 22170725. doi:10.1210/jc.2011-1997. Arquivado dende o orixinal o 25 de setembro de 2019. Consultado o 13 de novembro de 2017.
- ↑ Reddy DS, Rogawski MA (2012). "Neurosteroids — Endogenous Regulators of Seizure Susceptibility and Role in the Treatment of Epilepsy". En Noebels JL, Avoli M, Rogawski MA, et al. Jasper's Basic Mechanisms of the Epilepsies [Internet]. 4th edition. Bethesda (MD): National Center for Biotechnology Information (US).
- ↑ Reddy DS (2010). "Neurosteroids: endogenous role in the human brain and therapeutic potentials". Prog. Brain Res. 186: 113–37. PMC 3139029. PMID 21094889. doi:10.1016/B978-0-444-53630-3.00008-7.
- ↑ Li P, Bracamontes J, Katona BW, Covey DF, Steinbach JH, Akk G (June 2007). "Natural and enantiomeric etiocholanolone interact with distinct sites on the rat alpha1beta2gamma2L GABAA receptor". Mol. Pharmacol. 71 (6): 1582–90. PMID 17341652. doi:10.1124/mol.106.033407. Arquivado dende o orixinal o 25 de setembro de 2019. Consultado o 13 de novembro de 2017.
- ↑ 8,0 8,1 8,2 Kaminski RM, Marini H, Kim WJ, Rogawski MA (June 2005). "Anticonvulsant activity of androsterone and etiocholanolone". Epilepsia 46 (6): 819–27. PMC 1181535. PMID 15946323. doi:10.1111/j.1528-1167.2005.00705.x.
- ↑ Zolkowska D, Dhir A, Krishnan K, Covey DF, Rogawski MA (September 2014). "Anticonvulsant potencies of the enantiomers of the neurosteroids androsterone and etiocholanolone exceed those of the natural forms". Psychopharmacology 231 (17): 3325–32. PMC 4134984. PMID 24705905. doi:10.1007/s00213-014-3546-x.
- ↑ 10,0 10,1 10,2 10,3 Maiworm, R. E.; Langthaler, W. U. (1992). "Influence of Androstenol and Androsterone on the Evalulation of Men of Varying Attractiveness Levels": 575–579. doi:10.1007/978-1-4757-9655-1_88.
- ↑ Janeczko A, Skoczowski A (2005). "Mammalian sex hormones in plants". Folia Histochemica et Cytobiologica 43 (2): 71–79.