Punto triplo
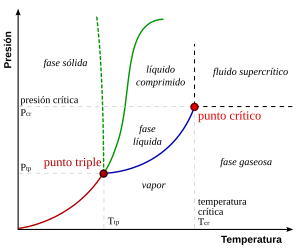
En física, o punto triplo é a temperatura e presión na que coexisten en equilibrio termodinámico o estado sólido, gasoso e líquido nunha substancia. Defínese cunha temperatura e unha presión de vapor.
O punto triplo da auga, por exemplo, está a 273,16 K (0,01 °C) e a unha presión de 611,73 Pa ITS90. Esta temperatura, debido a que é un valor constante, serve para calibrar as escalas Kelvin e Celsius dos termómetros de gran precisión.
Punto triplo da auga
editarA única combinación de presión e temperatura á que a auga en estado líquido, sólido e gasoso poden coexistir nun equilibrio estable prodúcese exactamente a unha temperatura de 273,1598 K (0,0098 °C) e a unha presión parcial de vapor de auga de 611,73 pascais (6,1173 milibares; 0,0060373057 atm). Nesas condicións, é posible cambiar o estado de toda a masa de auga a xeo, auga líquida ou vapor arbitrariamente facendo pequenos cambios na presión e na temperatura. Débese ter en conta que incluso se a presión total dun sistema está moi por riba de 611,73 pascais (é dicir, un sistema cunha presión atmosférica normal), se a presión parcial do vapor de auga é de 611,73 pascais, entón o sistema pode encontrarse aínda no punto triplo da auga . Estritamente falando, as superficies que separan as distintas fases tamén debe ser perfectamente planas, para evitar os efectos das tensións de superficie.
A auga ten un infrecuente e complexo diagrama de fase (aínda que isto non afecta as consideracións xerais expostas sobre o punto triplo). A altas temperaturas, incrementando a presión, primeiro obtense auga líquida e, a continuación, auga sólida. Por encima de 109 Pa aproximadamente obtense unha forma cristalina de xeo que é máis denso que a auga líquida. A temperaturas máis baixas en virtude da compresión, o estado líquido deixa de aparecer e a auga pasa directamente de sólido a gas.
A presións constantes por arriba do punto triplo, quentar xeo fai que se pase de sólido a líquido e deste a gas (ou vapor). A presións por abaixo do punto triplo, como as que se encontran no espazo exterior, onde a presión é próxima a cero, a auga líquida non pode existir e, ao quecer, o xeo convértese directamente en vapor de auga sen pasar polo estado líquido, proceso coñecido como sublimación.
A presión do punto triplo da auga foi utilizada durante a misión Mariner 9 a Marte como un punto de referencia para definir "o nivel do mar". Misións máis recentes fan uso de altimetría láser e gravimetría en lugar da presión atmosférica para medir a elevación en Marte.
Táboa de puntos triplos
editarNesta táboa inclúense os puntos triplos dalgunhas substancias comúns. Estes datos están baseados nos proporcionados pola National Bureau of Standards (agora NIST) dos Estados Unidos de América.[1]
| Substancia | T (K) | P (kPa) |
|---|---|---|
| Acetileno | 192,4 | 120 |
| Amoníaco | 195,40 | 6,076 |
| Argon | 83,81 | 68,9 |
| Grafito | 3900 | 10100 |
| Dióxido de carbono | 216,55 | 517 |
| Monóxido de carbono | 68,10 | 15,37 |
| Deuterio | 18,63 | 17,1 |
| Etano | 89,89 | 8 × 10−4 |
| Etileno | 104,0 | 0,12 |
| Helio-4 | 2,19 | 5,1 |
| Hidróxeno | 13,84 | 7,04 |
| Cloruro de hidróxeno | 158,96 | 13,9 |
| Mercurio | 234,2 | 1,65 × 10−7 |
| Metano | 90,68 | 11,7 |
| Neon | 24,57 | 43,2 |
| Óxido nítrico | 109,50 | 21,92 |
| Nitróxeno | 63,18 | 12,6 |
| Óxido nitroso | 182,34 | 87,85 |
| osíxeno | 54,36 | 0,152 |
| Paladio | 1825 | 3,5 × 10−3 |
| Platino | 2045 | 2,0 × 10−4 |
| Dióxido de xofre | 197,69 | 1,67 |
| Titanio | 1941 | 5,3 × 10−3 |
| Hexafluoruro de uranio | 337,17 | 151,7 |
| Auga | 273,16 | 0,61 |
| Xenon | 161,3 | 81,5 |
| Zinc | 692,65 | 0,065 |
Notas
editar- ↑ Yunus A. Cengel, Robert H. Turner. Fundamentals of thermal-fluid sciences. McGraw-Hill, 2004, p. 78. ISBN 0-07-297675-6