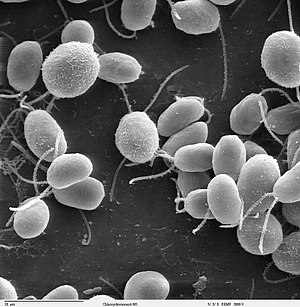
Chlamydomonas reinhardtii
| Chlamydomonas reinhardtii | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||
| Clasificación científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| 'Chlamydomonas reinhardtii' P.A.Dang. | |||||||||||||||
Chlamydomonas reinhardtii é unha especie de alga verde unicelular de aproximadamente 10 micrómetros de diámetro que nada impulsándose con dous flaxelos e vive en augas doces e no solo. Ten unha parede celular feita de glicoproteínas ricas en hidroxiprolina, un cloroplasto grande con forma de copa, un grande pirenoide, e unha "mancha ocular" que percibe a luz.
Está amplamente distribuída por todo o mundo en augas doces e no solo, e utilízase principalmente como organismo modelo en estudos biolóxicos de diversos campos. Cando recibe luz, C. reinhardtii pode crecer en medios carentes de fontes de carbono orgánico e de enerxía química facendo a fotosíntese, pero pode tamén crecer na escuridade cando se lle subministran eses produtos. C. reinhardtii é tamén interesante para a produción de produtos biofarmacéuticos e de biocombustibles, xa que pode producir hidróxeno.
Historia
editarA C. reinhardtii de tipo salvaxe da cepa de laboratorio c137 (mt+) orixinouse a partir dun illado feito preto de Amherst, Massachusetts, en 1945 por Gilbert M. Smith.[1][2]
O nome da especie tense escrito de diferentes maneiras debido ás variadas transliteracións dun apelido ruso en cirílico: reinhardi, reinhardii, reinhardti e reinhardtii (este último é o nome científico actual: C. reindhardtii Dangeard).[3] A especie foi descrita por P. A. Dangeard en 1888, que lle puxo ese nome en honor ao botánico ucraíno Ludwig Reinhard(t), que describiu en 1876 o apareamento desta especie (á cal el lle dera outro nome).[4]
C. reinhardtii, igual que as outras algas verdes, era clasificada tradicionalmemte como protista. Nas clasificacións actuais as algas verdes tenden a clasificarse xunto coas plantas, con varios nomes, segundo os autores, para o taxon superior no que se inclúen (por exemplo Viridiplantae ou Plantae).
Organismo modelo
editarCh. reindhardtii utilízase como organismo modelo para investigar cuestións fundamentais da bioloxía da célula e bioloxía molecular como:
- Como se moven as células.
- Como responden á luz.
- Como se recoñecen unhas a outras.
- Como xeran as células as ondulacións falxelares regulares e repetibles.
- Como regulan as células o seu proteoma para controlar a lonxitude do flaxelo.
- Como responden as células aos cambios na súa nutrición en minerais (xofre, nitróxeno etc.).
Coñécense moitos mutantes de C. reinhardtii. Estes mutantes son ferramentas útiles para estudar diversos procesos biolóxicos, como a motilidade flaxelar, a fotosíntese, e a síntese de proteínas. Como esta especie, e outras especies de Chlamydomonas, son normalmente haploides, os efectos das mutacións poden verse inmediatamente sen ter que facer máis cruzamentos.
En 2007, publicouse a secuencia xenómica nuclear completa de C. reinhardtii.[5]
As proteínas canalrodopsina-1 e canalrodopsina-2, que funcionan como canais iónicos de apertura controlada pola luz, illáronse orixinalmente de C. reinhardtii.[6][7]
Reprodución
editarAs células vexetativas de C. reinhardtii son haploides e teñen 17 pequenos cromosomas. Cando hai carencia de nitróxeno, as células vexetativas diferéncianse en gametos haploides.[8] As células pertencen a dous tipos de apareamento posibles, que son idénticos en aparencia, chamados mt(+) e mt(-), que se fusionan para formar un cigoto diploide. O cigoto non é flaxelado e funciona como unha forma dormente da especie no solo. En presenza de luz, o cigoto sofre meiose e orixina catro células haploides flaxeladas que reinician o ciclo de vida vexetativo.
En condicións de crecemento ideais, as células poden ás veces sufrir dúas ou tres mitoses antes de que as células fillas se liberen da vella parede celular. Así, nunha soa etapa de crecemento pode orixinar 4 ou 8 células fillas por cada célula nai.
O ciclo celular desta alga verde unicelular pode ser sincronizado alternando períodos de luz e escuridade. A fase de crecemento depende da luz, mentres que, despois dun punto chamado de transición ou de compromiso, os procesos son independentes da luz.[9]
Xenética
editarO atractivo que ten esta alga como organismo modelo incrementouse recentemente coa publicación de varios recursos xenómicos que pasaron a dominio público. O borrador Chlre3 da secuencia xenómica nuclear desta especie preparado polo Joint Genome Institute do Departamento de Enerxía dos Estados Unidos comprende 1557 armazóns cun total de 120 Mb. Aproximadamente a metade do xenoma está contido en 24 armazóns de polo menos 1,6 Mb de lonxitude cada un. A ensamblaxe actual do xenoma nuclear está dispoñible en liña.[10]
O xenoma mitocondrial (acceso á base de datos: NC_ 001638) está tamén dispoñible en liña na base de datos do NCBI.[11] O xenoma cloroplástico completo de >200 kb está igualmente dispoñible en liña.[12]
Ademais dos datos da secuencia xenómica, hai unha gran cantidade de datos de secuencias de expresión dispoñibles como librarías de ADNc e marcadores de secuencias expresadas (ESTs). En liña están dispoñibles sete destas librarías de ADNc.[13] A libraría BAC pode mercarse no Clemson University Genomics Institute.[14] Hai tamén dúas bases de datos en liña de >50.000 [15] e >160.000 ESTs.[16]
Evolución
editarChlamydomonas foi utilizada para estudar diferentes aspectos da bioloxía evolutiva e ecoloxía. É un organismo de elección para moitos experimentos de selección porque (1) ten un curto tempo de xeración, (2) funciona tanto como organismo heterótrofo coma de forma autótrofa facultativa, (3) pode reproducirse tanto sexualmente coma asexualmente, e (4) hai unha ampla información xenética dispoñible sobre ela.
Algúns exemplos (non exhaustivos) dos traballos evolutivos realizados con Chlamydomonas son a evolución da reprodución sexual,[17] o efecto na eficacia biolóxica ou fitness das mutacións,[18] e o efecto da adaptación a distintos niveis de CO2.[19]
Segundo unha hipótese frecuentemente citada,[20] a reprodución sexual (a diferenza da asexual) é mantida adaptativamente en ambientes favorables porque reduce a carga mutacional ao combinar mutacións deletéreas de diferentes liñas de descendencia e incrementa a fitness media. Porén, nun estudo experimental a longo prazo con C. reinhardtii, as probas obtidas contradín esa hipótese. Nas poboacións sexuais, non se atopou que houbese eliminación de mutacións e non se viu que se incrementase a fitness.[21]
Técnicas de transformación do ADN
editarA transformación xénica ocorre principalmente por recombinación homóloga nos cloroplastos e recombinación heteróloga no núcleo. O xenoma cloroplástico de C. reinhardtii pode ser transformado realizando un bombrdeo con partículas microproxectís ou por axitación con esferiñas de cristal, aínda que este último método é menos eficaz. O xenoma nuclear foi transformado con axitación con esferiñas de cristal e por electroporacón. O procedemento de bombardeo de partículas parece ser o método máis eficaz para introducir ADN no xenoma do cloroplasto. Isto débese probablemente a que o cloroplasto ocupa case a metade do volume da célula, o que fai que sexa unha grande diana para os microproxectís. A electroporación é a forma máis eficaz para introducir ADN no xenoma nuclear cunhas frecuencias de transformación máximas de dúas ordes de magnitude maiores que as obtidas usando o método da axitación con esferiñas de cristal.
Produción de produtos biofarmacéuticos
editarUtilizáronse células de Ch. reinhardtii transformadas por enxeñaría xenética para producir diversos compostos útiles, como unha proteína amiloide sérica de mamífero, e tamén un anticorpo humano, o factor de crecemento vascular humano, unha potencial vacina terapéutica do Papillomavirus humano 16,[22] unha potencial vacina da malaria,[23] e un fármaco de complexo deseño que podería utilizarse na loita contra o cancro.[24]
Fonte limpa para a produción de hidróxeno
editarEn 1939, o investigador alemán Hans Gaffron (1902–1979), que daquela traballaba na Universidade de Chicago, descubriu o metabolismo do hidróxeno das algas verdes unicelulares. Ch. reinhardtii e algunhas outras algas verdes poden, baixo espeiciais circunstancias, deixar de producir oxíxeno na fotosíntese e empezar a producir hidróxeno. Esta reacción feita pola hidroxenase, un encima que está activo só en ausencia de oxíxeno, ten curta duración. Nos seguintes trinta anos, Gaffron e o seu equipo descubriron a mecánica básica da produción fotosintética de hidróxeno feita polas algas.[25]
Para incrementar a produción de hidróxeno, os investigadores seguiron varios camiños:
- O primeiro camiño foi desacoplar a hidroxenase da fotosíntese. Deste xeito, a acumulación de oxíxeno xa non pode inhibir a produción de hidróxeno. E, se se vai un paso alén e se cambia a estrutura do encima hidroxenase, faise posible facer a hidroxenase insensible ao oxíxeno. Isto fai posible unha produción continua de hidróxeno. Nese caso, o fluxo de electróns necesario para a produción xa non procede da produción de azucres fotosintética senón que deriva da degradación das propias reservas acumuladas de amidón.[26]
- Unha segunda vía de investigación é interromper temporalmente o proceso da fotosíntese, por medio da manipulación xenética da hidroxenase. Isto impide que o oxíxeno chegue a un nivel no que podería causar a detención da produción de hidróxeno.[27]
- O terceiro camiño seguido, principalmente na década de 1950, son os métodos mecánicos ou químicos de eliminación do O2 producido pola actividade fotosintética das células das algas. Entre estes están a adición de eliminadores de O2, a adición de redutores, e a purga dos cultivos con gases inertes.[28] Con todo, estes métodos non son escalables, e non poden utilizarse en sistemas aplicados. Apareceron novas liñas de investigación sobre a eliminación do oxíxeno en cultivos de algas, que poden eliminar os problemas de escalabilidade.
- Unha cuarta liña de investigación usa sales de cobre para desacoplar a acción da hidroxenase da produción de oxíxeno.[29]
Notas
editar- ↑ "CC-125 wild type mt+ 137c". Chlamydomonas Center core collection list. Arquivado dende o orixinal o 27 de xullo de 2009. Consultado o 26 de decembro de 2014.
- ↑ The Chlamydomonas Sourcebook, ISBN 978-0-12-370873-1)
- ↑ http://megasun.bch.umontreal.ca/protists/chlamy/taxonomy.html Chlamydomonas Taxonomy.
- ↑ Elizabeth H. Harris. The Chlamydomonas Sourcebook: A Comprehensive Guide to Biology and Laboratory Use. Páxina 16. Google books. [1]
- ↑ Merchant; Prochnik, SE; Vallon, O; Harris, EH; Karpowicz, SJ; Witman, GB; Terry, A; Salamov, A; et al. (2007). "The Chlamydomonas Genome Reveals the Evolution of Key Animal and Plant Functions". Science 318 (5848): 245–250. PMC 2875087. PMID 17932292. doi:10.1126/science.1143609.
- ↑ Nagel G, Ollig D, Fuhrmann M; et al. (June 28, 2002). "Channelrhodopsin-1: a light-gated proton channel in green algae". S cience 296 (5577): 2395–8. PMID 12089443. doi:10.1126/science.1072068.
- ↑ Lagali PS, Balya D, Awatramani GB, Münch TA, Kim DS, Busskamp V, Cepko CL, Roska B (June 2008). "Light-activated channels targeted to ON bipolar cells restore visual function in retinal degeneration". Nature Neuroscience 11 (6): 667–75. PMID 18432197. doi:10.1038/nn.2117.
- ↑ SAGER R, GRANICK S (July 1954). "Nutritional control of sexuality in Chlamydomonas reinhardi". J. Gen. Physiol. 37 (6): 729–42. PMC 2147466. PMID 13174779. doi:10.1085/jgp.37.6.729.
- ↑ Oldenhof H, Zachleder V., den Ende H. (2006). "Blue- and red-light regulation of the cell cycle in Chlamydomonas reinhardtii (Chlorophyta)". Eur. J. Phycol 41: 313–320. doi:10.1080/09670260600699920.
- ↑ http://genome.jgi-psf.org/Chlre3/Chlre3.home.html
- ↑ http://www.ncbi.nlm.nih.gov/
- ↑ http://www.chlamy.org/chloro/default.html
- ↑ "Copia arquivada". Arquivado dende o orixinal o 19 de outubro de 2004. Consultado o 26 de decembro de 2014.
- ↑ "Copia arquivada". Arquivado dende o orixinal o 26 de decembro de 2014. Consultado o 26 de decembro de 2014.
- ↑ http://www.kazusa.or.jp/en/plant/chlamy/EST/
- ↑ "Copia arquivada". Arquivado dende o orixinal o 04 de febreiro de 2005. Consultado o 26 de decembro de 2014.
- ↑ Colegrave N (2002). "Sex releases the speed limit on evolution". Nature 420 (6916): 664–666. PMID 12478292. doi:10.1038/nature01191.
- ↑ De Visser et al. 1996 The effect of sex and deleterious mutations on fitness in Chlamydomonas. Proc. R. Soc. Lond. B 263-193-200.
- ↑ Collins , Bell (2004). "Phenotypic consequences of 1,000 generations of selection at elevated CO2 in a green alga". Nature 431: 566–569. doi:10.1038/nature02945.
- ↑ Kondrashov AS (October 1984). "Deleterious mutations as an evolutionary factor. 1. The advantage of recombination". Genet. Res. 44 (2): 199–217. PMID 6510714. doi:10.1017/s0016672300026392.
- ↑ Renaut S, Replansky T, Heppleston A, Bell G (November 2006). "The ecology and genetics of fitness in Chlamydomonas. XIII. Fitness of long-term sexual and asexual populations in benign environments". Evolution 60 (11): 2272–9. PMID 17236420. doi:10.1554/06-084.1.
- ↑ Demurtas OC, Massa S, Ferrante P, Venuti A, Franconi R, et al. (2013) A Chlamydomonas-Derived Human Papillomavirus 16 E7 Vaccine Induces SpecificTumor Protection. Arquivado 12 de outubro de 2013 en Wayback Machine. PLoS ONE 8(4): e61473. doi 10.1371/journal.pone.0061473
- ↑ (16 Maio 2012) Biologists produce potential malarial vaccine from algae PhysOrg, Retrieved 15 April 2013
- ↑ (10 de decembro de 2012) Engineering algae to make complex anti-cancer 'designer' drug PhysOrg, Retrieved 15 April 2013
- ↑ Anastasios Melis, Thomas Happe (2004). "Trails of green alga hydrogen research — from Hans Gaffron to new frontiers" (PDF). Photosynthesis Research 80 (1–3): 401–409. PMID 16328836. doi:10.1023/B:PRES.0000030421.31730.cb.
- ↑ Laurent Cournac, Florence Musa, Laetitia Bernarda, Geneviève Guedeneya, Paulette Vignaisb and Gilles Peltie (2002). "Limiting steps of hydrogen production in Chlamydomonas reinhardtii and Synechocystis PCC 6803 as analysed by light-induced gas exchange transients". International Journal of Hydrogen Energy 27 (11/12): 1229–1237. doi:10.1016/S0360-3199(02)00105-2.
- ↑ Anastasios Melis. "Hydrogen and hydrocarbon biofuels production via microalgal photosynthesis". Arquivado dende o orixinal o 03 de abril de 2008. Consultado o 2008-04-07.
- ↑ Kosourov, S. Tsyganov, A. Seibert, Ghirardi, M (June 2002). "Sustained Hydrogen Photoproduction by Chlamydomonas reinhardtii:Effects of Culture Parameters". Biotechnol. Bioeng. 78 (7): 731–40. PMID 12001165. doi:10.1002/bit.10254.
- ↑ Fernandez VM, Rua ML, Reyes P, Cammack R, Hatchikian EC. (November 1989). "Inhibition of Desulfovibrio gigas hydrogenase with copper salts and other metal ions". Eur. J. Biochem. 185 (2): 449–54. PMID 2555191. doi:10.1111/j.1432-1033.1989.tb15135.x.
Véxase tamén
editarBibliografía
editar- Aoyama, H., Kuroiwa, T. e Nakamura, S. 2009. The dynamic behaviour of mitochondria in living zygotes during maturation and meiosis in Chlamydomonas reinhardtii. Eur. J. Phycol. 44: 497 - 507.
- Jamers, A., Lenjou, M., Deraedt, P., van Bockstaele, D., Blust, R. e de Coen, W. 2009. Flow cytometric analysis of the cadmium-exposed green algae Chlamydomonas reinhadtii (Chlorophyceae). Eur. J. Phcol. 44: 54 - 550.
Ligazóns externas
editar- recursos sobre Chlamydomonas reinhardtii Arquivado 26 de decembro de 2014 en Wayback Machine.
- The Chlamydomonas Center - información xenómica, xenética e bibliográfica e colección de cultivos de Chlamydomonas.
- Chlamydomonas reinhardtii célula, vida, ciclo vital, cepas e tipos de apareamento
- eol 921552
- Guiry, M.D.; Guiry, G.M. (2008). "'Chlamydomonas reinhardtii'". AlgaeBase. World-wide electronic publication, National University of Ireland, Galway.