Colo uterino
O colo uterino ou colo do útero,[1] tamén chamado cérvix uterino (ou, abreviadamente, cérvix),[2] é unha parte do aparato reprodutor feminino formada pola porción inferior máis estreita do útero por onde este se comunica coa vaxina. Ten forma cilíndrica e cónica e fai protrusión na parede vaxinal superior. Aproximadamente a metade da súa lonxitude pode verse desde a vaxina co equipamento médico axeitado. O colo uterino ten unha abertura que permite que os espermatozoides e o fluído menstrual pasen a través del para entrar e saír do útero.[3] O cérvix produce a secreción dun moco espeso en determinados momentos do ciclo menstrual e no embarazo, que funciona como un tapón. O cancro de colo uterino é un dos cancros máis importantes na muller.
| Colo uterino | |
|---|---|
 | |
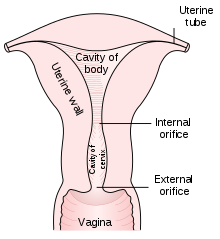
| Aparato reprodutor feminino en vista frontal | |
| Latín | cervix uteri |
| Gray's | pág.1259 |
| Sistema | Aparato reprodutor feminino |
| Arteria | arteria vaxinal, arteria uterina |
| Precursor | Conduto de Müller |
| MeSH | Cervix+uteri |
| Dorlands/Elsevier | cervix uteri |



Anatomía
editarDistínguense as seguintes partes:
Exocérvix ou ectocérvix
editarÉ a parte do colo uterino que se ve máis facilmente desde a vaxina nunha colposcopia. Está rodeado polos fondos da vaxina. Está cuberto por un epitelio escamoso estratificado rosa, de múltiples capas celulares. As capas celulares intermedia e superficial do epitelio escamoso conteñen glicóxeno, pero este epitelio non produce mucus.
Endocérvix
editarNon é visible en gran parte desde a vaxina, porque se encontra no centro do cérvix formando a canle endocervical que une o orificio cervical externo coa cavidade uterina. Está cuberto por un epitelio columnar ou cilíndrico avermellado dunha soa capa celular. Como media ten 3 cm de lonxitude e 2,5 cm de largura.
Orificio cervical externo
editarÉ o orificio que comunica a canle cervical do colo uterino co orificio cervical interno. Varía segundo o número de partos, e na muller que nunca pariu (nulípara) ten a forma dunha abertura circular de pouco diámetro, pero na muller multípara o aspecto cambia a causa dos desgarros do parto, adquirindo o aspecto de fenda transversal e estrelada en casos de desgarros oblicuos, que deforman a arquitectura do cérvix tendo como consecuencia a eversión do epitelio endocervical.
Canle endocervical
editarEsténdese desde o orificio cervical externo ata o orificio cervical interno, está revestido en todo o seu traxecto de epitelio endocervical columnar simple secretor de mucus, con células con núcleo basal e citoplasma cheo de moco e numerosas glándulas grandes mucosas. Esta abundante secreción fai que a súa luz estea ocluída totalmente polo moco cervical, constituíndo o chamado tapón mucoso endocervical, que impide que os xermes procedentes da vulva, vaxina e exocérvix ascendan aos xenitais internos; este tapón expúlsase ao comezo do parto ou pouco antes en forma de flegmas ou flegmas con sangue. A lonxitude da canle endocervical é variable, pero adoita medir de 7 a 8 mm de diámetro na zona máis larga nas mulleres en idade reprodutiva.
Orificio cervical interno
editarÉ o orificio que comunica a canle cervical co interior do útero. Non se observa a simple vista; cómpre facer unha ecografía transvaxinal para velo. Adoita medir non máis de 10 mm, delimita a canle endocervical co útero, a nivel dunha estrutura coñecida como istmo, durante o embarazo normal actúa como un esfínter, que ao fallar ocasiona unha incompetencia cervical con borramento e dilatación subseguinte do cérvix, provocando aborto tardío e nacemento prematuro.
Unión escamosa-columnar
editarTamén chamada unión escamo-cilíndrica ou cilindro-epidermoide. É a unión do epitelio columnar co escamoso e xeralmente está localizada no orificio cervical externo, pero varía segundo a idade, o momento do ciclo menstrual e outros factores como o embarazo e o uso de anticonceptivos orais. Esta é a chamada "zona de transición" ou "de transformación" dun epitelio a outro, que é o lugar de asentamento de frecuentes enfermidades como o cancro de colo uterino ou cancro cervical.
Histoloxía
editarO epitelio do cérvix é variado. O ectocérvix (parte máis distal que dá á vaxina) está composto por un epitelio escamoso estratificado non queratinizado. O endocérvix (máis proximal) está composto por un epitelio columnar simple produtor de mucus.[4] En certos momentos da vida, o epitelio columnar é substituído por un epitelio escamoso metaplásico, e é cando se chama zona de transformación.
A área adxacente ao bordo do endocérvix e ectocérvix coñécese como zona de transformación. A zona de transformación sofre metaplasia numerosas veces ao longo da vida normal. Cando o endocérvix se expón ao ambiente ácido da vaxina sofre metaplasia a un epitelio escamoso, que é máis axeitado para resistir as condicións vaxinais. De xeito similar, cando o ectocérvix pasa á zona menos hostil do interior do útero o epitelio faise columnar.
Os momentos da vida en que ocorre esta metaplasia da zona de transformación son:
- na puberdade; cando o endocervix se everte (móvese cara a fóra) do útero
- cos cambios do cérvix asociados co ciclo menstrual normal
- na posmenopausia; o útero encóllese movendo a zona de transformación cara a arriba.
Todos estes cambios son normais e a súa aparición dise que é fisiolóxica.
Porén, a metaplasia incrementa o risco de cancro nesta zona. A zona de transformación é a área máis común onde pode orixinarse o cancro cervical.
Os quistes de Naboth, de ata 5–6 mm de diámetro, fórmanse con frecuencia no cérvix como resultado da obliteración dos condutos dalgunhas glándulas produtoras de mucus.[5]
Moco cervical
editarO colo uterino produce unha secreción mucosa máis ou menos espesa segundo o momento do ciclo menstrual ou durante o embarazo. O moco cervical é nun 90% auga. Dependendo do seu contido de auga, que varía durante o ciclo menstrual, o mucus funciona como unha barreira ou como un medio de transporte para os espermatozoides. O moco cervical contén tamén electrólitos (calcio, sodio e potasio), compoñentes orgánicos como a glicosa, aminoácidos e proteínas solubles.[6]
O moco cervical contén trazas de elementos metálicos, como o cinc, cobre, ferro, manganeso e selenio, cuxos niveis varían dependendo da variación cíclica hormonal durante as diferentes fases do ciclo menstrual [7] Identificáronse varios encimas no moco cervical humano. Outro ingrediente orgánico do moco cervical é o glicerol.[8][9][10][11] Diversos estudos indicaron que a cantidade de glicerol no fluído cervical se incrementa durante a excitación sexual.[9] Este incremento de glicerol suxeriuse que é responsable das propiedades lubricantes do fluído cervical fértil e pode ser bioloxicamente relevante durante as primeiras fases da reprodución.
Despois de que remata un ciclo menstrual, o orificio externo do cérvix está bloqueado por un moco mesto e ácido. Este moco espeso denomínase moco "infértil" e bloquea o paso de espermatozoides en dirección ao útero.[12] Durante un período de varios días arredor do momento da ovulación, prodúcese moco de tipo "fértil", que ten un contido de auga maior, é máis fluído, menos ácido e con maior contido en electrólitos. Estes electrólitos causan un patrón en "folla de fento" que pode observarse no moco seco visto a poucos aumentos no microscopio, xa que conforme o moco vai secando, os sales cristalizan, e forman un debuxo que semella a folla dun fento.[13]
Nalgúns métodos de control da natalidade estímase o período de fertilidade feminina examinando os cambios nas propiedades do moco cervical (método Billings), entre outros cambios corporais: a súa sensación na vulva, sensación de humidade, a súa elasticidade (fibrosidade), transparencia, e a proba da "folla de fento" (un debuxo que forma o moco seco parecido ás follas desa planta visto ao microscopio).[13] Na fase folicular do ciclo o moco é escaso, pouco espeso, case transparente, pegañento e máis alcalino, pero durante o ciclo irá aumentando a súa elasticidade. Nos días previos á ovulación é moi elástico (forma fíos que se estiran sen romper) e ten unha consistencia parecida á clara de ovo, e denomínase "moco fértil", que facilita o paso dos espermatozoides e prodúcelle á muller unha sensación de humidade; coincide con niveis altos de estróxenos. Na fase lútea do ciclo o moco é branquecho, mesto, máis ácido e cremoso; coincide con niveis altos de proxesterona.
A maioría dos métodos de contracepción hormonal funcionan principalmente impedindo a ovulación, pero tamén impiden a formación de moco cervical de tipo "fértil", o que incrementa a súa efectividade. Inversamente, os métodos que rebaixan o espesor do moco poden axudar a conseguir un embarazo cando isto é o que se procura. Un dos métodos suxeridos é tomar guaifenesina poucos días antes da ovulación.[14]
Ademais dos cambios durante o ciclo menstrual, durante a xestación, o cérvix está bloqueado por un tapón de moco cervical especialmente espeso antibacteriano, que impide a infección. Na xestación fanse máis grandes as glándulas cervicais, que proliferan e producen gran cantidade de moco, e o tecido conxuntivo entre elas adelgaza moito. O tapón de moco despréndese cando o cérvix se dilata durante o parto ou pouco antes.
Posición cervical
editarDespois da menstruación e baixo a influencia directa dos estróxenos, o cérvix sofre unha serie de cambios de posición e textura. Durante a maior parte do ciclo menstrual, o cérvix permanece firme, dunha dureza similar á da punta do nariz, e está en posición baixa e pechada. Porén, cando unha muller se aproxima ao momento da ovulación, o cérvix faise máis suave, similar aos beizos, e elévase e ábrese en resposta aos niveis elevados de estróxenos presentes na ovulación.[15] Estes cambios, acompañados da produción de moco cerrvical de tipo fértil, favorecen a supervivencia e o desprazamento dos espermatozoides.
Función
editarDurante a menstruación o colo uterino estírase abríndose lixeiramente para permitir que o endometrio se desescame e saia a regra. Este estiramento crese que é responsable de parte das dores ou cambras que moitas mulleres experimentan nese momento. Unha proba disto é que as cambras dalgunhas mulleres diminúen ou desaparecen despois do seu primeiro parto vaxinal, porque a abertura cervical se amplía. Durante o parto, as contraccións do útero dilatan o cérvix ata os 10 cm en diámetro para permitir que o neno pase a través del.
Durante o orgasmo, pénsase que o cérvix ten convulsións e o orificio externo do cérvix dilátase. Robin Baker e Mark A. Bellis, da Universidade de Manchester, foron os primeiros en propoñer que este comportamento do cérvix tende a dirixir o seme que está na vaxina ao interior do útero, incrementando a probabilidade de que se produza a concepción.[16][17] Pero non todos están de acordo, e a historiadora da Ciencia Elisabeth Lloyd cuestiona a lóxica desta teoría e a calidade dos datos experimentais utilizados para apoiala.[18][19]
Os cérvix curtos [20] son o mellor signo para predicir un parto prematuro.[21][22][23] Algúns tratamentos para previr o cancro cervical, poden acurtar o cérvix.
Enfermidades
editarCancro cervical
editarA infección por papilomavirus humano (VPH ou HPV) é un factor necesario no desenvolvemento de case todos os casos de cáncer cervical ou de colo uterino. A vacina contra o papilomavirus pode reducir a probabilidade de desenvolver cancro cervical, se é administrada antes do inico da actividade sexual. Cambios potencialmente precancerosos no cérvix poden detectarse pola citoloxía vaxinal (frotis de Papanicolau), no cal as células epiteliais son raspadas da superficie do colo uterino e examinadas ao microscopio. Co tratamento apropiado das anormalidades que poidan ser detectadas, pode previrse o cancro cervical.
En todo o mundo, o cancro cervical é o quinto cancro con maior mortalidade nas mulleres.[24] Cada ano afecta a unhas 16 de cada 100.000 mulleres e mata a 9 de cada 100.000.[25] O frotis de Papanicolau reduciu moito a incidencia do cancro cervical e da súa mortalidade nas nacións que fan programas de prevención que inclúen esta proba. Tamén existen probas de ADN para detectar o papilomavirus.[26]
Tumores benignos
editarPrincipalmente pólipos endocervicais de tecido conxuntivo que infiltra as glándulas próximas ao endometrio.
Cervicite
editarA cervicite é unha inflamación do colo uterino aguda ou crónica, na maioría dos casos debida a infeccións microbianas patóxenas de gonococos, clamidias, Trichomonas vaginalis, Candida ou micoplasmas ; o ben por organismos saprófitos vaxinais como os estreptococos, enterococos e estafilococos. A cervicite aguda é común no puerperio.
Outras imaxes
editar-
Aparato reprodutor feminino.
-
Útero e trompas de Falopio.
Notas
editar- ↑ Diccionario galego de termos médicos. Real Academia de Medicina e Cirurxía de Galicia. Xunta de Galicia. 2002. Páxina 164. ISBN 84-453-3371-2
- ↑ Definición de Colo uterino no Dicionario de Galego de Ir Indo e a Xunta de Galicia.
- ↑ Health and Wellness for Life
- ↑ BUHistology - 19404loa
- ↑ Weschler, pp. 227–228.
- ↑ Wagner,G.& Levin, R. J. (1980). "Electrolytes in vaginal fluid during the menstrual cycle of coitally active and inactive women". J Reprod Fertil. (en inglés) 60 (1): 27–27. PMID 7431318.
- ↑ Hagenfeldt et al., 1973;Pandey et al., 1986.
- ↑ Volatile constituents of human vaginal secretions. Authors: George Huggins and George Preti (University of Pennsylvania School of Medicine). Am J Obstet Gynecol, 1976 Sep 1;126(1):129-36.
- ↑ 9,0 9,1 Alterations in the organic compounds of vaginal secretions caused by sexual arousal. Authors: George Preti, George Huggins and Geoffrey Silverberg (University of Pennsylvania School of Medicine). Fertil Steril 1979;32:47–54.
- ↑ Vaginal odors and secretions. Authors: George Huggins and George Preti (University of Pennsylvania School of Medicine). Clinical Obstetrics and Gynecology, 1981; 24; 355-377.
- ↑ A vaginal fluid simulant. Authors: Derek Owen and David Katz (Duke University). Contraception, 1999 Feb;59(2):91-5.
- ↑ Ann Westinore; Evelyn, Dr Billings (1998). The Billings Method: Controlling Fertility Without Drugs or Devices. Toronto: Life Cycle Books. p. 37. ISBN 0-919225-17-9.
- ↑ 13,0 13,1 Weschler, pp. 58–59.
- ↑ Weschler, p. 173.
- ↑ Weschler, Toni, MPH, Taking Charge of Your Fertility, Second Edition, 2002, pp. 59, 64.
- ↑ Singh D, Meyer W, Zambarano RJ, Hurlbert DF (1998). "Frequency and timing of coital orgasm in women desirous of becoming pregnant". Arch Sex Behav 27 (1): 15–29. PMID 9494687. doi:10.1023/A:1018653724159.
- ↑ Whipple, Beverly; Komisaruk, Barry R.; Beyer, Carlos; Carlos Beyer-Flores (2006). The science of orgasm. Baltimore: Johns Hopkins University Press. ISBN 0-8018-8490-X.
- ↑ Lloyd, Elisabeth Anne (2006). The Case of the Female Orgasm: Bias in the Science of Evolution. Cambridge: Harvard University Press. ISBN 0-674-02246-7.
- ↑ "The ideas interview: Elisabeth Lloyd". The Guardian (London). 2005-09-26. Consultado o 2010-04-28.
- ↑ Goldenberg RL, Iams JD, Mercer BM; et al. (1998). "The preterm prediction study: the value of new vs standard risk factors in predicting early and all spontaneous preterm births. NICHD MFMU Network". Am J Public Health 88 (2): 233–8. PMC 1508185. PMID 9491013. doi:10.2105/AJPH.88.2.233.
- ↑ To MS, Skentou CA, Royston P, Yu CKH, Nicolaides KH. Prediction of patient-specific risk of early preterm delivery using maternal history and sonographic measurement of cervical length: a population-based prospective study. Ultra Obstet Gynecol 2006; 27: 362–367.
- ↑ Fonseca et al. Progesterone and the risk of preterm birth among women with a short cervix. NEJM 2007; vol 357, no 5, pg 462–469.
- ↑ Romero, Roberto (2007-09-26). "Prevention of spontaneous preterm birth: the role of sonographic cervical length in identifying patients who may benefit from progesterone treatment". Ultrasound in Obstetrics and Gynecology (en inglés) 30 (5): 675–686. doi:10.1002/uog.5174. Arquivado dende o orixinal o 28 de maio de 2020. Consultado o 07 de abril de 2019.
- ↑ World Health Organization (2006). "Fact sheet No. 297: Cancer". Consultado o 2007-12-01.
- ↑ "GLOBOCAN 2002 database: summary table by cancer". Arquivado dende o orixinal o 16 de xuño de 2008. Consultado o 2008-10-26.
- ↑ Luis M. Puig-Tintoré. Utilización del test de VPH en el cribado primario del cáncer de cérvix. [1] Arquivado 08 de setembro de 2008 en Wayback Machine.
Véxase tamén
editarLigazóns externas
editar- My Beautiful Cervix—site with a series of photographs illustrating the cervix over a menstrual cycle. (en inglés)
- Proyecto bebé Imaxes sobre o aspecto do moco cervical en diferentes momentos. (en castelán)