Argonauta (proteína)
Argonauta (en inglés Argonaute) é unha familia proteica que desempeña un papel central no proceso de silenciamento do ARN, no cal as proteínas desta familia funcionan como compoñentes catalíticos esenciais do complexo silenciador inducido por ARN (RISC). O RISC é responsable do fenómeno de silenciamento de ARN chamado interferencia de ARN (RNAi). As proteínas Argonauta únense a diferentes clases de pequenos ARN non codificantes, como os microARNs (miRNAs), ARNs interferentes pequenos (siRNAs) e ARNs que interaccionan con piwi (piRNAs). Pequenos ARNs guían as proteínas Argonauta ás súas dianas específicas por medio de complementariedade de secuencia (apareamento de bases), o que despois producirá a clivaxe do ARN mensaxeiro ou a inhibición da tradución.
| Argonauta (proteína) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
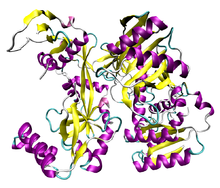 Unha proteína Argonauta da arquea Pyrococcus furiosus. PDB 1U04
. O dominio PIWI está á dereita e o dominio PAZ á esquerda. | |||||||||
| Identificadores | |||||||||
| Símbolo | Piwi | ||||||||
| Pfam | PF02171 | ||||||||
| InterPro | IPR003165 | ||||||||
| PROSITE | PS50822 | ||||||||
| CDD | cd02826 | ||||||||
| |||||||||
| Argonauta (proteína) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Paz | ||||||||
| Pfam | PF12212 | ||||||||
| InterPro | IPR021103 | ||||||||
| SCOPe | b.34.14.1 / SUPFAM | ||||||||
| |||||||||

Descubrimento
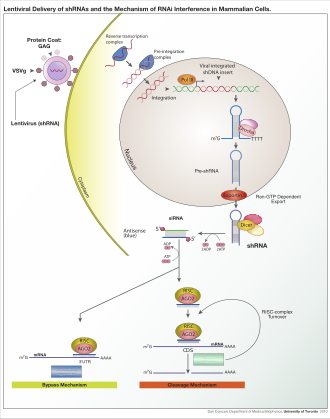
editarOs primeiros informes sobre a interferencia de ARN (RNAi) apareceron en 1995 obra de Guo e Kemphues, e vías similares denominadas en conxunto silenciamento do ARN descubríronse en plantas e fungos. Non se empezou a coñecer o mecanismo do silenciamento de ARN ata 1998 cos experimentos de Fire e os seus colegas, que demostraron que o ARN bicatenario desencadeaba a interferencia de ARN.[1] A vía do silenciamento do ARN procesa longos ARNs orixinando pequenos ARNs que dirixen a represión da transcrición ou tradución de ácidos nucleicos diana que teñen unha secuencia que se corresponde complementariamente coa dos mencionados ARNs pequenos. Estes ARNs monocatenarios, denominados febras guía, son incorporados nos complexos efectores silenciadores do ARN como o complexo silenciador inducido por ARN (RISC). Estes complexos efectores silenciadores do ARN conteñen proteínas da familia Argonauta.
Argonauta na interferencia de ARN
editarA interferencia de ARN é un importante proceso biolóxico no cal moléculas de ARN inhiben a expresión xénica. Este proceso realízase tipicamente causando a destrución de moléculas de ARNm específicas. A interferencia de ARN ten unha grande importancia na defensa das células contra secuencias nucleotídicas parasitas. En moitos eucariotas, incluíndo os animais existe esta vía de interferencia de ARN, que é iniciada polo encima Dicer. Dicer cliva moléculas longas de ARN bicatenario dando lugar a fragmentos bicatenarios curtos de arredor de 20 nucleótidos de siRNAs. As dúas febras do ARN bicatenario sepáranse despois orixinando dous ARN monocatenarios, que se denominan febra pasaxeira e febra guía. Seguidamente, a febra pasaxeira é degradada, mentres que a febra guía se incorpora ao complexo silenciador inducido por ARN (RISC). O resultado mellor estudado da interferencia de ARN é o silenciamento de xenes postranscricional, que ten lugar cando a febra guía se aparea cunha secuencia complementaria dunha molécula de ARNm e induce a clivaxe deste por parte da proteína Argonauta, que se encontra no núcleo do RISC.
As proteínas Argonauta son a parte activa do RISC, e clivan (cortan) a febra de ARNm diana complementaria do siRNA unido a elas.[2] Teoricamente o Dicer produce curtos fragmentos bicatenarios polo que deberían producirse dous siRNA monocatenarios funcionais. Pero só será utilizado un dos dous ARN monocatenarios para unirse por apareamento de bases co ARNm diana. Este é o que se denomina febra guía, que é incorporada na proteína Argonauta e produce o silenciamento xénico. O outro ARN monocatenario, chamado febra pasaxeira, é degradado durante os procesos do RISC.[3]
Unha vez que a Argonauta está asociada co pequeno ARN, a actividade encimática do dominio PIWI cliva só a febra pasaxeira do siRNA. A separación das febras do ARN e a incorporación á proteína Argonauta son guiadas pola forza das interaccións de pontes de hidróxeno no extremo 5' do dúplex de ARN, o que se coñece como regra da asimetría. Ademais, o grao de complementariedade entre as dúas febras do dúplex de ARN intermediario define como será distribuído o miARN nos diferentes tipos de proteína Argonauta.
En animais, a Argonauta asociada co miARN únese á rexión non traducida 3' (3'-UTR) do ARNm e impide a produción de proteínas de diversos modos. O recrutamento de proteínas Argonauta no ARNm diana pode inducir a degradación do ARNm. O complexo Argonauta-miARN pode tamén obstaculizar a formación de ribosomas funcionais no extremo 5' do ARNm. O complexo aquí compite con factores de iniciación da tradución ou impide a ensamblaxe do ribosoma. Ademais, o complexo Argonauta-miARN pode axustar a produción de proteínas ao recrutar factores celulares como péptidos ou encimas que realizan unha modificación postraducional, que degradan os polipéptidos en crecemento.[4]
Nas plantas, unha vez que se xeran os dúplex de ARN bicatenario de novo co ARNm diana, intervén un encima de tipo RNase III descoñecido, que produce novos siRNAs, os cales son despois cargados nas proteínas Argonauta que conteñen dominios PIWI, que carecen dos residuos de aminoácidos catalíticos, o cal podería inducir outro nivel de silenciamento de xenes específico.
Dominios funcionais das argonautas e mecanismos de acción
editarA familia de xenes Argonauta (AGO) codifica catro dominios característicos: N- terminal, PAZ, Mid e un dominio PIWI C-terminal.[5]
O dominio PAZ chámase así polas iniciais das proteínas PIWI, AGO, e Zwille, nas que é un dominio conservado. O dominio PAZ é un módulo de unión ao ARN que recoñece o extremo 3' de ARNs interferentes pequenos e microARNs, de maneira dependente de secuencia. En consecuencia, únese ao ARNm para a súa clivaxe ou inhibición da tradución por interacción de apareamento de bases.[6]
A proteína PIWI de Drosophila recibiu o seu nome porque presenta ese característico motivo. Lembra estruturalmente á RNaseH, e o dominio PIWI é esencial para a clivaxe da súa diana. O sitio activo ten a tríade aspartato-aspartato-glutamato que alberga un ión metálico, que é necesario para a catálise. Os membros da familia de AGO que perderon esta característica conservada durante a evolución carecen da actividade de clivaxe. Nas AGO humanas, o motivo PIWI tamén media a interacción proteína-proteína na caixa PIWI, onde se une a Dicer nun dos dominios de RNase III.[7]
Na interface dos dominios PIWI e Mid sitúase o extremo 5' fosfato dun ARN interferente pequeno ou dun microARN, que se considera esencial para o funcionamento do encima. No dominio Mid está un motivo MC, que é unha estrutura homóloga ao motivo da estrutura cap que se encontra en eIF4E. Probouse que o motivo MC intervén na unión da estrutura cap e, en consecuencia, no control da tradución.[5]
Membros da familia
editarNos humanos hai oito membros da familia Argonauta (AGO), algúns dos cales están a ser investigados intensamente. Porén, aínda que as proteínas AGO1 a AGO4 poden cargar miARN, a actividade de endonuclease e, por tanto, o silenciamento de xenes dependente de interferencia de ARN, encóntrase exclusivamente na proteína AGO2. Considerando a conservación de secuencia dos dominios PAZ e PIWI en toda a familia, a exclusividade de acción que presenta AGO2 crese que xurdiu ou no N-terminal ou na rexión espazadora que une os motivos PAZ e PIWI.[7]
Tamén se están facendo grandes esforzos de investigación para estudar varias familias AGO das plantas. AGO1 está claramente implicada na degradación do ARN relacionada con miARN, e xoga un papel central na morfoxénese. Nalgúns organismos, é estritramente necesaria para o silenciamento epixenético. Un dato interesante é que está regulada polo propio miARN. AGO4 non está implicada na degradación de ARN dirixida por interferencia de ARN, senón na metilación do ADN e outras regulacións epixenéticas, por medio dunha vía de pequenos ARN (smRNA). AGO10 está implicada no desenvolvemento das plantas. AGO7 ten unha función distinta de AGO 1 e 10, e non se encontrou que interveña en silenciamento de xenes inducido por transxenes, senón que está relacionada coa temporalización do desenvolvemento nas plantas.[8]
Doenzas e ferramentas terapéuticas
editarPara as doenzas nas que está implicada unha expresión elevada ou selectiva dun xene identificado determinado, como o cancro pancreático, a alta especificidade de secuencia da interferencia do ARN debería facela axeitada para o tratamento desas doenzas, e especialmente apropiada para combater cancros asociados con secuencias de xenes endóxenos mutados. Informouse que varios pequenos ARNs non codificantes (microARNs) están relacionados con cancros humanos, xa que o miR-15a e o miR-16a están frecuentemente ausentes ou regulados á baixa nos pacientes. Aínda que as funcións biolóxicas daos miARNs non se comprenden totalmente, descubríronse as funcións dos miARNs na coordinación da proliferación celular e a morte celular durante o desenvolvemento e no metabolismo. Confíase en que os miARNs poidan dirixir regulacións positivas ou negativas a diferentes niveis, o cal depende dos miARNs específicos e interaccións de apareamento de bases coa diana e os cofactores que os recoñecen.[9]
Como moitos virus teñen como material xenético ARN en vez de ADN e pasan polo menos por unha etapa do seu ciclo vital no que teñen ARN bicatenario, a interferencia de ARN foi considerada como un posible mecanismo evolutivo antigo que protexía aos organismos contra os virus. Os ARN interferentes pequenos producidos pola proteína Dicer causan silenciamento de xenes postranscricional específico de secuencia ao guiar unha endonuclease (o RISC) ao ARNm. Este proceso obsevouse nunha ampla gama de organismos, como o fungo Neurospora (no cal se coñece como quelling), plantas (silenciamento de xenes postranscricional) e células de mamífero (interferencia de ARN). Se hai unha secuencia con complementariedade completa ou case completa entre o pequeno ARN e a diana, a proteína Argonauta compoñente do RISC media a clivaxe do transcrito diana; o mecanismo implica predominantemente a represión da tradución.
Notas
editar- ↑ Guo, S.; Kemphues, K.J. (1995). "par-1, a gene required for establishing polarity in C. elegans embryos, encodes a putative Ser/Thr kinase that is asymmetrically distributed". Cell 81 (4): 611–620. PMID 7758115. doi:10.1016/0092-8674(95)90082-9.
- ↑ Kupferschmidt, K. (2013). "A Lethal Dose of RNA". Science 341 (6147): 732–3. PMID 23950525. doi:10.1126/science.341.6147.732.
- ↑ Gregory R, Chendrimada T, Cooch N, Shiekhattar R (2005). "Human RISC couples microRNA biogenesis and posttranscriptional gene silencing". Cell 123 (4): 631–40. PMID 16271387. doi:10.1016/j.cell.2005.10.022.
- ↑ Hutvagner, Gyorgy; et al. "Argonaute proteins: key players in RNA silencing". Nature Reviews Molecular Cell Biology 9 (1): 22–32. doi:10.1038/nrm2321.
- ↑ 5,0 5,1 Hutvagner, Gyorgy; Simard, Martin J. "Argonaute proteins: key players in RNA silencing". Nature Reviews Molecular Cell Biology 9 (1): 22–32. doi:10.1038/nrm2321.
- ↑ Tang, G (February 2005). "siRNA and miRNA: an insight into RISCs.". Trends in Biochemical Sciences 30 (2): 106–14. PMID 15691656. doi:10.1016/j.tibs.2004.12.007.
- ↑ 7,0 7,1 Meister, Gunter; Landthaler, Markus; Patkaniowska, Agnieszka; Dorsett, Yair; Teng, Grace; Tuschl, Thomas (Jul 2004). "Human Argonaute2 Mediates RNA Cleavage Targeted by miRNAs and siRNAs". Molecular Cell 15 (2): 185–197. PMID 15260970. doi:10.1016/j.molcel.2004.07.007.
- ↑ Meins F, Jr; Si-Ammour, A; Blevins, T (2005). "RNA silencing systems and their relevance to plant development.". Annual review of cell and developmental biology 21 (1): 297–318. PMID 16212497. doi:10.1146/annurev.cellbio.21.122303.114706.
- ↑ Hannon, GJ (2002). "RNA interference". Nature 418 (6894): 244–51. PMID 12110901. doi:10.1038/418244a.
Véxase tamén
editarLigazóns externas
editar- starBase database: base de datos para explorar os mapas de interaccións microARN–ARNm de Argonaute CLIP-Seq (HITS-CLIP, PAR-CLIP) e Degradome-Seq data.