Hidroperoxilo
O radical hidroperoxilo, tamén chamado radical perhidroxilo, é un radical que é a forma protonada do superóxido e ten a fórmula HO2. Esta especie química xoga un importante papel na atmosfera terrestre e, como especie reactiva do oxíxeno, en bioloxía celular.[2]
| Hidroperoxilo | |
|---|---|
 | |
 | |
Dioxidanil | |
Outros nomes Radical peroxilo | |
| Identificadores | |
| Número CAS | 3170-83-0 |
| PubChem | 520535 |
| ChemSpider | 454055 |
| ChEBI | CHEBI:25935 |
| Referencia Gmelin | 506 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | HO2 |
| Masa molar | 33,01 g mol−1 |
| Acidez (pKa) | 4,88[1] |
| Basicidade (pKb) | 9,12 (basicidade do ión superóxido) |
| Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
Estrutura e reaccións
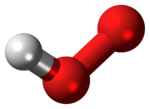
editarA molécula ten unha estrutura dobrada nun ángulo duns 104º.[3]
O anión superóxido, O−
2 e o radical hidroperoxilo coexisten en equilibrio químico en solución acuosa:
- O−
2 + H2O ⇌ HO2 + OH−
A pKa do HO2 é 4,88. Por tanto, un 0,3% dos superóxidos presentes no citosol dunha célula típica están en forma protonada.[4]
Oxida o óxido nítrico a dióxido de nitróxeno:[2]
- NO + HO2 → NO2 + HO
Especies reactivas do oxíxeno en bioloxía
editarXunto coa súa base conxugada superóxido, o hidroperoxilo é unha importante especie reactiva do oxíxeno. A diferenza do O−
2, que ten propiedades redutoras, o HO2 pode actuar como oxidante en varias reaccións biolóxicas importantes, como a abstracción de átomos de hidróxeno do tocoferol e de ácidos graxos poliinsaturados na bicapa lipídica da membrana celular, polo que pode ser un importante iniciador da peroxidación de lípidos.
Importancia na química atmosférica
editarO hidroperoxilo gasoso está implicado en ciclos de reaccións que destrúen o ozono estratosférico. Tamén está presente na troposfera, onde esencialmente é o subproduto da oxidación do monóxido de carbono e de hidrocarburos polo radical hidroxilo.[5]
Como a constante dieléctrica ten un forte efecto sobre o pKa, e a constante dieléctrica do aire é bastante baixa, o superóxido producido (fotoquimicamente) na atmosfera está presente case exclusivamente en forma de HO2. Como o HO2 é bastante reactivo, actúa como un "limpador" na atmosfera ao degradar certos contaminantes orgánicos, polo que a química do HO2 é de considerable importancia xeoquímica.
Notas
editar- ↑ "Reactivity of HO2/O−
2 Radicals in Aqueous Solution". J. Phys. Chem. Ref. Data 14 (4): 1041–1091. 1985. - ↑ 2,0 2,1 Heard, Dwayne E.; Pilling, Michael J. (2003). "Measurement of OH and HO2 in the Troposphere". Chemical Reviews 103: 5163–5198. doi:10.1021/cr020522s.
- ↑ Liskow, Dean H.; Schaefer, Henry F., III; Bender, Charles F. (1971). "Geometry and electronic structureof the hydroperoxyl Radical". Journal of the American Chemical Society 93: 6734–7. doi:10.1021/ja00754a003.
- ↑ De Grey, Aubrey D. N. J. (2002). "HO2·: The Forgotten Radical". DNA and Cell Biology 21: 251–257. doi:10.1089/104454902753759672.
- ↑ "Hydroperoxyl radical". Glossary of Meteorology. American Meteorological Society. 25 April 2012. Consultado o 22 August 2013.