Lípido de membrana
Os lípidos de membrana son un grupo de compostos (estruturalmene similares ás graxas e aceites) que forman a dobre capa que forma a membrana plasmática de todas as células (a bicapa lipídica). As tres clases principais dos lípidos de membrana son fosfolípidos, glicolípidos e colesterol. Estes lípidos son anfifílicos: teñen un extremo que é afín á auga (polar) e outro extremo que é soluble en graxas (non polar). Ao formaren a dobre capa cos extremos polares dirixidos á parte externa da bicapa e os extremos non polares dirixidos cara ao interior, lonxe do contacto coa auga, manteñen o interior acuoso da célula separado do exterior acuoso. A disposición dos lípidos e varias proteínas, serve para que actúen como receptores e poros canles na membrana, controlando a entrada e saída doutras moléculas e ións como parte do metabolismo das células. Para realizar funcións fisiolóxicas, as proteínas de membrana poden rotar e difundir lateralmente nas dúas dimensións da bicapa lpídica pola presenza dunha cuberta de lípidos estreitamente pegados á superficie da proteína, chamados capa ou cuberta lipídica anular. Os lípidos tamén teñen mobilidade na membrana.
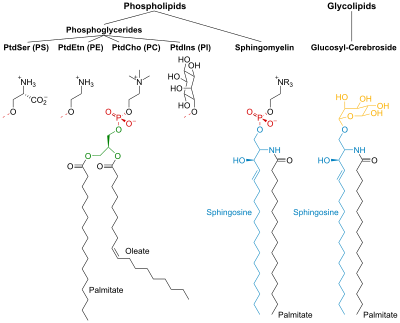
PtdCho - fosfatidilcolina; PtdEtn - fosfatidiletanolamina; PtdIns - fosfatidilinositol; PtdSer - fosfatidilserina.
Funcións biolóxicas editar
A bicapa lipídica formada polos lípidos de membrana serve como unidade de contención para a célula viva. Os lípidos de membrana tamén forman unha matriz na cal se encontran as proteínas de membrana. Historicamente os lípidos pensábase que exercían simplemente un papel estrutural. En realidade, os papeis funcionais dos lípidos son moitos: serven como axentes reguladores no crecemento e adhesión celular; participan na biosíntese doutras biomoléculas, e poden servir para incrementar a actividade de encimas.[1]
Os lipidos que non forman bicapas, como o monogalactosil diglicérido (MGDG) predominan na masa de lípidos das membranas dos tilacoides. Porén, en combinación con outros lípidos e carotenoides/clorofilas das membranas dos tilacoides, tamén conforman as bicapas lipídicas.[2]
Principais clases editar
Fosfolípidos editar
Os fosfolípidos e glicolípidos constan de dúas cadeas hidrocarbonadas longas non polares (hidrófobas) ligadas a un grupo cabeza hidrófila.
As cabezas dos fosfolípidos son fosforilados e poden constar de:
- Glicerol (e, por iso denomínanse fosfoglicéridos), ou
- Esfingosina (por exemplo nas esfingomielinas e ceramidas).
O glicerol dialquil glicerol tetraéter (GDGT) axuda a estudar os factores ambientais de tempos antigos.[3]
Glicolípidos editar
As cabezas dos glicolípidos conteñen unha esfingosina con unha ou varias unidades de azucre unidas a ela. As cadeas hidrófobas poden ser:
- dous ácidos graxos, no caso dos fosfoglicéridos, ou
- un ácido graxo e a cola hidrocarbonada da esfingosina, no caso da esfingomielina e os glicolípidos.
Os galactolípidos monogalactosil diglicérido (MGDG) e digalactosil diglicérido (DGDG) forman os lípidos predominantes nas membranas dos tilacoides de plantas superiores; as estruturas liposómicas formadas por un extracto de lípidos total da membrana dos tilacoides son sensibles á sacarosa a medida que as bicapas se transforman en estruturas micelares.[4]
Ácidos graxos editar
Os ácidos graxos de fosfolípidos e glicolípidos xeralmente conteñen un número par, normalmente entre 14 e 24, de átomos de carbono, sendo os máis comúns os de 16 e 18. Os ácios graxos poden ser saturados ou insaurados, cunha configuración dos dobres enlaces case sempre cis. A lonxitude e grao de saturación das cadeas de ácidos graxos teñen un profundo efecto na fluidez das membranas. As membranas dos tilacoides das plantas manteñen unha alta fluidez, incluso a temperaturas ambientais relativamente frías, debido á abundacia de cadeas de acilo graxos de 18 carbonos con tres dobres enlaces, como o ácido linolénico, como revelaron estudos de 13-C NMR.[5]
Fosfoglicéridos editar
Nos fosfoglicéridos, os grupos hidroxilo en C1 e C2 do glicerol están esterificados aos grupos carboxilo dos ácidos graxos. O grupo hidroxilo C3 está esterificado por un ácido fosfórico. O composto resultante, chamado fosfatidato, é o fosfoglicerato máis simple. Soamente están presentes pequenas cantidades de fosfatidato nas membranas. Porén, é un intermediario clave na biosíntese doutros fosfoglicéridos.
Esfingolípidos editar
A esfingosina é un amino alcohol que contén unha longa cadea hidrocarbonada insaturada. Na esfingomielina e os glicolípidos, o grupo amino da esfingosina está unida aos ácidos graxos por un enlace amida. Na esfingomielina o grupo hidroxilo primario da esfingosina está esterificado á fosforil colina.
Nos glicolípidos, o compoñente azucre está unido a este grupo. O glicolípido máis simple é o cerebrósido, no cal hai só un residuo de azucre, que pode ser glicosa ou galactosa. Glicolípidos máis complexos como os gangliósidos, conteñen unha cadea ramificada feita de ata sete residuos de azucres.
Esterois editar
O esterol mellor coñecido é o colesterol, que se encontra en humanos e outros eucariotas, pero non en membranas de plantas ou de procariotas. Os esterois teñen unha estrutura ríxida de catro ciclos hidrófoba e unha pequena cabeza polar.
O colesterol biosintetízase a partir do mevalonato por medio da ciclación do terpenoide escualeno. As membranas celulares requiren altos niveis de colesterol, xeralmente unha media dun 20% de colesterol na membrana completa, incrementándose localmente en áreas de balsa lipídica que chegan ao 50% de colesterol (a % é a razón molecular aquí).[6] Asóciase preferencialmente cos esfingolípidos (ver diagrama) nas áreas de balsa lipídica ricas en colesterol das membranas das células eucariotas.[7] A formación de balsas lipídicas promove a agregación de proteínas transmembrana e periféricas de membrana, incluíndo as proteínas de atraque SNARE e VAMP proteins.[8] Os fitoesterois, como o sitoesterol e estigmasterol nas plantas e os hopanoides nos procariotas exercen funcións similares.
Véxase tamén editar
Outros artigos editar
Notas editar
- ↑ R. B. Gennis. Biomembranes - Molecular Structure and Function. Springer-Verlag, New York (1989).
- ↑ YashRoy R.C. (1990) Lamellar dispersion and phase separation of chloroplast membrane lipids by negative staining electron microscopy. Journal of Biosciences, vol. 15(2), pp. 93-98.https://www.researchgate.net/publication/230820037_Lamellar_dispersion_and_phase_separation_of_chloroplast_membrane_lipids_by_negative_staining_electron_microscopy?ev=prf_pub
- ↑ Weijers; et al. (2007). "Environmental controls on bacterial tetraether membrane lipid distribution in soils". Geochimica et Cosmochimica Acta 71 (3): 703–713. Bibcode:2007GeCoA..71..703W. doi:10.1016/j.gca.2006.10.003.
- ↑ YashRoy R.C. (1994) Destabilisation of lamellar dispersion of thylakoid membrane lipids by sucrose. Biochimica et Biophysica Acta, vol. 1212, pp. 129-133.https://www.researchgate.net/publication/15042978_Destabilisation_of_lamellar_dispersion_of_thylakoid_membrane_lipids_by_sucrose?ev=prf_pub
- ↑ YashRoy R.C. (1987) 13-C NMR studies of lipid fatty acyl chains of chloroplast membranes. Indian Journal of Biochemistry and Biophysics, vol. 24(6), pp. 177-178.https://www.researchgate.net/publication/230822408_13-C_NMR_studies_of_lipid_fatty_acyl_chains_of_chloroplast_membranes?ev=prf_pub
- ↑ de Meyer F, Smit B. Effect of cholesterol on the structure of a phospholipid bilayer. Proc Natl Acad Sci U S A 2009; 106: 3654-8.
- ↑ Chen, Heshun; Born, Ella; Mathur, Satya N.; Field, F. Jeffrey (1 de decembro de 1993). "Cholesterol and sphingomyelin syntheses are regulated independently in cultured human intestinal cells, CaCo-2: role of membrane cholesterol and sphingomyelin content" (PDF). Journal of Lipid Research (American Society for Biochemistry and Molecular Biology) 34 (12): 2159–67. ISSN 0022-2275. PMID 8301234. doi:10.1016/S0022-2275(20)35356-6.
- ↑ Lang T, Bruns D, Wenzel D, Riedel D, Holroyd P, Thiele C, Jahn R. SNAREs are concentrated in cholesterol-dependent clusters that define docking and fusion sites for exocytosis EMBO J 2001;20:2202-13.
Ligazóns externas editar
| Wikimedia Commons ten máis contidos multimedia na categoría: Lípido de membrana |
- Membrane lipids Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.