Citocromo
Os citocromos son, en xeral, hemoproteínas que conteñen grupos hemo unidas a membranas (como a membrana mitocondrial interna), que interveñen principalmente no transporte de electróns necesario para crear as condicións para xerar ATP.
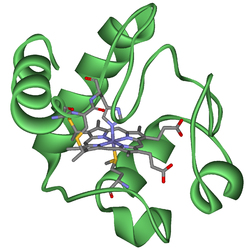
Atópanse como proteínas monoméricas (como o citocromo c) ou como subunidades proteicas de complexos encimáticos maiores que catalizan reaccións redox.
Historia editar
Os citocromos foron descritos inicialmente en 1884 por MacMunn como pigmentos respiratorios (miohematina ou histohematina).[1] Na década de 1920, Keilin redescubriu estes pigmentos respiratorios e denominounos citocromos, ou “pigmentos celulares”, e clasificou estas hemoproteínas baseándose na posición da súa banda de absorción de enerxía máis baixa no estado reducido, como citocromos a (605 nm), b (~565 nm), e c (550 nm). As sinaturas espectroscópicas UV-visible dos hemos aínda se usan para identificar os tipos de hemo desde o estado ligado a bis piridina reducido, é dicir, o método hemocromo piridina. En cada un dos tipos de citocromo, a, b, ou c, os primeiros citocromos descubertos son numerados consecutivamente, por exemplo, cyt c, cyt c1, e cyt c2, e os exemplos máis recentes desígnanse polo seu máximo de banda R do estado reducido, por exemplo cyt c559.[2]
Estrutura e función editar
O grupo hemo é un sistema de aneis altamente conxugado (o que permite que os seus electróns sexan moi móbiles) que rodea un ión metálico, o cal facilmente se interconverte entre distintos estados de oxidación. Para moitos citocromos, o ión metálico presente é o ferro, que se interconverte entre os estados de Fe2+ (reducido) e Fe3+ (oxidado) (procesos de transferencia de electróns) ou entre os estados de Fe2+ (reducido) e Fe3+ (formal, oxidado) (procesos oxidativos). Os citocromos poden realizar reaccións redox. Como os citocromos (e outros complexos) están dentro de membranas en forma organizada, as reaccións redox son levadas a cabo na correcta secuencia para a máxima eficiencia ; algúns citocromos son máis móbiles e solubles, e só se unen feblemente a membranas, como o c.
No proceso da cadea de transporte de electróns e a fosforilación oxidativa, que é o principal proceso xerador de enerxía que levan a cabo os organismos, outros complexos unidos a membrana e solubles e cofactores están implicados na cadea de reaccións redox, co efecto adicional neto dun bombeo de protóns (H+), que se transportan a través da membrana mitocondrial interna. O gradiente de protóns transmembrana (forza protón-motriz) utilízase para xerar ATP nas mitocondrias.
Tipos editar
Hai varios tipos de citocromos que se poden distinguir por espectroscopía, estrutura exacta do seu grupo hemo, sensibilidade aos inhibidores, e potencial de redución.
Podemos distinguir tres tipos de citocromos polos seus grupos prostéticos:
| Tipo | grupo prostético | comentario |
| Citocromo a | hemo a | Os citocromos a da cadea de transporte de electróns están asociados a átomos de cobre, que serán oxidados/reducidos polos Fe das porfirinas, mais nunca o Cu formará parte dos grupos hemo. |
| Citocromo b | hemo b | |
| Citocromo d | quelato tetrapirrólico de ferro[3] |
Existe tamén o citocromo c, que non se define polo seu grupo hemo.[4] Hai tamén un citocromo f, que se considera un tipo de citocromo c, pero non existe o "citocromo e".[5] O citocromo c contén o grupo hemo c, que, a diferenza dos outros hemos, se une directamente (e non por enlaces coordinados) á proteína, concretamente por medio de dúas cisteínas que forman dous enlaces tiol.
Nas mitocondrias e cloroplastos, estes citocromos están a miúdo combinados na cadea de transporte electrónico e vías metabólicas relacionadas. Orixínase as seguintes combinacións:
| Citocromos | Combinación |
| a e a3 | Citocromo c oxidase ("Complexo IV") no que os electróns son cedidos ao complexo polo citocromo c soluble |
| b e c1 | Coencima Q-citocromo c redutase ("Complexo III") |
| b6 e f | Plastoquinol-plastocianina redutase |
Citocromo P450 editar
- Artigo principal: Citocromo P450.
Unha familia de citocromos completamente distinta, con funcións catalíticas que non intervén na cadea respiratoria, é a do citocromo P450, chamado así polo seu característico pico de absorbancia de luz na lonxitude de onda dos 450 nm cando o ferro do hemo é reducido (con sodio ditionito) e acomplexado co monóxido de carbono. Estes encimas, abreviados como CYPs, están implicados principalmente na esteroidoxénese e na detoxificación.
Notas editar
- ↑ Mac Munn, C. A (1886). "Researches on Myohaematin and the Histohaematins". Philosophical Transactions of the Royal Society of London (The Royal Society) 177 (0): 267–298. JSTOR 109482. doi:10.1098/rstl.1886.0007.
- ↑ Reedy, C. J. & Gibney, B. R. (February 2004). "Heme protein assemblies". Chem Rev 104 (2): 617–49. PMID 14871137. doi:10.1021/cr0206115.
- ↑ Cytochrome d Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- ↑ Cytochrome c Group Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA. .
- ↑ eMedicineDictionary Cytochrome Arquivado 08 de marzo de 2014 en Wayback Machine.
Véxase tamén editar
Ligazóns externas editar
- Base de datos Scripps de metaloproteínas
- Cytochromes Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.