Carbaril
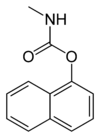
O carbaril (1-naftil metilcarbamato ; carbaryl) é un composto químico da familia dos carbamatos usado principalmente como insecticida. É ilegal na Unión Europea, pero non noutros países.[3] Tamén se usa como medicamento veterinario. É un sólido cristalino branco.
| Carbaril | |
|---|---|
|

|
Outros nomes Carbaryl, | |
| Identificadores | |
| Número CAS | 63-25-2 |
| PubChem | 6129 |
| ChemSpider | 5899 |
| UNII | R890C8J3N1 |
| Número CE | 200-555-0 |
| Número UN | 2757 |
| KEGG | D07613 |
| ChEBI | CHEBI:3390 |
| ChEMBL | CHEMBL46917 |
| Número RTECS | FC5950000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C12H11NO2 |
| Masa molar | 201,22 g mol−1 |
| Aspecto | Sólido cristalino incoloro |
| Densidade | 1,2 g/cm3 |
| Punto de fusión | 142 °C; 288 °F; 415 K |
| Punto de ebulición | descomponse |
| Solubilidade en auga | moi baixa (0,01% a 20 °C)[1] |
| Perigosidade | |
| Pictogramas GHS |    
|
| Palabra sinal GHS | Danger (Perigo) |
| Punto de inflamabilidade | 193-202 |
| LD50 | 710 mg/kg (coello, oral) 250 mg/kg (coello de Indias, oral) 850 mg/kg (rata, oral) 759 mg/kg (can, oral) 500 mg/kg (rata, oral) 150 mg/kg (gato, oral) 128 mg/kg (rato, oral) 230 mg/kg (rata, oral)[2][1] |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |

Historia editar
Antes vendíase co nome comercial Sevin, que era unha marca da Compañía Bayer. A marca Sevin foi despois adquirida por GardenTech, que eliminou o carbaril como ingrediente da maioría das formulacións de Sevin.[4][5] Union Carbide descubriu o carbaril e introduciuno no mercado en 1958. Bayer mercou Aventis CropScience en 2002, unha empresa que incluía operacións co pesticida de Union Carbide. O carbaril pasou a ser un insecticida moi utilizado; por exemplo, en EUA era o terceiro máis usado en xardíns domésticos, agricultura comercial e protección forestal e de pasteiros.
Produción editar
O carbaril adoita producirse de forma barata por reacción indirecta de metil isocianato con 1-naftol.[6]
- C10H7OH + CH3NCO → C10H7OC(O)NHCH3
Alternativamente, o 1-naftol pode ser tratado cun exceso de fosxeno para producir 1-naftilcloroformato, que se converte despois en carbaril por reacción con metilamina.[6] O proceso anterior era o que se levaba a cabo na fábrica sinistrada en 1984 de Bhopal. En comparación, o último tipo de síntese usa exactamente os mesmos reactivos, pero en diferente secuencia, o que evita os posibles perigos do metil isocianato.
Bioquímica editar
Os insecticidas de carbamato son inhibidores lentamente reversibles do encima acetilcolinesterase. Parécense á acetilcolina, pero o encima carbamoilado sofre o paso de hidrólise final moi lentamente (minutos) comparado co encima acetilado xerado pola acetilcolina (microsegundos). Interfire co sistema nervioso colinérxico e causa a morte debido a que os efectos do neurotransmisor acetilcolina non poden ser causados pola acción da acetilcolinesterase carbamoilada.
Aplicacións editar
O desenvolvemento de insecticidas carbamatos considerouse un gran logro na industria dos pesticidas. Os carbamatos non teñen a persistencia dos pesticidas clorados. Aínda que e tóxico para os insectos, o carbaril é detoxificado e eliminado rapidamente polos vertebrados. Non se concentra nas graxas nin se segrega no leite, polo que é o favorecido en cultivos de alimentos en países como os EUA.[7] É o ingrediente activo do xampú Carylderm usado para combater os piollos da cabeza ata que se elimina a infestación.[8]
Ecoloxía editar
O carbaril mata tanto insectos prexudiciais (por exemplo, os mosquitos transmisores da malaria) coma insectos beneficiosos (por exemplo, abellas), e tamén mata crustáceos.[9] Como é moi tóxico para o zooplancto, as algas das que este se alimentaba experimentan floracións. Boone e Bridges en 2003 atoparon que os comedores de algas máis grandes como o sapo Bufo woodhousii benefícianse deste efecto.[10]
O seu uso está aprobado para máis de 100 cultivos nos Estados Unidos, pero é ilegal na Unión Europea[3] e Angola.[11]
Seguridade editar
O carbaril é un inhibidor da colinesterase e é tóxico para os humanos. Está clasificado como probablemente carcinóxeno pola Axencia de Proteción Ambiental dos Estados Unidos (EPA.)[12] O seu LD50 oral é de 250 a 850 mg/kg para ratas e de 100 a 650 mg/kg para ratos.[9]
O carbaril pode producirse usando metil isocianato (MIC) como intermediario.[6] Unha fuga de MIC usado na produción de carbaril causou o sonado desastre de Bhopal na India, o accidente industrial máis letal da historia, acontecido en 1984.[13]
Notas editar
- ↑ 1,0 1,1 "NIOSH Pocket Guide to Chemical Hazards #0100". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "Carbaryl". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ 3,0 3,1 "L_2007133EN.01004001.XML".
- ↑ "When Familiar Pesticides Change".
- ↑ "When is Sevin not Sevin?". 14 de febreiro de 2018.
- ↑ 6,0 6,1 6,2 Thomas A. Unger (1996). Pesticide Synthesis Handbook (fragmento de Google Books). William Andrew. pp. 67–68. ISBN 0-8155-1401-8.
- ↑ Robert L. Metcalf "Insect Control" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2002. doi 10.1002/14356007.a14_263
- ↑ Carbaryl against lice
- ↑ 9,0 9,1 Carbaryl General Fact Sheet - National Pesticide Information Center
- ↑ Kendall, Ronald; Lacher, Thomas E.; Cobb, George P.; Cox, Stephen B., eds. (2010). Wildlife Toxicology: Emerging Contaminant and Biodiversity Issues. Boca Raton: CRC. ISBN 978-1-4398-1794-0. OCLC 646404494. 5.4.1 Taxon-Wide Impacts — Pesticides and Contaminants, and Their Roles in the Decline of Amphibian Populations. Moore, Robin D.; Claude Gascon. pp. 111-145.
- ↑ Carbaryl Insecticide Hazard Data Arquivado 11 de maio de 2010 en Wayback Machine.
- ↑ Interim Reregistration Eligibility Decision for Carbaryl Arquivado 25 de xullo de 2008 en Wayback Machine., U.S. EPA, Xuño de 2003.
- ↑ Eckerman, Ingrid (2005). The Bhopal Saga—Causes and Consequences of the World's Largest Industrial Disaster. India: Universities Press. ISBN 81-7371-515-7. doi:10.13140/2.1.3457.5364.
Véxase tamén editar
Ligazóns externas editar
- Carbaryl Technical Fact Sheet - National Pesticide Information Center
- Carbaryl Pesticide Information Profile - Extension Toxicology Network
- Cholinesterase Inhibition - Extension Toxicology Network
- EPA info
- EPA factsheet
- IPCS (WHO) Health and Safety Guide
- Environmental Health Criteria - WHO
- Exclusive Chemistry Ltd - routes of Sevin synthesis
- CDC - NIOSH Pocket Guide to Chemical Hazards